 理科(高校生)
理科(高校生)
 理科(高校生)
理科(高校生)
【現役講師による詳しい解説と講評!】2024年共通テスト化学基礎解答解説〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#大学入試過去問(化学)#共通テスト#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
3rd School
問題文全文(内容文):
2024年共通テスト化学基礎解説動画です
この動画を見る
2024年共通テスト化学基礎解説動画です
有機化学第36回【最終回】 芳香族化合物の分離②(問題演習

単元:
#化学#有機#芳香族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
有機化学第36回【最終回】 芳香族化合物の分離②(問題演習)
※図は動画内参照
この動画を見る
有機化学第36回【最終回】 芳香族化合物の分離②(問題演習)
※図は動画内参照
【2024年共通テスト解答速報(2日目)】日本最速解答速報LIVE|数学ⅠA→ⅡB→物理 ※冒頭7分55秒まで音声が乱れております。申し訳ございません。

単元:
#大学入試過去問(数学)#物理#センター試験・共通テスト関連#共通テスト#大学入試過去問(物理)#数学(高校生)#理科(高校生)#大学入試解答速報#数学#共通テスト#物理#共通テスト#共通テスト
指導講師:
理数個別チャンネル
問題文全文(内容文):
10000人登録目指しています。
何卒チャンネル登録お願いします!!!
※冒頭7分55秒まで音声が乱れております。申し訳ございません。
◆解答のまとめ◆
https://note.com/kobetsu_teacher/n/nf15e55b4c121
◆出演者◆
・TAKAHASHI名人
https://www.youtube.com/playlist?list=PLdLgDY469Qr7UEbDX8OecmSefwQulR35t
・ゆう☆たろう
https://www.youtube.com/playlist?list=PLdLgDY469Qr5zKa9ZgI9StW_-cNtbBDsn
・烈's study
https://www.youtube.com/playlist?list=PLdLgDY469Qr7QbP6MrNjpltLkbkyaggpv
・理数大明神
https://www.youtube.com/playlist?list=PLdLgDY469Qr6TpcFul6_A9hu5xZ1bQjNU
◆スタッフ◆
しまだじろう
https://www.youtube.com/playlist?list=PLdLgDY469Qr5kqaeicgkr6YhPZdkMEB3k
◆ドーナツ差し入れありがとう!!◆
岡ちゃん先生
https://www.youtube.com/playlist?list=PLdLgDY469Qr4OulJQO0KGCDMdykOS6pnX
◎対数の領域の問題で間違えた方はこちらを是非見てください!
(インタビューで烈's study!先生が言っていた動画です)
https://youtu.be/ZAXcZQC_sjw
◎ベクトルで間違えた方はこちらを是非見てください!
(インタビューでゆう☆たろう先生が言っていた動画です)
https://youtu.be/CYcQZEYqXj8
produced by 質問解決DB
https://kaiketsu-db.net/
produced by 理数個別チャンネル
https://www.youtube.com/@UCdQ0y9lyNRKcbH8dv2janrw
この動画を見る
10000人登録目指しています。
何卒チャンネル登録お願いします!!!
※冒頭7分55秒まで音声が乱れております。申し訳ございません。
◆解答のまとめ◆
https://note.com/kobetsu_teacher/n/nf15e55b4c121
◆出演者◆
・TAKAHASHI名人
https://www.youtube.com/playlist?list=PLdLgDY469Qr7UEbDX8OecmSefwQulR35t
・ゆう☆たろう
https://www.youtube.com/playlist?list=PLdLgDY469Qr5zKa9ZgI9StW_-cNtbBDsn
・烈's study
https://www.youtube.com/playlist?list=PLdLgDY469Qr7QbP6MrNjpltLkbkyaggpv
・理数大明神
https://www.youtube.com/playlist?list=PLdLgDY469Qr6TpcFul6_A9hu5xZ1bQjNU
◆スタッフ◆
しまだじろう
https://www.youtube.com/playlist?list=PLdLgDY469Qr5kqaeicgkr6YhPZdkMEB3k
◆ドーナツ差し入れありがとう!!◆
岡ちゃん先生
https://www.youtube.com/playlist?list=PLdLgDY469Qr4OulJQO0KGCDMdykOS6pnX
◎対数の領域の問題で間違えた方はこちらを是非見てください!
(インタビューで烈's study!先生が言っていた動画です)
https://youtu.be/ZAXcZQC_sjw
◎ベクトルで間違えた方はこちらを是非見てください!
(インタビューでゆう☆たろう先生が言っていた動画です)
https://youtu.be/CYcQZEYqXj8
produced by 質問解決DB
https://kaiketsu-db.net/
produced by 理数個別チャンネル
https://www.youtube.com/@UCdQ0y9lyNRKcbH8dv2janrw
これほんまなん?

単元:
#化学#化学理論#物質の三態と状態変化#理科(高校生)
指導講師:
【楽しい授業動画】あきとんとん
問題文全文(内容文):
カナダで水が綺麗に凍る動画が本当なのかに関して解説していきます。
この動画を見る
カナダで水が綺麗に凍る動画が本当なのかに関して解説していきます。
1分で解いてほしい化学計算問題 (39) ポリマーの完全燃焼

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 京都薬科大学B方式(改)]
重合度$n$が$1.2×10^4$のポリイソプレン$1.7g$を完全燃焼させたとき、発生する二酸化炭素は最大何$g$か、四捨五入して小数第1位まで求めよ。
ただし、両末端の置換基を考慮する必要はない。
※イソプレンの化学式:$H_2C=C(CH_3)-CH=CH_2$
原子量 $H=1.0 C=12 O=16$
この動画を見る
[2023年 京都薬科大学B方式(改)]
重合度$n$が$1.2×10^4$のポリイソプレン$1.7g$を完全燃焼させたとき、発生する二酸化炭素は最大何$g$か、四捨五入して小数第1位まで求めよ。
ただし、両末端の置換基を考慮する必要はない。
※イソプレンの化学式:$H_2C=C(CH_3)-CH=CH_2$
原子量 $H=1.0 C=12 O=16$
【高校物理】毎日原子10日目【共通テストまで毎日19時投稿】
単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
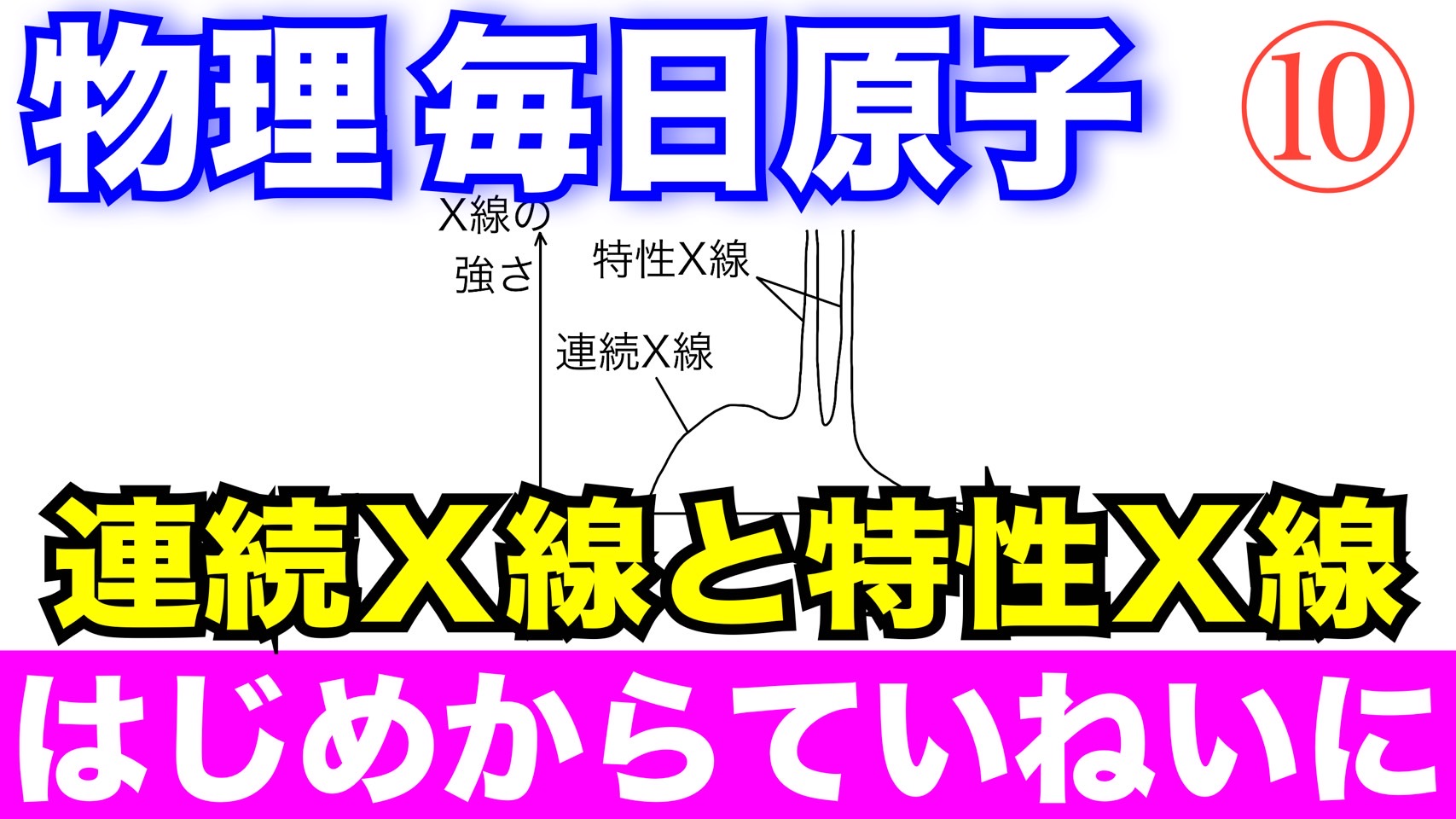
X線管において、初速度0の電子を電圧1.5kVで加速し、陽極金属に衝突させると、X線が発生して、図のようなスペクトルが得られた。電気素量を$1.6×10^{-19}$[C]、プランク定数を$6.6×10^{-34}$[J・s]、真空中の光速を$3.0×10^8$[m/s]とする。次の各問に答えよ。
(1) 加速された電子のもつエネルギーは何eVか。
(2) 連続X線の最短波長はいくらか。
(3) 加速電圧を3倍にしたとき、次の値は何倍になるか。
① 連続X線の最短波長 ② 特性X線の波長
宿題
右図は、X線管によって発生したX線のスペクトルである。プランク定数をh、光速をcとする。
(1) 右図の①、②に適当な語句を入れよ。
(2) 初速度0で陰極を出た電子(電気量−e)を電圧Vで加速し、陰極に当てたとき、陰極から放出されるX線光子の持つ最大エネルギーを求めよ。
(3)(2)のとき、X線の最短波長λ₀はいくらか。
(4) ②X線の波長をλ₁、λ₂とすると、加速電圧Vを大きくしても変化しないのは、λ₀、λ₁、λ₂ のどれか。
この動画を見る
X線管において、初速度0の電子を電圧1.5kVで加速し、陽極金属に衝突させると、X線が発生して、図のようなスペクトルが得られた。電気素量を$1.6×10^{-19}$[C]、プランク定数を$6.6×10^{-34}$[J・s]、真空中の光速を$3.0×10^8$[m/s]とする。次の各問に答えよ。
(1) 加速された電子のもつエネルギーは何eVか。
(2) 連続X線の最短波長はいくらか。
(3) 加速電圧を3倍にしたとき、次の値は何倍になるか。
① 連続X線の最短波長 ② 特性X線の波長
宿題
右図は、X線管によって発生したX線のスペクトルである。プランク定数をh、光速をcとする。
(1) 右図の①、②に適当な語句を入れよ。
(2) 初速度0で陰極を出た電子(電気量−e)を電圧Vで加速し、陰極に当てたとき、陰極から放出されるX線光子の持つ最大エネルギーを求めよ。
(3)(2)のとき、X線の最短波長λ₀はいくらか。
(4) ②X線の波長をλ₁、λ₂とすると、加速電圧Vを大きくしても変化しないのは、λ₀、λ₁、λ₂ のどれか。
【化学】古い過去問 センター試験2002年度 第2問 問1 ヘンリーの法則

単元:
#化学#化学理論#気体の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
温度一定で、圧力を変えて、一定量の水に溶解する窒素の量を調べた。
下のグラフに、窒素の圧力(横軸)と、溶解した窒素の量(縦軸)の関係を示す。
次の問い(a・b)に答えよ。
ただし、窒素は理想気体とみなす。
a 溶解した窒素の量を物質量で示すグラフとして、
最も適当なものを、次の①~④のうちから一つ選べ。
b 溶解した窒素の量をそのときの圧力における体積で示すグラフとして、
最も適当なものを、次の①~④のうちから一つ選べ。
※(a・b)のグラフは動画内参照
この動画を見る
温度一定で、圧力を変えて、一定量の水に溶解する窒素の量を調べた。
下のグラフに、窒素の圧力(横軸)と、溶解した窒素の量(縦軸)の関係を示す。
次の問い(a・b)に答えよ。
ただし、窒素は理想気体とみなす。
a 溶解した窒素の量を物質量で示すグラフとして、
最も適当なものを、次の①~④のうちから一つ選べ。
b 溶解した窒素の量をそのときの圧力における体積で示すグラフとして、
最も適当なものを、次の①~④のうちから一つ選べ。
※(a・b)のグラフは動画内参照
【高校物理】毎日原子9日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
定常状態の水素原子では、質量m、電気量-eの電子が、電気量+eの原子核(陽子)の周りを、半径r、速さvで等速円運動していると考えられる。クーロンの法則の比例定数をkとすると、円運動の式は(1)となる。また、電子は粒子であると同時に、波の性質ももっていて、プランク定数を h とすると、その波長λはλ=(2)となる。この波動性に対して、ボーアは(3)の条件を満たしていると考えた。ただし、nは自然数とする。以上の関係式からrとnの関係に注目すると、rは(4)に比例し、軌道半径はnによって定まる不連続な値しかとり得ないことがわかった。
この動画を見る
定常状態の水素原子では、質量m、電気量-eの電子が、電気量+eの原子核(陽子)の周りを、半径r、速さvで等速円運動していると考えられる。クーロンの法則の比例定数をkとすると、円運動の式は(1)となる。また、電子は粒子であると同時に、波の性質ももっていて、プランク定数を h とすると、その波長λはλ=(2)となる。この波動性に対して、ボーアは(3)の条件を満たしていると考えた。ただし、nは自然数とする。以上の関係式からrとnの関係に注目すると、rは(4)に比例し、軌道半径はnによって定まる不連続な値しかとり得ないことがわかった。
【高校物理】毎日原子5日目「放射線の進路」の宿題を解いてみた【番外編】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
図のように,真空中に放射線源と磁石を配置した。α線,β線,γ線の放射線が放射線源から鉛直上向きに飛び出したとすると,各々の放射線の進路はどのようになるか,図の(a)~(c)から選べ。
この動画を見る
図のように,真空中に放射線源と磁石を配置した。α線,β線,γ線の放射線が放射線源から鉛直上向きに飛び出したとすると,各々の放射線の進路はどのようになるか,図の(a)~(c)から選べ。
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第6問 問2 イオン交換樹脂
単元:
#化学#大学入試過去問(化学)#共通テスト#化学(高分子)#合成樹脂とゴム#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
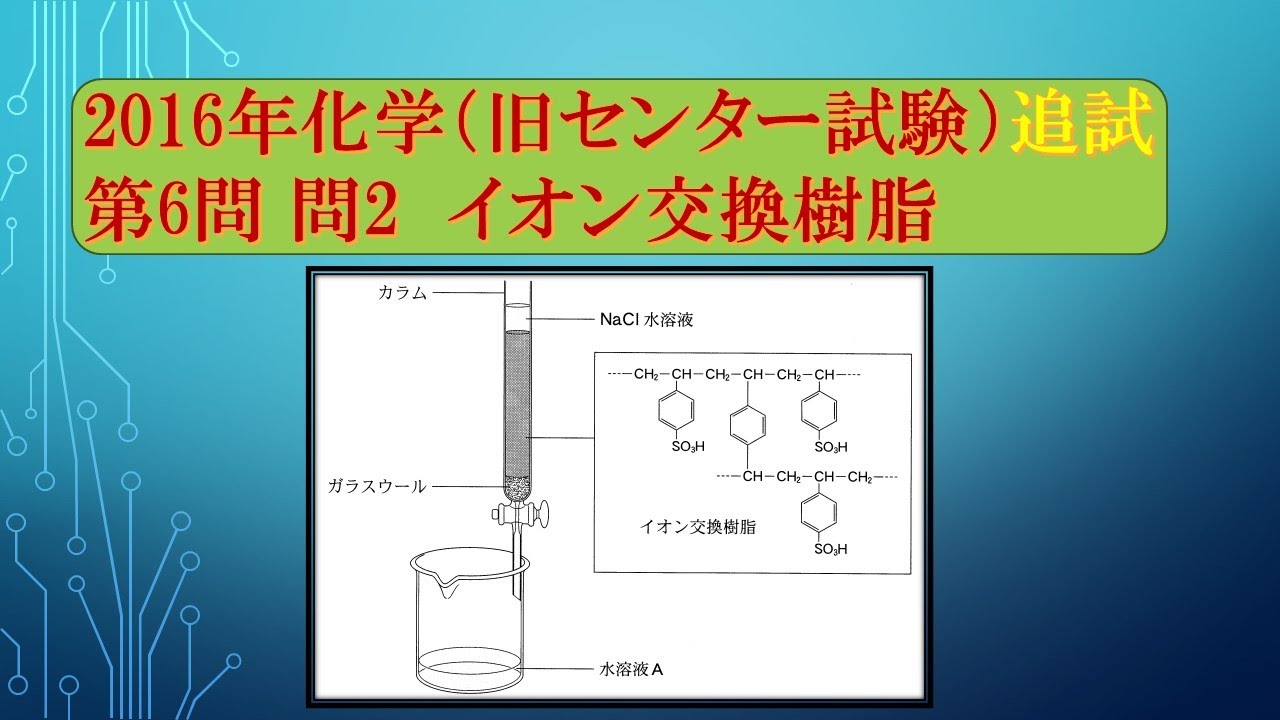
$NaCl$ 水溶液を、図1に示すイオン交換樹脂をつめたカラムに通して、イオン交換された水溶液Aを得た。
この水溶液の性質(液性)と、Aに含まれる。
水素イオンと水酸化物イオン以外のイオンの組合せとして最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、イオン交換樹脂は水溶液に含まれるイオンの量に対して十分な量を用いたものとする。
※図・表は動画内参照
この動画を見る
$NaCl$ 水溶液を、図1に示すイオン交換樹脂をつめたカラムに通して、イオン交換された水溶液Aを得た。
この水溶液の性質(液性)と、Aに含まれる。
水素イオンと水酸化物イオン以外のイオンの組合せとして最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、イオン交換樹脂は水溶液に含まれるイオンの量に対して十分な量を用いたものとする。
※図・表は動画内参照
【高校物理】毎日原子8日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
図のように格子面の間隔(格子定数)が$d$で、原子が規則的に配列している結晶に、波長$λ$の特性$X$線が格子面に対して角$\theta$で入射している。
(1) 格子面1、格子面2で反射した2つのX線の経路差を$d、\theta$を用いて表せ。
(2) 反射$X$線の強めあう条件を、$d、\theta、λ$、正の数$n(=1、2、…)$を用いて表せ。
(3) $θ$を0°から大きくしていくと、$\theta=\theta_0$のとき、はじめて反射$X$線が強めあった。格子定数$d$を、$\theta_0、λ$を用いて表せ。
この動画を見る
図のように格子面の間隔(格子定数)が$d$で、原子が規則的に配列している結晶に、波長$λ$の特性$X$線が格子面に対して角$\theta$で入射している。
(1) 格子面1、格子面2で反射した2つのX線の経路差を$d、\theta$を用いて表せ。
(2) 反射$X$線の強めあう条件を、$d、\theta、λ$、正の数$n(=1、2、…)$を用いて表せ。
(3) $θ$を0°から大きくしていくと、$\theta=\theta_0$のとき、はじめて反射$X$線が強めあった。格子定数$d$を、$\theta_0、λ$を用いて表せ。
【高校物理】毎日原子6日目「光電効果」の宿題を解いてみた【番外編】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
仕事関数が1.8[eV]の金属の表面に真空中での波長が$4.0×10^{-7}$[m]の光を当てる。真空中の光の速さをc=$3.0×10^8$[m/s],プランク定数をh=$6.6×10^{-34}$[J・s],電気素量を$1.6×10^{-19}$[C]とする。この光の光子1個のエネルギーは□.□[eV]である。金属の表面から飛び出した光電子の最大の運動エネルギーは□.□[eV]である。
この動画を見る
仕事関数が1.8[eV]の金属の表面に真空中での波長が$4.0×10^{-7}$[m]の光を当てる。真空中の光の速さをc=$3.0×10^8$[m/s],プランク定数をh=$6.6×10^{-34}$[J・s],電気素量を$1.6×10^{-19}$[C]とする。この光の光子1個のエネルギーは□.□[eV]である。金属の表面から飛び出した光電子の最大の運動エネルギーは□.□[eV]である。
【高校物理】毎日原子3日目「半減期」の宿題を解いてみた【番外編】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
古代遺跡から発掘された植物体内の$^{14}C$ の$^{12}C$ に対する割合は,大気中のそれの0.71倍であった。この発掘された植物は今からおよそ何年前に生育していたものと推定されるか。これを有効数字2桁で表すとき,次の式中の空欄ア〜ウに入れる数字として最も適当なものを答えよ。ただし,$^{14}C$ のβ崩壊の半減期は$5.73×10^3$年であり,大気中の$^{14}C$ と$^{12}C$ の割合は常に一定とする。また,$\frac{1}{\sqrt{2}}=0.71$である。$ □ .□×10^□$
この動画を見る
古代遺跡から発掘された植物体内の$^{14}C$ の$^{12}C$ に対する割合は,大気中のそれの0.71倍であった。この発掘された植物は今からおよそ何年前に生育していたものと推定されるか。これを有効数字2桁で表すとき,次の式中の空欄ア〜ウに入れる数字として最も適当なものを答えよ。ただし,$^{14}C$ のβ崩壊の半減期は$5.73×10^3$年であり,大気中の$^{14}C$ と$^{12}C$ の割合は常に一定とする。また,$\frac{1}{\sqrt{2}}=0.71$である。$ □ .□×10^□$
1分で解いてほしい化学計算問題 (38) 混合気体の燃焼

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 京都先端科学大学]
メタンとの混合気体$100mL$を空気中で完全燃焼させ、二酸化炭素が$180mL$生成した。
混合気体中に含まれていたプロパンの体積は何$mL$か。
次の①~⑤のうちから最も近い値を一つ選びなさい。
ただし、気体の体積はすべて標準状態$(0℃,1.013 ×10^5Pa )$のものとする。
$① 10 ② 20 ③ 40 ④ 60 ⑤ 80$
この動画を見る
[2023年 京都先端科学大学]
メタンとの混合気体$100mL$を空気中で完全燃焼させ、二酸化炭素が$180mL$生成した。
混合気体中に含まれていたプロパンの体積は何$mL$か。
次の①~⑤のうちから最も近い値を一つ選びなさい。
ただし、気体の体積はすべて標準状態$(0℃,1.013 ×10^5Pa )$のものとする。
$① 10 ② 20 ③ 40 ④ 60 ⑤ 80$
これホンマなん?
【高校物理】毎日原子7日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
図のように、波長λ[m]のX線を質量m[kg]の静止している電子に向けて入射したとき、電子は図のθの方向に速さv〔m/s)でたたき出され、入射線はθ’の方向に波長でλ’[m]となって散乱されたとする。プランク定数をh[J・s]、光速をc[m/s]とする。
(1) X線の入射方向の運動量保存則を表せ。
(2) X線の入射方向に垂直な方向の運動量保存則を表せ。
(3) 衝突前後のエネルギー保存の法則を表せ。
宿題
真空中に静止していた質量 m[kg]の電子に波長λ[m]のX線光子を衝突させる。
電子はX線の入射方向 θ の角をなす方向に速さ v[m/s]ではね飛ばされ、X線光子は
入射方向と垂直な方向に波長λ’[m]となって散乱された。光速をc[m/s]、プラ
ンク定数をh[J・s]とする。
(1)衝突前後のエネルギー保存則を表せ。
(2)X線の入射方向に関する運動量保存則を表せ。
(3)X線の入射方向に垂直な方向に関する運動量保存則を表せ。
この動画を見る
図のように、波長λ[m]のX線を質量m[kg]の静止している電子に向けて入射したとき、電子は図のθの方向に速さv〔m/s)でたたき出され、入射線はθ’の方向に波長でλ’[m]となって散乱されたとする。プランク定数をh[J・s]、光速をc[m/s]とする。
(1) X線の入射方向の運動量保存則を表せ。
(2) X線の入射方向に垂直な方向の運動量保存則を表せ。
(3) 衝突前後のエネルギー保存の法則を表せ。
宿題
真空中に静止していた質量 m[kg]の電子に波長λ[m]のX線光子を衝突させる。
電子はX線の入射方向 θ の角をなす方向に速さ v[m/s]ではね飛ばされ、X線光子は
入射方向と垂直な方向に波長λ’[m]となって散乱された。光速をc[m/s]、プラ
ンク定数をh[J・s]とする。
(1)衝突前後のエネルギー保存則を表せ。
(2)X線の入射方向に関する運動量保存則を表せ。
(3)X線の入射方向に垂直な方向に関する運動量保存則を表せ。
有機化学第35回 芳香族化合物の分離①(基本的な考え方)

単元:
#化学#有機#芳香族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
考え方:塩は水層、塩でなければエーテル層
①$+Cℓ$
②$+NaHCO_3$
③$+NaOH$
※図は動画内参照
この動画を見る
考え方:塩は水層、塩でなければエーテル層
①$+Cℓ$
②$+NaHCO_3$
③$+NaOH$
※図は動画内参照
【高校物理】毎日原子6日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
仕事関数が2.0[eV]の金属の表面に波長$4.0×10^{-7}$[m]の光を当てた。プランク定数をh=$6.6×10^{-34}$[J・s]、真空中の光の速さをc=$3.0×10^8$[m/s]、電気素量を$1.6×10^{-19}$[C]とする。金属の表面から飛び出してくる電子の運動エネルギーの最大値は□.□[eV]である。
宿題
仕事関数が1.8[eV]の金属の表面に真空中での波長が$4.0×10^{-7}$[m]の光を当てる。真空中の光の速さをc=$3.0×10^8$[m/s],プランク定数をh=$6.6×10^{-34}$[J・s],電気素量を$1.6×10^{-19}$[C]とする。この光の光子1個のエネルギーは□.□[eV]である。金属の表面から飛び出した光電子の最大の運動エネルギーは□.□[eV]である。
この動画を見る
仕事関数が2.0[eV]の金属の表面に波長$4.0×10^{-7}$[m]の光を当てた。プランク定数をh=$6.6×10^{-34}$[J・s]、真空中の光の速さをc=$3.0×10^8$[m/s]、電気素量を$1.6×10^{-19}$[C]とする。金属の表面から飛び出してくる電子の運動エネルギーの最大値は□.□[eV]である。
宿題
仕事関数が1.8[eV]の金属の表面に真空中での波長が$4.0×10^{-7}$[m]の光を当てる。真空中の光の速さをc=$3.0×10^8$[m/s],プランク定数をh=$6.6×10^{-34}$[J・s],電気素量を$1.6×10^{-19}$[C]とする。この光の光子1個のエネルギーは□.□[eV]である。金属の表面から飛び出した光電子の最大の運動エネルギーは□.□[eV]である。
【短時間でテスト・共通テスト前の最終チェック!!】生物基礎確認事項の全まとめ〔現役塾講師解説、高校生物、生物基礎、2024年度版〕

単元:
#生物#大学入試過去問(生物)#共通テスト・センター試験#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
共通テスト直前、生物基礎で確認するべき内容をまとめています!
短時間で復習できるように速いスピードで進めていますので、速いと感じた場合は0.75倍速などでご覧ください
この動画を見る
共通テスト直前、生物基礎で確認するべき内容をまとめています!
短時間で復習できるように速いスピードで進めていますので、速いと感じた場合は0.75倍速などでご覧ください
【化学】硫酸の濃度換算

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
密度18.6g/cm³、質量パーセント濃度98%濃硫酸のモル濃度を求めよ
$H_2SO_4$の分子量98.0
この動画を見る
密度18.6g/cm³、質量パーセント濃度98%濃硫酸のモル濃度を求めよ
$H_2SO_4$の分子量98.0
理系的に空気を読むには?

共通テスト(旧センター試験)過去問解説 化学 2016年追試 第6問 問1 繰り返し単位の数

単元:
#化学#大学入試過去問(化学)#共通テスト#化学(高分子)#合成繊維と天然繊維#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
高分子化合物の平均分子量は、その希薄水溶液の浸透圧から求めることができる。
いま、(繰り返し単位の式量$44$) $0.50g$を水に溶解させて$50mL$とした希薄水溶液の浸透圧は、$27℃$で$8.3×10^2 Pa$であった。
このポリビニルアルコールの平均重合度として最も適当な数値を、 次の①~⑥のうちから一つ選べ。
ただし、気体定数は$R = 8.3×10^3Pa・L/(K・mol )$とする。
①$6.2 ×10^2$
②$6.8 ×10^2$
③$6.2 ×10^3$
④$6.8 ×10^3$
⑤$6.2 ×10^4$
⑥$6.8 ×10^4$
この動画を見る
高分子化合物の平均分子量は、その希薄水溶液の浸透圧から求めることができる。
いま、(繰り返し単位の式量$44$) $0.50g$を水に溶解させて$50mL$とした希薄水溶液の浸透圧は、$27℃$で$8.3×10^2 Pa$であった。
このポリビニルアルコールの平均重合度として最も適当な数値を、 次の①~⑥のうちから一つ選べ。
ただし、気体定数は$R = 8.3×10^3Pa・L/(K・mol )$とする。
①$6.2 ×10^2$
②$6.8 ×10^2$
③$6.2 ×10^3$
④$6.8 ×10^3$
⑤$6.2 ×10^4$
⑥$6.8 ×10^4$
【高校物理】毎日原子5日目【共通テストまで毎日19時投稿】
単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
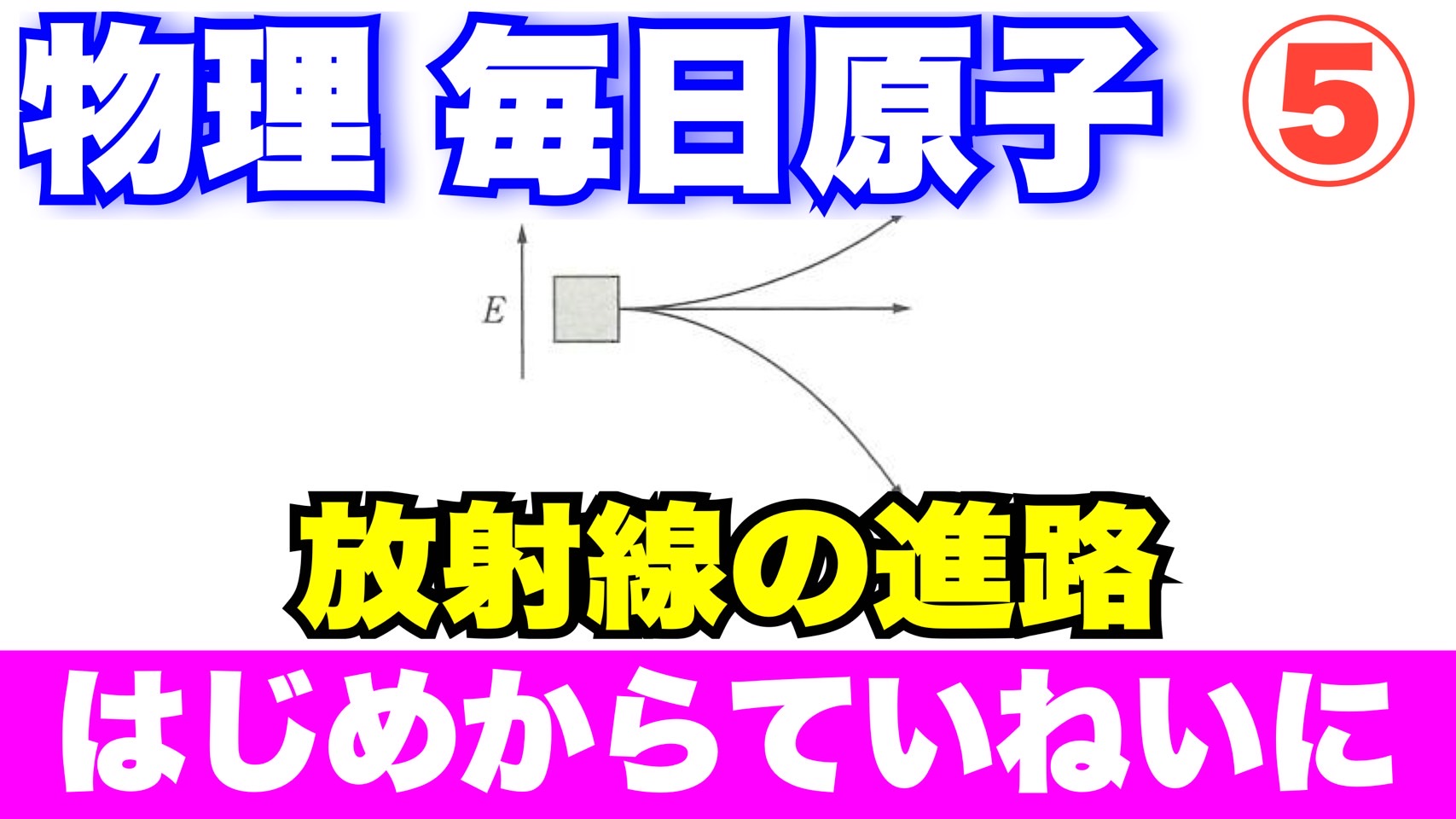
α線,β線,γ線すべてを含む放射線に,図に示す向きに電場Eを加えた。このときのα線,β線,γ線各々の進路を図の(ア)~(ウ)の中から選べ。
宿題
図のように,真空中に放射線源と磁石を配置した。α線,β線,γ線の放射線が放射線源から鉛直上向きに飛び出したとすると,各々の放射線の進路はどのようになるか,図の(a)~(c)から選べ。
この動画を見る
α線,β線,γ線すべてを含む放射線に,図に示す向きに電場Eを加えた。このときのα線,β線,γ線各々の進路を図の(ア)~(ウ)の中から選べ。
宿題
図のように,真空中に放射線源と磁石を配置した。α線,β線,γ線の放射線が放射線源から鉛直上向きに飛び出したとすると,各々の放射線の進路はどのようになるか,図の(a)~(c)から選べ。
【共通テスト・定期試験前の最終チェック!!】無機化学よく出る色を確認!!〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#大学入試過去問(化学)#共通テスト#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
共通テスト直前!無機化学で直前にチェックするべき内容をまとめています!
この動画を見る
共通テスト直前!無機化学で直前にチェックするべき内容をまとめています!
2024年 共通テスト 化学 出題予想!5つに絞ってみた

単元:
#化学#化学基礎2ー物質の変化#化学理論#無機#有機#大学入試過去問(化学)#物質の三態と状態変化#芳香族化合物#共通テスト#非金属元素の単体と化合物#化学(高分子)#合成樹脂とゴム#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2024年 共通テスト 化学 出題予想!5つに絞ってみた
予想1:滴定曲線(緩衝液)と$pH$
予想2:ボルンハーバーサイクル
予想3:オストワルト法
予想4:芳香族化合物の分離
予想5:合成高分子化合物(ゴム)
※共通テスト対策※
・過去問や模試の復習で知識の穴を減らしていく
・共通テスト形式の問題集で実践練習するとなお良い。
この動画を見る
2024年 共通テスト 化学 出題予想!5つに絞ってみた
予想1:滴定曲線(緩衝液)と$pH$
予想2:ボルンハーバーサイクル
予想3:オストワルト法
予想4:芳香族化合物の分離
予想5:合成高分子化合物(ゴム)
※共通テスト対策※
・過去問や模試の復習で知識の穴を減らしていく
・共通テスト形式の問題集で実践練習するとなお良い。
【高校物理】毎日原子4日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
核融合反応 $_1^2H+ _1^2H→_Z^AX + _1^1H$で得られる原子核Xの質量数Aと原子番号Zはそれぞれ□と□である□と□の核子1個当たりの結合エネルギーをそれぞれ1.1 MeVと2.8MeVとすると,この反応で放出されるエネルギーは□.□MeV となる。
宿題
$^2H$と$^3H$の原子核が反応して$^4He$と中性子ができた。$^2H$,$^3H$,$^4He$の核子1個あたりの結合エネルギーは,それぞれ1.1MeV,2.8MeV,7.1MeVである。この反応で解放されるエネルギーは□MeVである。
この動画を見る
核融合反応 $_1^2H+ _1^2H→_Z^AX + _1^1H$で得られる原子核Xの質量数Aと原子番号Zはそれぞれ□と□である□と□の核子1個当たりの結合エネルギーをそれぞれ1.1 MeVと2.8MeVとすると,この反応で放出されるエネルギーは□.□MeV となる。
宿題
$^2H$と$^3H$の原子核が反応して$^4He$と中性子ができた。$^2H$,$^3H$,$^4He$の核子1個あたりの結合エネルギーは,それぞれ1.1MeV,2.8MeV,7.1MeVである。この反応で解放されるエネルギーは□MeVである。
ゾロって刀いらんくね?

【化学】古い過去問 センター試験2001年度 第2問 問1 圧力変化のグラフ

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
濃度が$0.10 mol/L$の酸$a・b$を$10ml$ずつ取り、
それぞれを$0.10 mol/l$水酸化ナトリウム水溶液で滴定し、
滴下量と溶液の$pH$との関係を調べた。
図1に示した滴定曲線を与える酸の組合せとして最も適当なものを、下の①~ ⑥のうちから一つ選べ。
※図・表は動画内参照
この動画を見る
濃度が$0.10 mol/L$の酸$a・b$を$10ml$ずつ取り、
それぞれを$0.10 mol/l$水酸化ナトリウム水溶液で滴定し、
滴下量と溶液の$pH$との関係を調べた。
図1に示した滴定曲線を与える酸の組合せとして最も適当なものを、下の①~ ⑥のうちから一つ選べ。
※図・表は動画内参照
【高校物理】毎日原子3日目【共通テストまで毎日19時投稿】

単元:
#物理#理科(高校生)#原子
指導講師:
理数個別チャンネル
問題文全文(内容文):
$_{239}$Puは半減期$2.4×10^4$〔年〕で崩壊する放射性物質である。崩壊せずに残っている$_{239}$Puの量がもとの10%になるまでに要する年数tを有効数字2桁で表せ。ただし、$log_{10}2=0.30$とする。
宿題
古代遺跡から発掘された植物体内の$^{14}$Cの$^{12}$Cに対する割合は,大気中のそれの0.71倍であった。この発掘された植物は今からおよそ何年前に生育していたものと推定されるか。これを有効数字2桁で表すとき,次の式中の空欄ア〜ウに入れる数字として最も適当なものを答えよ。ただし,$^{14}$Cのβ崩壊の半減期は$5.73×10^3$年であり,大気中の$^{14}$Cと$^{12}$Cの割合は常に一定とする。また,$\frac{1}{\sqrt{2}}=0.71$である。 $□ .□×10^□$
この動画を見る
$_{239}$Puは半減期$2.4×10^4$〔年〕で崩壊する放射性物質である。崩壊せずに残っている$_{239}$Puの量がもとの10%になるまでに要する年数tを有効数字2桁で表せ。ただし、$log_{10}2=0.30$とする。
宿題
古代遺跡から発掘された植物体内の$^{14}$Cの$^{12}$Cに対する割合は,大気中のそれの0.71倍であった。この発掘された植物は今からおよそ何年前に生育していたものと推定されるか。これを有効数字2桁で表すとき,次の式中の空欄ア〜ウに入れる数字として最も適当なものを答えよ。ただし,$^{14}$Cのβ崩壊の半減期は$5.73×10^3$年であり,大気中の$^{14}$Cと$^{12}$Cの割合は常に一定とする。また,$\frac{1}{\sqrt{2}}=0.71$である。 $□ .□×10^□$
ゾロの顎の力はどれくらいなのか?

