 ぺんぎん高校化学問題集
ぺんぎん高校化学問題集
 ぺんぎん高校化学問題集
ぺんぎん高校化学問題集
※下の画像部分をクリックすると、先生の紹介ページにリンクします。
1分で解いてほしい化学計算問題 (19) 質量モル濃度(2)

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021年 神戸薬科大学]
質量パーセント濃度$60%$の酢酸水溶液$50g$に水を加えて希釈して、質量モル濃度$2.0mol/kg$の酢酸水溶液をつくった。
このとき、加えた水の質量$ [g]$はいくらか。
最も近い値を選べ。
($CH_3COOH$の分子量は$60$)
$(1)200 (2)230 (3)250 (4)320 (5)450$
$(6) 480 (7) 500 (8) 550 (9) 620$
この動画を見る
[2021年 神戸薬科大学]
質量パーセント濃度$60%$の酢酸水溶液$50g$に水を加えて希釈して、質量モル濃度$2.0mol/kg$の酢酸水溶液をつくった。
このとき、加えた水の質量$ [g]$はいくらか。
最も近い値を選べ。
($CH_3COOH$の分子量は$60$)
$(1)200 (2)230 (3)250 (4)320 (5)450$
$(6) 480 (7) 500 (8) 550 (9) 620$
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第6問 問2 ヌクレオチドの構造

単元:
#化学#有機#有機化合物の特徴と構造#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
天然に存在する核酸に関する記述として誤りを含むものを、次の①~⑤のう ちから一つ選べ。
① 核酸の単量体に相当する分子をヌクレオチドという。
② 核酸は、それを構成する糖のヒドロキシ基とリン酸が縮合した構造をもつ。
③ $RNA$は5種類の塩基をもつ。
④ $DNA$は4種類の塩基をもつ。
⑤ $DNA$ の二重らせん構造では、塩基どうしが水素結合を形成している。
この動画を見る
天然に存在する核酸に関する記述として誤りを含むものを、次の①~⑤のう ちから一つ選べ。
① 核酸の単量体に相当する分子をヌクレオチドという。
② 核酸は、それを構成する糖のヒドロキシ基とリン酸が縮合した構造をもつ。
③ $RNA$は5種類の塩基をもつ。
④ $DNA$は4種類の塩基をもつ。
⑤ $DNA$ の二重らせん構造では、塩基どうしが水素結合を形成している。
1分で解いてほしい化学計算問題 (18) 陽イオン交換樹脂

単元:
#化学#化学基礎2ー物質の変化#酸と塩基・水素イオン濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2022年 明星大学(改)]
濃度不明の塩化カルシウム$CaCl_2$水溶液$25mL$を、十分な量の陽イオン 交換樹脂に通した。
$25mL$の流出液を$0.10mol/L$の水酸化ナトリウム $NaOH$水溶液で滴定したところ、$20mL$加えたところで中和が完了し た。
この$CaCl_2$水溶液の濃度は何$mol/L$か。
有効数字2桁で答えなさい。
この動画を見る
[2022年 明星大学(改)]
濃度不明の塩化カルシウム$CaCl_2$水溶液$25mL$を、十分な量の陽イオン 交換樹脂に通した。
$25mL$の流出液を$0.10mol/L$の水酸化ナトリウム $NaOH$水溶液で滴定したところ、$20mL$加えたところで中和が完了し た。
この$CaCl_2$水溶液の濃度は何$mol/L$か。
有効数字2桁で答えなさい。
化学基礎の教科書を解説する動画 第65回 金属の製錬

無機化学第20回 アルミニウム(続き)・スズ・鉛

有機化学第23回 けん化価とヨウ素価

共通テスト(旧センター試験)過去問解説 化学 2015年追試 第6問 問1 グルコースとセルロース

単元:
#化学#化学(高分子)#糖類#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
グルコースとセルロースに関する記述として誤りを含むものを、次の①~⑤ のうちから一つ選べ。
① グルコースは、5個のヒドロキシ基をもつ。
② 結晶状態のグルコースは、六員環の構造をもつ。
③ グルコースは、フルクトースの構造異性体である。
④ セルロース中にあるグルコース単位には、4個のヒドロキシ基が存在する。
⑤ セルロースは、デンプンのようならせん状ではなく、直線状の構造をとる。
この動画を見る
グルコースとセルロースに関する記述として誤りを含むものを、次の①~⑤ のうちから一つ選べ。
① グルコースは、5個のヒドロキシ基をもつ。
② 結晶状態のグルコースは、六員環の構造をもつ。
③ グルコースは、フルクトースの構造異性体である。
④ セルロース中にあるグルコース単位には、4個のヒドロキシ基が存在する。
⑤ セルロースは、デンプンのようならせん状ではなく、直線状の構造をとる。
1分で解いてほしい化学計算問題 (17) 電解質水溶液の凝固点

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2022 千葉大学(改)]
塩化ナトリウム$5.85g$を水$500g$に溶かした水溶液の凝固点は何$℃$か答 えなさい。計算過程も示し、有効数字2けたで答えなさい。
ただし、水のモル凝固点降下を$1.85K・kg/mol$とし、塩化ナトリウムはすべて電離 するものとする。
($NaCI$の式量は$58.5$)
この動画を見る
[2022 千葉大学(改)]
塩化ナトリウム$5.85g$を水$500g$に溶かした水溶液の凝固点は何$℃$か答 えなさい。計算過程も示し、有効数字2けたで答えなさい。
ただし、水のモル凝固点降下を$1.85K・kg/mol$とし、塩化ナトリウムはすべて電離 するものとする。
($NaCI$の式量は$58.5$)
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第5問 問3 合成高分子化合物の構造
単元:
#化学#大学入試過去問(化学)#共通テスト#化学(高分子)#合成樹脂とゴム#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
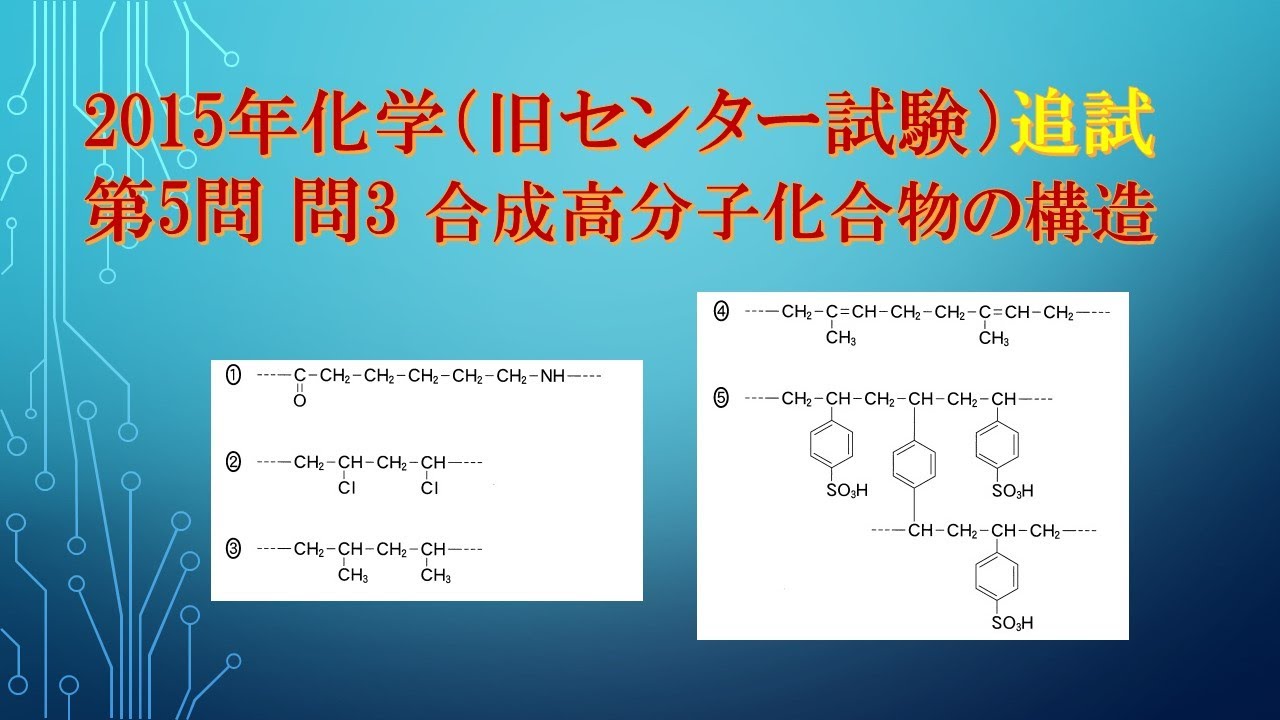
次の記述(a・b)に高分子の構造の一部として最も適当なもの を、下の①~⑤のうちから一つずつ選べ。
a イオン交換樹脂として用いられる高分子$\boxed{ 3 }$
b 天然ゴム(生ゴム)の主成分である高分子$\boxed{ 4 }$
この動画を見る
次の記述(a・b)に高分子の構造の一部として最も適当なもの を、下の①~⑤のうちから一つずつ選べ。
a イオン交換樹脂として用いられる高分子$\boxed{ 3 }$
b 天然ゴム(生ゴム)の主成分である高分子$\boxed{ 4 }$
1分で解いてほしい化学計算問題 (16) シュウ酸水溶液の調製

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023 中京大学(改)]
$5.00 ×10-2mol/L$のシュウ酸水溶液をつくるため、シュウ酸二水和物の結晶を$W [mg]$ 、少量の純水に溶かした後、$100mL$のメスフラスコに入れ標線まで純水を加えた。
$W$の値を有効数字3桁で求めよ。
(原子量: $H 1.0 C12 Ο 16$)
この動画を見る
[2023 中京大学(改)]
$5.00 ×10-2mol/L$のシュウ酸水溶液をつくるため、シュウ酸二水和物の結晶を$W [mg]$ 、少量の純水に溶かした後、$100mL$のメスフラスコに入れ標線まで純水を加えた。
$W$の値を有効数字3桁で求めよ。
(原子量: $H 1.0 C12 Ο 16$)
化学基礎の教科書を解説する動画 第64回 電池(燃料電池)

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎の教科書を解説する動画 電池(燃料電池)
この動画を見る
化学基礎の教科書を解説する動画 電池(燃料電池)
無機化学第19回 アルミニウム

有機化学第22回 油脂のけん化・付加反応

単元:
#化学#有機#酸素を含む脂肪族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
有機化学の高校教科書を解説していきます。
〔油脂のけん化・付加反応〕
この動画を見る
有機化学の高校教科書を解説していきます。
〔油脂のけん化・付加反応〕
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第5問 問2 合成高分子化合物

単元:
#化学#大学入試過去問(化学)#共通テスト#化学(高分子)#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
高分子化合物の合成に関する記述として誤りを含むものを、
次の①~⑤のうちから一つ選べ。
① ナイロン6は、カプロラクタム($\varepsilon^-$カプロラクタム)の開環重合でつくられる。
② ポリエチレンテレフタラート テレフタル酸とエチレングリコールの縮 合重合でつくられる。
でれる
③ ポリビニルアルコールは、ビニルアルコールの付加重合でつくられる。
④ スチレンーブタジエンゴムは、スチレンとブタジエンの共重合でつくられる。
⑤ フェノール樹脂は、フェノールとホルムアルデヒドの付加縮合でつくられる。
この動画を見る
高分子化合物の合成に関する記述として誤りを含むものを、
次の①~⑤のうちから一つ選べ。
① ナイロン6は、カプロラクタム($\varepsilon^-$カプロラクタム)の開環重合でつくられる。
② ポリエチレンテレフタラート テレフタル酸とエチレングリコールの縮 合重合でつくられる。
でれる
③ ポリビニルアルコールは、ビニルアルコールの付加重合でつくられる。
④ スチレンーブタジエンゴムは、スチレンとブタジエンの共重合でつくられる。
⑤ フェノール樹脂は、フェノールとホルムアルデヒドの付加縮合でつくられる。
1分で解いてほしい化学計算問題 (15) ペプチドの配列

単元:
#化学#化学(高分子)#アミノ酸とタンパク質、核酸#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 大阪公立大学(中期)]
グリシン、バリン、セリン各1分子からなる鎖状のトリペプチドの配列順序は何通りあるか。
数字で答えよ。
ただし、アミノ酸に鏡像異性体が存在する場合は区別して教えよ。
この動画を見る
[2023年 大阪公立大学(中期)]
グリシン、バリン、セリン各1分子からなる鎖状のトリペプチドの配列順序は何通りあるか。
数字で答えよ。
ただし、アミノ酸に鏡像異性体が存在する場合は区別して教えよ。
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第5問 問1 合成高分子化合物の特徴

単元:
#化学#化学(高分子)#合成樹脂とゴム#合成繊維と天然繊維#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
合成分子化学物に関する記述として誤りを含むものを、次の①~⑤のうちから一つ選べ。
① 鎖状構造だけではなく、網目状構造の高分子もある。
② 重合度の異なる分子が集まってできている。
③ 非結晶部分(無定形部分)をもたない。
④ 明確な融点を示さない。
⑤ 熱可型性樹脂は、加熱によって成型加工しやすい。
この動画を見る
合成分子化学物に関する記述として誤りを含むものを、次の①~⑤のうちから一つ選べ。
① 鎖状構造だけではなく、網目状構造の高分子もある。
② 重合度の異なる分子が集まってできている。
③ 非結晶部分(無定形部分)をもたない。
④ 明確な融点を示さない。
⑤ 熱可型性樹脂は、加熱によって成型加工しやすい。
1分で解いてほしい化学計算問題 (14) ヘンリーの法則

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021 東京理科大学(改)]
窒素は$20℃ 1.0 \times 10^5Pa$, 水$1.0L$に$7.1×10{-4}mol$溶ける。
$20℃, 1.0 \times 10^5Pa$において空気が水に接しているとき、$10L$の水に溶解している窒素$〔g〕$の質量を有効数字2桁で求めよ。
ただし、空気は窒素と酸素を体積の比$4:1$で混合した気体とする。
原子量 $N 28$
この動画を見る
[2021 東京理科大学(改)]
窒素は$20℃ 1.0 \times 10^5Pa$, 水$1.0L$に$7.1×10{-4}mol$溶ける。
$20℃, 1.0 \times 10^5Pa$において空気が水に接しているとき、$10L$の水に溶解している窒素$〔g〕$の質量を有効数字2桁で求めよ。
ただし、空気は窒素と酸素を体積の比$4:1$で混合した気体とする。
原子量 $N 28$
化学基礎の教科書を解説する動画 第63回 電池(ダニエル電池)

無機化学第18回 アルカリ土類金属

単元:
#化学#無機#典型金属元素の単体と化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
無機化学分野の教科書の解説
〔無機化学第18回 アルカリ土類金属〕
この動画を見る
無機化学分野の教科書の解説
〔無機化学第18回 アルカリ土類金属〕
有機化学第21回 油脂 油脂の構造式の書き方・脂肪と脂肪油・硬化油

共通テスト(旧センター試験)過去問解説 化学 2015年追試 第4問 問6 アジピン酸のエステル化に関する計算問題

単元:
#化学#有機#酸素を含む脂肪族化合物#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
アジビン酸(分子量$146$)を濃硫酸を触媒として十分な量のメタノールと反応させ、完全にエステル化した。
このとき分子内に二つのエステル結合をもつ 化合物が$3.48g$生成した。
この反応で生成した水の質量は何$g$か。
最も適当な数値を、下の①~⑤のうちから一つ選べ。
アジビン酸:$HOOC-(CH_2)_4-COOH$
原子量:$H1 C12 O16$
①$0.36$ ②$0.39$ ③$0.60$
④$0.72$ ⑤$0.78$
この動画を見る
アジビン酸(分子量$146$)を濃硫酸を触媒として十分な量のメタノールと反応させ、完全にエステル化した。
このとき分子内に二つのエステル結合をもつ 化合物が$3.48g$生成した。
この反応で生成した水の質量は何$g$か。
最も適当な数値を、下の①~⑤のうちから一つ選べ。
アジビン酸:$HOOC-(CH_2)_4-COOH$
原子量:$H1 C12 O16$
①$0.36$ ②$0.39$ ③$0.60$
④$0.72$ ⑤$0.78$
1分で解いてほしい化学計算問題 (13) けん化価

単元:
#化学#有機#酸素を含む脂肪族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 聖マリアンナ医科大学(改)〕
けん化価とは、油脂1gを完全にけん化するのに必要な水酸化カリウム$KOH$の質量を$mg$単位で表した数値である。
分子量が$884$の油脂のけん化価を有効数字2桁で求めよ。
$H 1 O 16 K39$
この動画を見る
〔2023 聖マリアンナ医科大学(改)〕
けん化価とは、油脂1gを完全にけん化するのに必要な水酸化カリウム$KOH$の質量を$mg$単位で表した数値である。
分子量が$884$の油脂のけん化価を有効数字2桁で求めよ。
$H 1 O 16 K39$
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第4問 問5 元素分析装置
単元:
#化学#物質の成分と構成元素#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
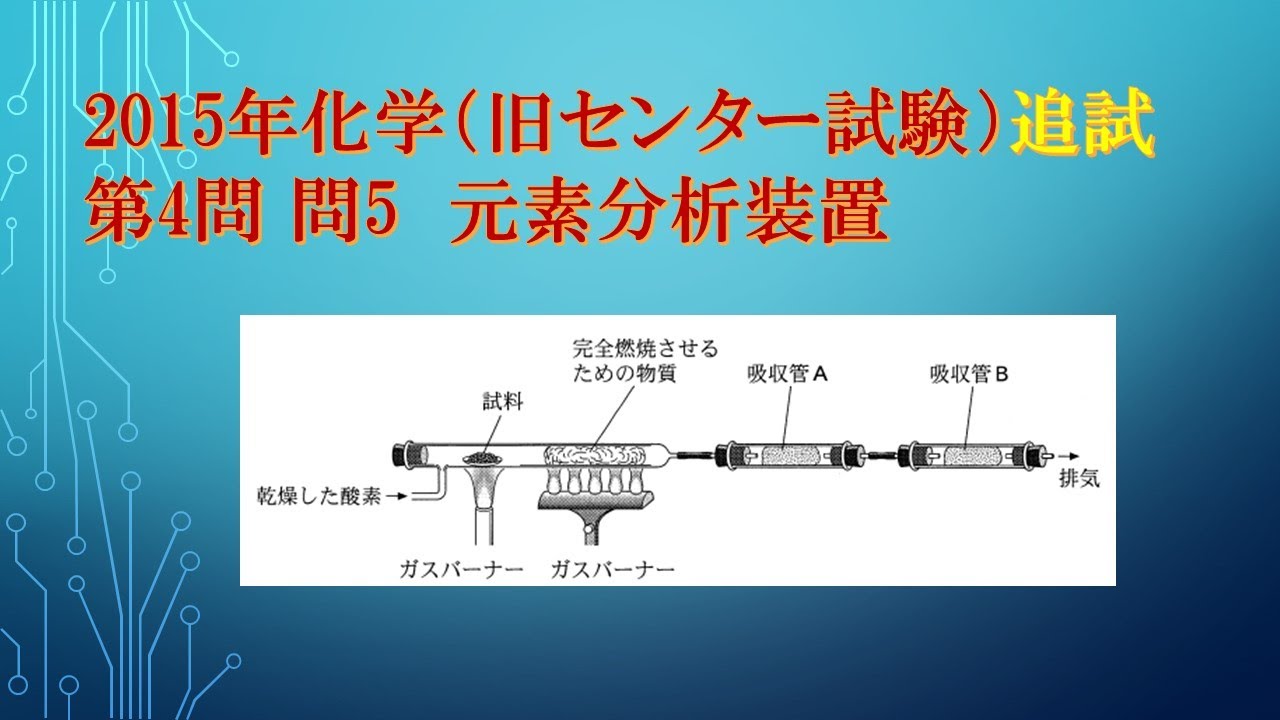
図1は、炭素、水素、酸素からなる有機化合物の元素分析を行うための装置を示している。
試料を完全燃焼させ、発生する2種類の気体を吸収管$A$と吸 収管$B$でそれぞれ吸収させる。
吸収管$A$に入れる物質と吸収管$B$で吸収させる物質の組合せとして最も適当なものを、下の①~⑥のうちから一つ選べ。
※図は動画内参照
この動画を見る
図1は、炭素、水素、酸素からなる有機化合物の元素分析を行うための装置を示している。
試料を完全燃焼させ、発生する2種類の気体を吸収管$A$と吸 収管$B$でそれぞれ吸収させる。
吸収管$A$に入れる物質と吸収管$B$で吸収させる物質の組合せとして最も適当なものを、下の①~⑥のうちから一つ選べ。
※図は動画内参照
1分で解いてほしい化学計算問題 (12) 圧平衡定数

単元:
#化学#化学理論#化学平衡と平衡移動#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 京都産業大学(改)〕
密閉容器中、温度$1000K$で、次の反応が平衛状態となっている。
$CO_2$(気)$+C$(固)$⇄2CO$(気)
全圧は$1.0 \times 10^5Pa,CO$の体積百分率は$80%$であった。
このときの圧平衛定数を単位をつけて有効数字2桁で求めよ。
この動画を見る
〔2023 京都産業大学(改)〕
密閉容器中、温度$1000K$で、次の反応が平衛状態となっている。
$CO_2$(気)$+C$(固)$⇄2CO$(気)
全圧は$1.0 \times 10^5Pa,CO$の体積百分率は$80%$であった。
このときの圧平衛定数を単位をつけて有効数字2桁で求めよ。
化学基礎の教科書を解説する動画 第62回 金属の反応(2) 金属と酸の反応

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎の教科書を解説する動画
〔金属の反応(2) 金属と酸の反応〕
この動画を見る
化学基礎の教科書を解説する動画
〔金属の反応(2) 金属と酸の反応〕
無機化学第17回 アンモニアソーダ法 炭酸ナトリウムNa₂CO₃の工業的製法

単元:
#化学#無機#典型金属元素の単体と化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
無機化学
〔アンモニアソーダ法 炭酸ナトリウムNa₂CO₃の工業的製法〕
この動画を見る
無機化学
〔アンモニアソーダ法 炭酸ナトリウムNa₂CO₃の工業的製法〕
有機化学第20回 けん化 強塩基によるエステルの加水分解

共通テスト(旧センター試験)過去問解説 化学 2015年追試 第4問 問4 フェノールの製法
単元:
#化学#有機#大学入試過去問(化学)#芳香族化合物#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
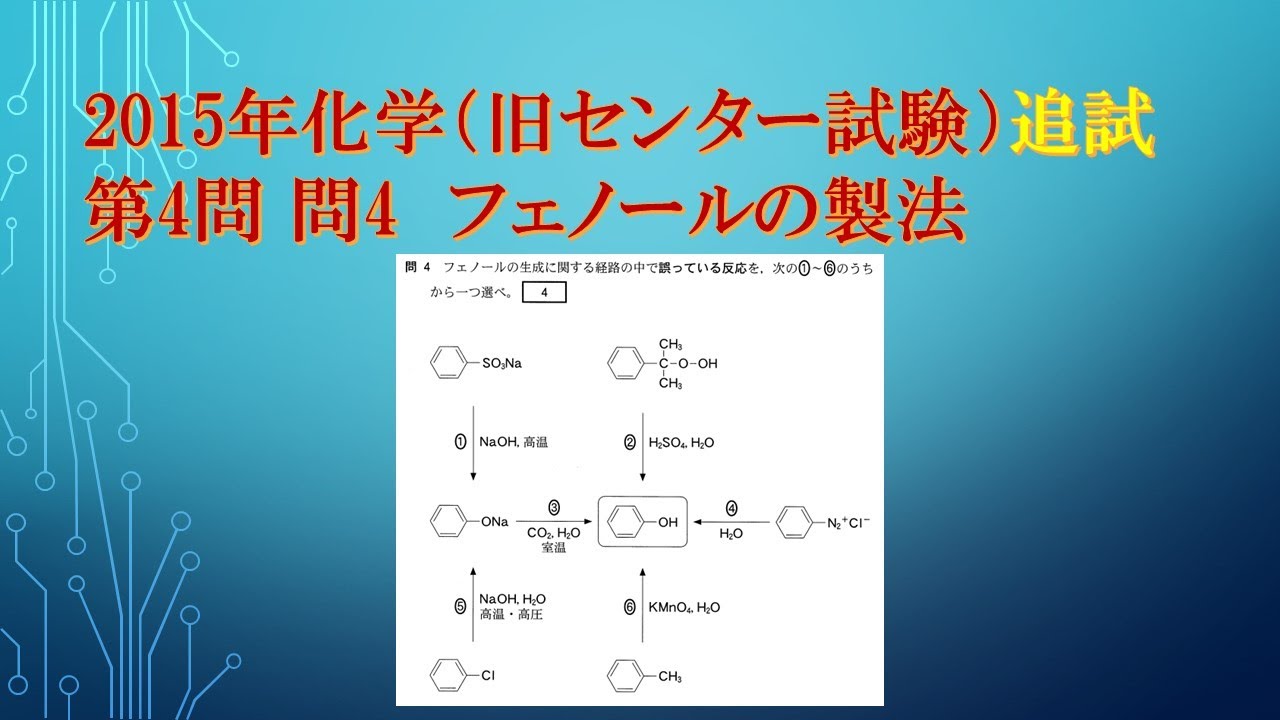
フェノールの生成に関する経路の中で誤っている反応を、
次の①~⑥のうちから選べ。
※図は動画内参照
この動画を見る
フェノールの生成に関する経路の中で誤っている反応を、
次の①~⑥のうちから選べ。
※図は動画内参照
1分で解いてほしい化学計算問題 (11) 過酸化水素の平均分解速度

単元:
#化学#化学理論#化学反応の速さ#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2022 金城学院大学(改)〕
ある濃度の過酸化水素水に、ある濃度の塩化鉄(Ⅲ)水溶液を加え$100mL$とした。
反応開始から発生した酸素物質量を、時間を追って測定したところ、次の表に示す結果が得られた。
最初に$20$秒間において、混合水溶液中の過酸化水素の平均分解速度は何$moL/(L・S)$か、有効数字2桁で答えよ。
※表は動画内参照
この動画を見る
〔2022 金城学院大学(改)〕
ある濃度の過酸化水素水に、ある濃度の塩化鉄(Ⅲ)水溶液を加え$100mL$とした。
反応開始から発生した酸素物質量を、時間を追って測定したところ、次の表に示す結果が得られた。
最初に$20$秒間において、混合水溶液中の過酸化水素の平均分解速度は何$moL/(L・S)$か、有効数字2桁で答えよ。
※表は動画内参照
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第4問 問3 エチレンとアセチレンの反応

単元:
#化学#有機#大学入試過去問(化学)#脂肪族炭化水素#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
エチレン(エテン)またはアセチレン(エチン)に関する反応記述として最も適当なものを、次の①~⑤のうちから一つ選べ。
① エチレンが塩化水素と反応すると、塩化ビニルが発生する。
② エチレンが臭素と反応すると1,2‐ジブロモエタンが発生する。
③ 炭化カルシウム(カルシウムカーバイド)が水と反応すると、エチレンが生成される。
④ アセチレン$1mol$が水素$2mol$と完全に反応すると、エチレン$1mol$が生成する。
⑤ アセチレンが水と反応すると、酢酸が生成される。
この動画を見る
エチレン(エテン)またはアセチレン(エチン)に関する反応記述として最も適当なものを、次の①~⑤のうちから一つ選べ。
① エチレンが塩化水素と反応すると、塩化ビニルが発生する。
② エチレンが臭素と反応すると1,2‐ジブロモエタンが発生する。
③ 炭化カルシウム(カルシウムカーバイド)が水と反応すると、エチレンが生成される。
④ アセチレン$1mol$が水素$2mol$と完全に反応すると、エチレン$1mol$が生成する。
⑤ アセチレンが水と反応すると、酢酸が生成される。


