 ぺんぎん高校化学問題集
ぺんぎん高校化学問題集
 ぺんぎん高校化学問題集
ぺんぎん高校化学問題集
※下の画像部分をクリックすると、先生の紹介ページにリンクします。
1分で解いてほしい化学計算問題 (27) 炭酸カルシウムの純度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 愛知医科大学(改)]
炭酸カルシウム$CaCO_3$を主成分とする大理石$12.0g$に$1.00mol/L$の塩酸を少しずつ加えていくと二酸化炭素が発生し、加えた塩酸の体積が$200mL$になった時点で、二酸化炭素の発生がとまった。
ただし、二酸化炭素は炭酸カルシウムと塩酸の反応でのみ発生し、大理石中の他の成分は塩酸と反応しないものとする。
大理石の炭酸カルシウムの純度(質量百分率)は何$%$か。
有効数字3桁で答えよ。
$CaCO_3$の式量:$100$
この動画を見る
[2023年 愛知医科大学(改)]
炭酸カルシウム$CaCO_3$を主成分とする大理石$12.0g$に$1.00mol/L$の塩酸を少しずつ加えていくと二酸化炭素が発生し、加えた塩酸の体積が$200mL$になった時点で、二酸化炭素の発生がとまった。
ただし、二酸化炭素は炭酸カルシウムと塩酸の反応でのみ発生し、大理石中の他の成分は塩酸と反応しないものとする。
大理石の炭酸カルシウムの純度(質量百分率)は何$%$か。
有効数字3桁で答えよ。
$CaCO_3$の式量:$100$
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問6 電気分解の量的関係
単元:
#化学#化学理論#大学入試過去問(化学)#電池と電気分解#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
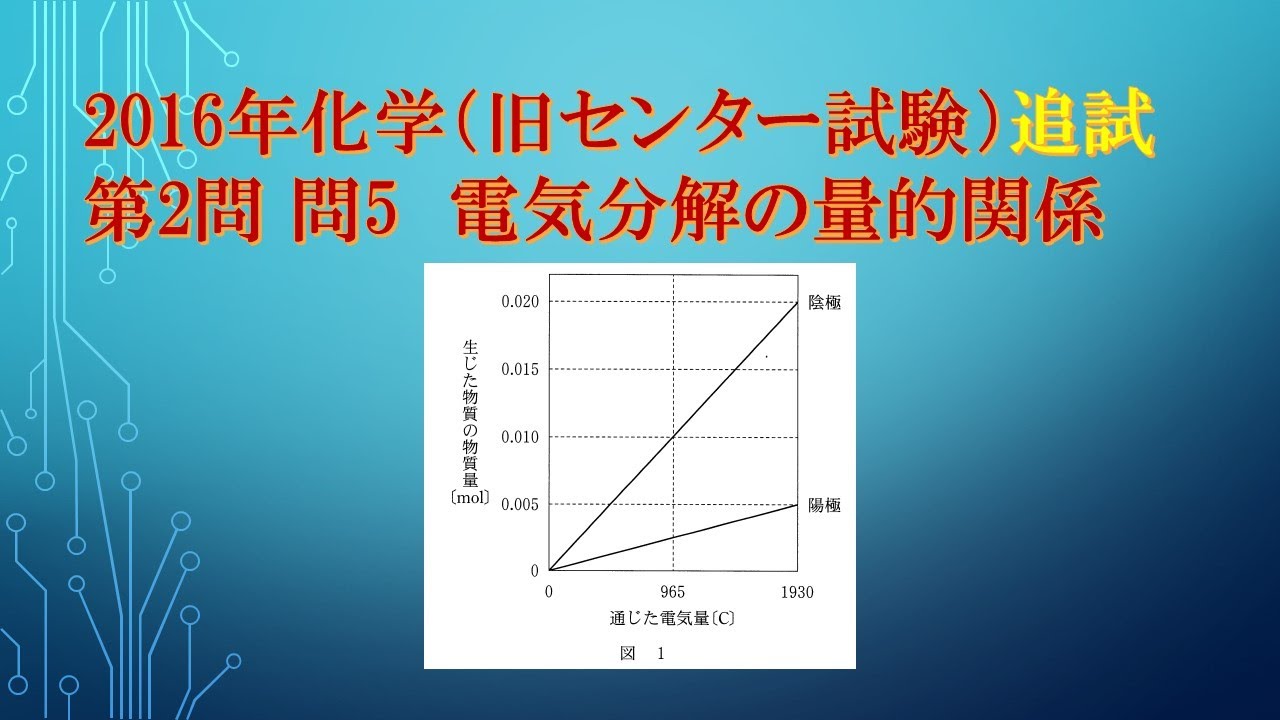
ある電解質$A$の水溶液を、白金電極を用いて電気分解したところ、通じた電気量と両極で生じた物質の物質量との関係が図のようになった。
電解質$A$として最も適当なものを、下の①~⑤のうちから一つ選べ。
①$NaCH$
②$Na_2SO_4$
③$KCI$
④$CuCI_2$
⑤$AgNO_3$
※図は動画内参照
この動画を見る
ある電解質$A$の水溶液を、白金電極を用いて電気分解したところ、通じた電気量と両極で生じた物質の物質量との関係が図のようになった。
電解質$A$として最も適当なものを、下の①~⑤のうちから一つ選べ。
①$NaCH$
②$Na_2SO_4$
③$KCI$
④$CuCI_2$
⑤$AgNO_3$
※図は動画内参照
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問6 電気分解の量的関係

単元:
#化学#化学理論#大学入試過去問(化学)#電池と電気分解#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ある電解質Aの水溶液を、白金電極を用いて電気分解したところ、通じた電気量と両極で生じた物質の物質量との関係が図1のようになった。
電解質Aとして最も適当なものを、下の①~⑤のうちから一つ選べ。
①$NaOH$
②$NA_2SO_4$
③$KCI$
④$CuCI_2$
⑤$AgNO_3$
※図は動画内参照
この動画を見る
ある電解質Aの水溶液を、白金電極を用いて電気分解したところ、通じた電気量と両極で生じた物質の物質量との関係が図1のようになった。
電解質Aとして最も適当なものを、下の①~⑤のうちから一つ選べ。
①$NaOH$
②$NA_2SO_4$
③$KCI$
④$CuCI_2$
⑤$AgNO_3$
※図は動画内参照
1分で解いてほしい化学計算問題 (26) 電気分解

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023年 神戸女学院大学(改)〕
陽極に不純物を含む粗銅版を使用し、硫酸酸性の硫酸銅(Ⅱ)水溶液を$5.0A$の電流で$1.93 \times 10^3$秒電気分解した。
析出した銅の質量$〔g〕$はいくらか。
ファラデー定数を$9.65 \times 10^4C/mol$とする。
この動画を見る
〔2023年 神戸女学院大学(改)〕
陽極に不純物を含む粗銅版を使用し、硫酸酸性の硫酸銅(Ⅱ)水溶液を$5.0A$の電流で$1.93 \times 10^3$秒電気分解した。
析出した銅の質量$〔g〕$はいくらか。
ファラデー定数を$9.65 \times 10^4C/mol$とする。
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問4 中和反応後のpH

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#酸と塩基・水素イオン濃度#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
濃度不明の塩酸$1.0L$を$0.030mol/L$の水酸化ナトリウム水溶液$1.0L$と混合したところ、$0.56kJ$の発熱があった。
この混合溶液の$pH$として最も適当な数値を①~⑧のうちから一つ選べ。
ただし、中和熱は$56kJ/mol$とし、中和反応以外による発熱または吸熱は無視できるものとする。
①$1$ ②$2$ ③$3$ ④$5$ ⑤$9$ ⑥$11$ ⑦$12$ ⑧$13$
この動画を見る
濃度不明の塩酸$1.0L$を$0.030mol/L$の水酸化ナトリウム水溶液$1.0L$と混合したところ、$0.56kJ$の発熱があった。
この混合溶液の$pH$として最も適当な数値を①~⑧のうちから一つ選べ。
ただし、中和熱は$56kJ/mol$とし、中和反応以外による発熱または吸熱は無視できるものとする。
①$1$ ②$2$ ③$3$ ④$5$ ⑤$9$ ⑥$11$ ⑦$12$ ⑧$13$
無機化学第24回 銅と銀

有機化学第27回 配向性

共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問3 平衡定数の計算(基礎)

単元:
#化学#化学理論#大学入試過去問(化学)#化学平衡と平衡移動#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$1.0mol$の気体$A$のみが入った密閉容器に$1.0mol$の気体$B$を加えたところ、気体$C$および$D$が生成して、次式の平衛が成立した。
$A+B⇄C+D$
このときの$C$の物質として最も適当な数値を、次の①~⑤のうちから一つ選べ。
ただし、容器内の温度と体積は一定とし、子の温度における反応平衛定数は$0.25$とする。
①$0.25$ ②$0.33$ ③$0.50$ ④$0.67$ ⑤$0.75$
この動画を見る
$1.0mol$の気体$A$のみが入った密閉容器に$1.0mol$の気体$B$を加えたところ、気体$C$および$D$が生成して、次式の平衛が成立した。
$A+B⇄C+D$
このときの$C$の物質として最も適当な数値を、次の①~⑤のうちから一つ選べ。
ただし、容器内の温度と体積は一定とし、子の温度における反応平衛定数は$0.25$とする。
①$0.25$ ②$0.33$ ③$0.50$ ④$0.67$ ⑤$0.75$
1分で解いてほしい化学計算問題 (25) 鉛蓄電池の放電による質量変化

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023年 愛知工業大学(改)〕
鉛蓄電池の構成は、次のように表される。
$\begin{array}{c|c}
(-)Pb & H_2SO_{4aq} &PbO_2(+) \\
\\
\end{array}$
この電池の両極を外部回路に接続し、$2.0A$の一定電流で1時間20分25秒間放電させたとき、この放電による負極の質量の変化を$+,-$をつけて有効数字2桁で答えなさい。
(原子量:H 1 O 16 S 32 Pb 207 $,ファデラー定数 9.65 \times 10^4C/mol$)
この動画を見る
〔2023年 愛知工業大学(改)〕
鉛蓄電池の構成は、次のように表される。
$\begin{array}{c|c}
(-)Pb & H_2SO_{4aq} &PbO_2(+) \\
\\
\end{array}$
この電池の両極を外部回路に接続し、$2.0A$の一定電流で1時間20分25秒間放電させたとき、この放電による負極の質量の変化を$+,-$をつけて有効数字2桁で答えなさい。
(原子量:H 1 O 16 S 32 Pb 207 $,ファデラー定数 9.65 \times 10^4C/mol$)
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問2 メタンハイドレート

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
将来のエネルギー資源として期待されているメタンハイドレートは、水分子 が形成するかご状構造の中にメタン分子が取り込まれた固体物質として海底な どに存在する。メタン1分子あたり平均$5.8$個の水分子で構成されるメタンハ イドレート $1.2kg$から、メタンを気体としてすべて取り出して完全燃焼させる。
次の問い(a・b)に答えよ。
原子量
$H1 C 12 Ο 16$
a 燃焼で消費される酸素の物質量は何$mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$5.0$ ②$10$ ③$20$ ④$65$ ⑤$75$ ⑥$130$
b このとき発生する熱量は何$kJ$か。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
ただし、気体のメタンの燃焼熱は$890 kJ/mol$とする。
①$8.9 \times 10^2$
②$4.5 \times 10^3$
③$5.8 \times 10^3$
④$8.9 \times 10^3$
⑤$4.5 \times 10^4$
⑥$5.8 \times 10^4$
この動画を見る
将来のエネルギー資源として期待されているメタンハイドレートは、水分子 が形成するかご状構造の中にメタン分子が取り込まれた固体物質として海底な どに存在する。メタン1分子あたり平均$5.8$個の水分子で構成されるメタンハ イドレート $1.2kg$から、メタンを気体としてすべて取り出して完全燃焼させる。
次の問い(a・b)に答えよ。
原子量
$H1 C 12 Ο 16$
a 燃焼で消費される酸素の物質量は何$mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$5.0$ ②$10$ ③$20$ ④$65$ ⑤$75$ ⑥$130$
b このとき発生する熱量は何$kJ$か。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
ただし、気体のメタンの燃焼熱は$890 kJ/mol$とする。
①$8.9 \times 10^2$
②$4.5 \times 10^3$
③$5.8 \times 10^3$
④$8.9 \times 10^3$
⑤$4.5 \times 10^4$
⑥$5.8 \times 10^4$
1分で解いてほしい化学計算問題 (24) 油脂への水素付加

単元:
#化学#有機#酸素を含む脂肪族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021年 愛知学院大学]
リノレン酸$C_17H_29COOH$(分子量$278$)とグリセリン(分子量$92$)からなる油脂がある。
この油脂$21.8g$に付加できる水素$H_2$は標準状態$(0℃, 1.013×10^5Pa)$で最大何$L$ですか。
有効数字2桁で答えなさい。
モル体積: $22.4L/mol$
この動画を見る
[2021年 愛知学院大学]
リノレン酸$C_17H_29COOH$(分子量$278$)とグリセリン(分子量$92$)からなる油脂がある。
この油脂$21.8g$に付加できる水素$H_2$は標準状態$(0℃, 1.013×10^5Pa)$で最大何$L$ですか。
有効数字2桁で答えなさい。
モル体積: $22.4L/mol$
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問1 熱化学方程式

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
アンモニア(気)と塩化水素(気)から塩化アンモニウム(固)が生成する反応の反応熱は$176 kJ/mol$である。
塩化アンモニウム(固)の生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑧のうちから一つ選べ。
ただし、アンモニア(気) および塩化水素(気)の生成熱は、
それぞれ$46 kJ/mol$ および$92 kJ/mol$である。
①$-314$ ②$-176$ ③$-138$ ④$-38$ ⑤$38$ ⑥$138$ ⑦$176$ ⑧$314$
この動画を見る
アンモニア(気)と塩化水素(気)から塩化アンモニウム(固)が生成する反応の反応熱は$176 kJ/mol$である。
塩化アンモニウム(固)の生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑧のうちから一つ選べ。
ただし、アンモニア(気) および塩化水素(気)の生成熱は、
それぞれ$46 kJ/mol$ および$92 kJ/mol$である。
①$-314$ ②$-176$ ③$-138$ ④$-38$ ⑤$38$ ⑥$138$ ⑦$176$ ⑧$314$
無機化学第23回 亜鉛の単体と化合物

有機化学第26回 ベンゼンの置換反応

共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問6 ケイ素の単体と化合物

単元:
#化学#無機#大学入試過去問(化学)#共通テスト#無機物質と人間生活#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ケイ素およびその化合物に関する記述として誤りを含むものを、次の①~⑥のうちから一つ選べ。
①ケイ素は、炭素と同じ14族に属する
②ケイ素は、地殻中に次いで多く存在している元素である。
③ケイ素の結晶中では、一個のケイ素原子を中心に4個のケイ素原子が正四面体を形づくっている。
④ケイ素の単体は、太陽電池の材料に用いられる。
⑤ケイ酸塩は、セラミックスなどの原料として用いられる。
⑥二酸化ケイ素の結晶は、固体の二酸化炭素と同様に分子結晶である。
この動画を見る
ケイ素およびその化合物に関する記述として誤りを含むものを、次の①~⑥のうちから一つ選べ。
①ケイ素は、炭素と同じ14族に属する
②ケイ素は、地殻中に次いで多く存在している元素である。
③ケイ素の結晶中では、一個のケイ素原子を中心に4個のケイ素原子が正四面体を形づくっている。
④ケイ素の単体は、太陽電池の材料に用いられる。
⑤ケイ酸塩は、セラミックスなどの原料として用いられる。
⑥二酸化ケイ素の結晶は、固体の二酸化炭素と同様に分子結晶である。
1分で解いてほしい化学計算問題 (23) 状態変化と熱量

単元:
#化学#化学理論#物質の変化と熱・光#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
20$^{ \circ }$の水180gを加熱して100$^{ \circ }$の水蒸気にしたい。
必要な熱量[kJ]として、最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、液体の水1gを1K温度上昇させるのに必要な熱量は4.2J、水100$^{ \circ }$での蒸発熱は41kJ/molである。
水の分子量:18[2021年 成蹊大学]
①$60$
②$80$
③$1.0\times10^2$
④$4.1\times10^2$
⑤$4.7\times10^2$
⑥$5.3\times10^2$
この動画を見る
20$^{ \circ }$の水180gを加熱して100$^{ \circ }$の水蒸気にしたい。
必要な熱量[kJ]として、最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、液体の水1gを1K温度上昇させるのに必要な熱量は4.2J、水100$^{ \circ }$での蒸発熱は41kJ/molである。
水の分子量:18[2021年 成蹊大学]
①$60$
②$80$
③$1.0\times10^2$
④$4.1\times10^2$
⑤$4.7\times10^2$
⑥$5.3\times10^2$
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問5 気体の溶解(ヘンリーの法則)

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
この動画を見る
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
1分で解いてほしい化学計算問題 (22) アルコール発酵

単元:
#化学#有機#酸素を含む脂肪族化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021年 摂南大学(改)]
エタノールはグルコース$(C_6H_{12}O_6)$を原料としてアルコール発酵によっ ても作られている。
アルコール発酵によりエタノール$46g$を得るには低何$g$のグルコースが必要であるか、整数で答えなさい。
原子量 $H 1.0 C 12 0 16$
この動画を見る
[2021年 摂南大学(改)]
エタノールはグルコース$(C_6H_{12}O_6)$を原料としてアルコール発酵によっ ても作られている。
アルコール発酵によりエタノール$46g$を得るには低何$g$のグルコースが必要であるか、整数で答えなさい。
原子量 $H 1.0 C 12 0 16$
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問4 蒸気圧と状態方程式
単元:
#化学#化学理論#大学入試過去問(化学)#化学平衡と平衡移動#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
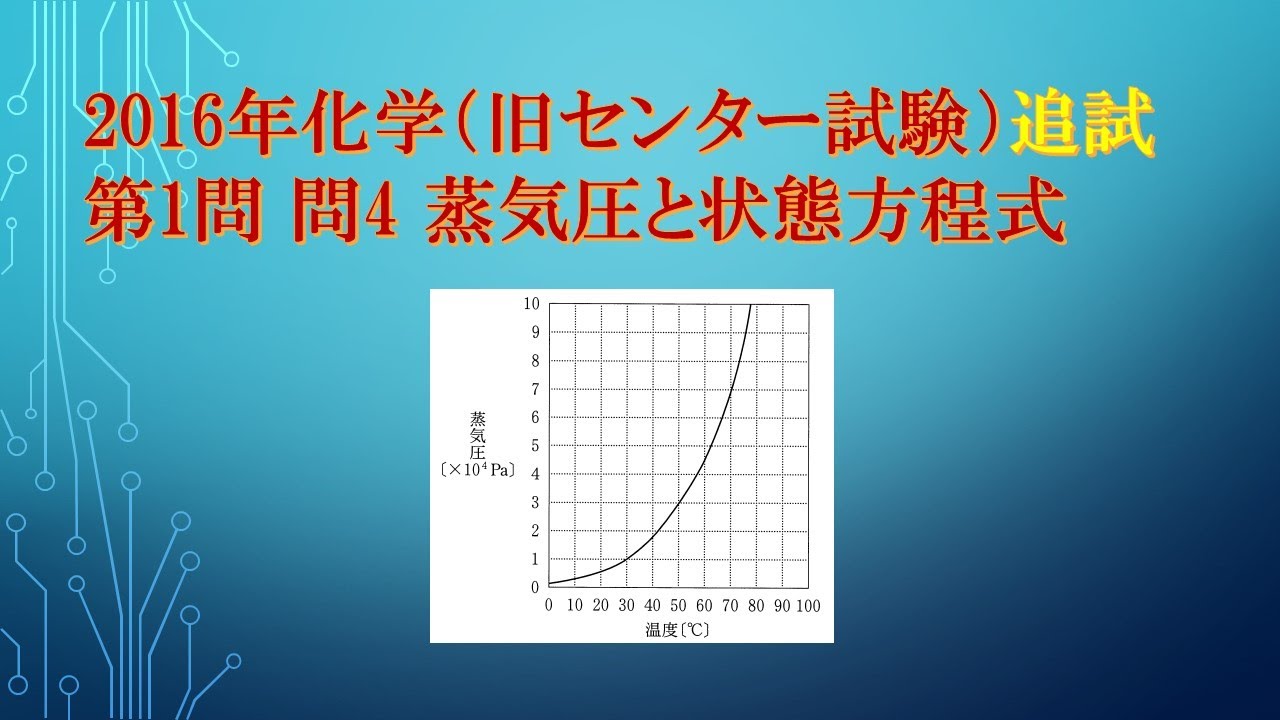
図2はエタノールの蒸気圧曲線である。
容積 $1.0L$の密閉容器に $0.010 mol$ のエタノールのみが入っている。
容器の温度が$40℃$および$60℃$のとき、容器内の圧力はそれぞれ何か、圧力の値の組合せとして最も適当なものを、下の①~⑦のうちから一つ選べ。
ただし、気体定数は $R = 8.3 × 10^2 Pa-L/(K・mol)$とする。
また、容器内での液体の体積は無視できるものとする。
※表・図は動画内参照
この動画を見る
図2はエタノールの蒸気圧曲線である。
容積 $1.0L$の密閉容器に $0.010 mol$ のエタノールのみが入っている。
容器の温度が$40℃$および$60℃$のとき、容器内の圧力はそれぞれ何か、圧力の値の組合せとして最も適当なものを、下の①~⑦のうちから一つ選べ。
ただし、気体定数は $R = 8.3 × 10^2 Pa-L/(K・mol)$とする。
また、容器内での液体の体積は無視できるものとする。
※表・図は動画内参照
無機化学第22回 錯イオン

有機化学第25回 芳香族化合物

共通テスト(旧センター試験)過去問解説 化学 2016年追試 第6問 問3 理想気体と実在気体

単元:
#化学#化学理論#大学入試過去問(化学)#気体の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
理想気体と実在気体に関する記述として下線部に誤りを含むものを、次の ①~⑤のうちから一つ選べ。
① 理想気体では、物質量と温度が一定であれば、圧力を変化させても圧力と 体積の積は変化しない。
② 理想気体では、体積一定のまま温度を下げると圧力は単調に減少する。
③ 理想気体では、気体分子自身の体積はないものと仮定している。
④ 実在気体は、常圧では温度が低いほど理想気体に近いふるまいをする。
⑤ 実在気体であるアンモニア$1mol$の体積が、標準状態において$22.4L$より小さいのは、アンモニア分子間に分子間力がはたらいているためである。
この動画を見る
理想気体と実在気体に関する記述として下線部に誤りを含むものを、次の ①~⑤のうちから一つ選べ。
① 理想気体では、物質量と温度が一定であれば、圧力を変化させても圧力と 体積の積は変化しない。
② 理想気体では、体積一定のまま温度を下げると圧力は単調に減少する。
③ 理想気体では、気体分子自身の体積はないものと仮定している。
④ 実在気体は、常圧では温度が低いほど理想気体に近いふるまいをする。
⑤ 実在気体であるアンモニア$1mol$の体積が、標準状態において$22.4L$より小さいのは、アンモニア分子間に分子間力がはたらいているためである。
1分で解いてほしい化学計算問題 (21) 金属結晶の密度

単元:
#化学#化学基礎1ー物質の構成#化学結合#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 愛知医科大学]
アルミニウムの単体は面心立方格子の結晶構造をもつ金属であり、単位格子の一辺の長さは$4.0×10^{-8}cm$であるとする。
アルミニウムの密度は 何$g/cm^3$か。
有効数字2桁で答えよ。
アボガドロ定数 $6.0×10^{23}/mol AI$の原子量 $27.0$
この動画を見る
[2023年 愛知医科大学]
アルミニウムの単体は面心立方格子の結晶構造をもつ金属であり、単位格子の一辺の長さは$4.0×10^{-8}cm$であるとする。
アルミニウムの密度は 何$g/cm^3$か。
有効数字2桁で答えよ。
アボガドロ定数 $6.0×10^{23}/mol AI$の原子量 $27.0$
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問2 ナトリウムの単位格子
単元:
#化学#化学基礎1ー物質の構成#化学結合#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
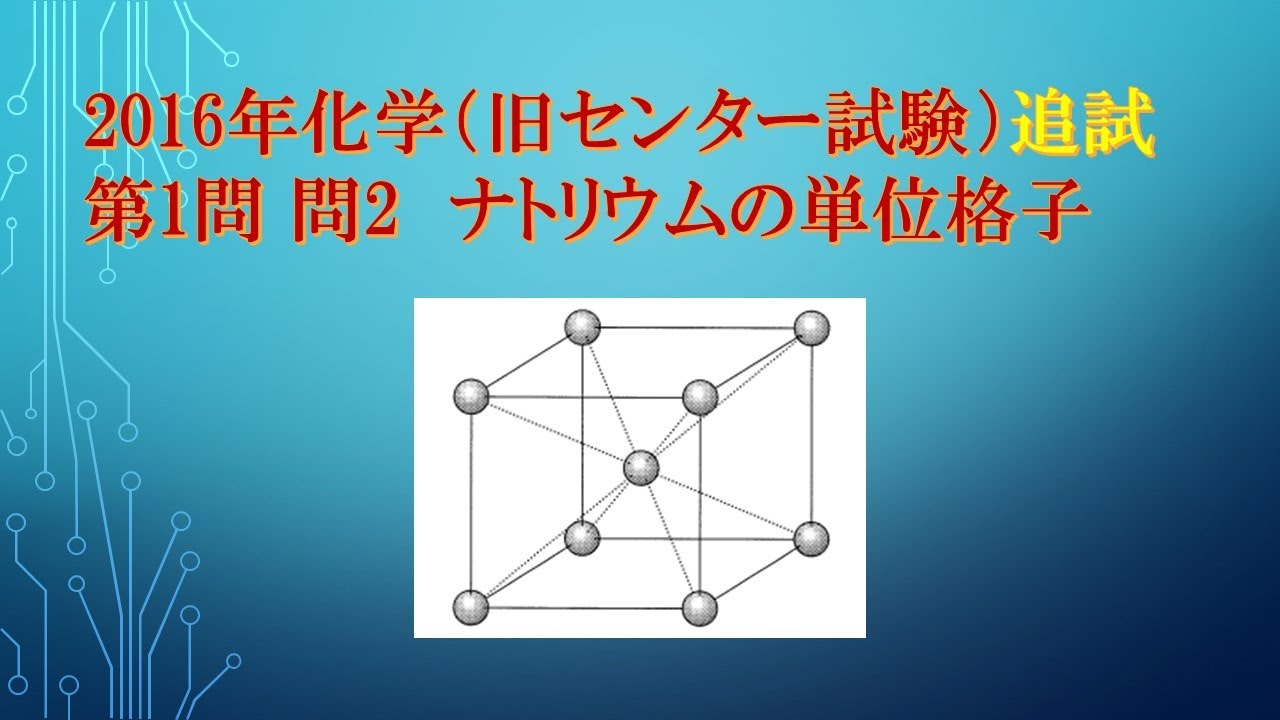
金属結晶では、金属原子が規則正しく配列している。
金属ナトリウムの単位格子は、図1の立方体で表される。
金属ナトリウムの密度を$d[g/cm^3]$.
ナトリウムのモル質量を$W(g/mol]$、
アボガドロ定数を$N_{A} 〔/mol〕$としたとき、
単位格子の体積を表す式として正しいものを、
下の①~⑥のうちから一つ選べ。
①$\displaystyle \frac{WN_{A}}{d}$
②$\displaystyle \frac{2WN_{A}}{d}$
③$\displaystyle \frac{5WN_{A}}{d}$
④$\displaystyle \frac{W}{dN_{A}}$
⑤$\displaystyle \frac{2W}{dN_{A}}$
⑥$\displaystyle \frac{5W}{dN_{A}}$
この動画を見る
金属結晶では、金属原子が規則正しく配列している。
金属ナトリウムの単位格子は、図1の立方体で表される。
金属ナトリウムの密度を$d[g/cm^3]$.
ナトリウムのモル質量を$W(g/mol]$、
アボガドロ定数を$N_{A} 〔/mol〕$としたとき、
単位格子の体積を表す式として正しいものを、
下の①~⑥のうちから一つ選べ。
①$\displaystyle \frac{WN_{A}}{d}$
②$\displaystyle \frac{2WN_{A}}{d}$
③$\displaystyle \frac{5WN_{A}}{d}$
④$\displaystyle \frac{W}{dN_{A}}$
⑤$\displaystyle \frac{2W}{dN_{A}}$
⑥$\displaystyle \frac{5W}{dN_{A}}$
1分で解いてほしい化学計算問題 (20) 糖の加水分解

単元:
#化学#化学(高分子)#糖類#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023年 青山学院大学(改)〕
空欄にあてはまる数値を整数で答えよ。
(原子量:$H 1 C 12 O 16$)
セルロース$90g$をセルラーゼアーゼで加水分離すると、
すべてグルコースになった。
このとき、グルコースは( )$g$得られた。
この動画を見る
〔2023年 青山学院大学(改)〕
空欄にあてはまる数値を整数で答えよ。
(原子量:$H 1 C 12 O 16$)
セルロース$90g$をセルラーゼアーゼで加水分離すると、
すべてグルコースになった。
このとき、グルコースは( )$g$得られた。
化学基礎の教科書を解説する動画 第3回 放射性同位体と半減期

単元:
#化学#化学基礎1ー物質の構成#原子の構成と元素の周期表#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎 教科書の解説
〔放射線同位体と半減期〕
(例題)
遺跡中の木材の$^{19}C$の割合が大気中の$\displaystyle \frac{1}{4}$だったとき、木材が切られたのは何年前か?
この動画を見る
化学基礎 教科書の解説
〔放射線同位体と半減期〕
(例題)
遺跡中の木材の$^{19}C$の割合が大気中の$\displaystyle \frac{1}{4}$だったとき、木材が切られたのは何年前か?
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第6問 問1 化学結合の種類

単元:
#化学#化学基礎1ー物質の構成#化学結合#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
共有結合を含まない物質を、次の①~⑥のうちから一つ選べ。
①水素 ②オゾン ③カリウム
④単斜硫黄 ⑤ベンゼン ⑥塩化水素
この動画を見る
共有結合を含まない物質を、次の①~⑥のうちから一つ選べ。
①水素 ②オゾン ③カリウム
④単斜硫黄 ⑤ベンゼン ⑥塩化水素
無機化学第21回 遷移元素の特徴

有機化学第24回 セッケン

共通テスト(旧センター試験)過去問解説 化学 2015年追試 第6問 問3 ペプチドの性質
単元:
#化学#化学(高分子)#アミノ酸とタンパク質、核酸#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
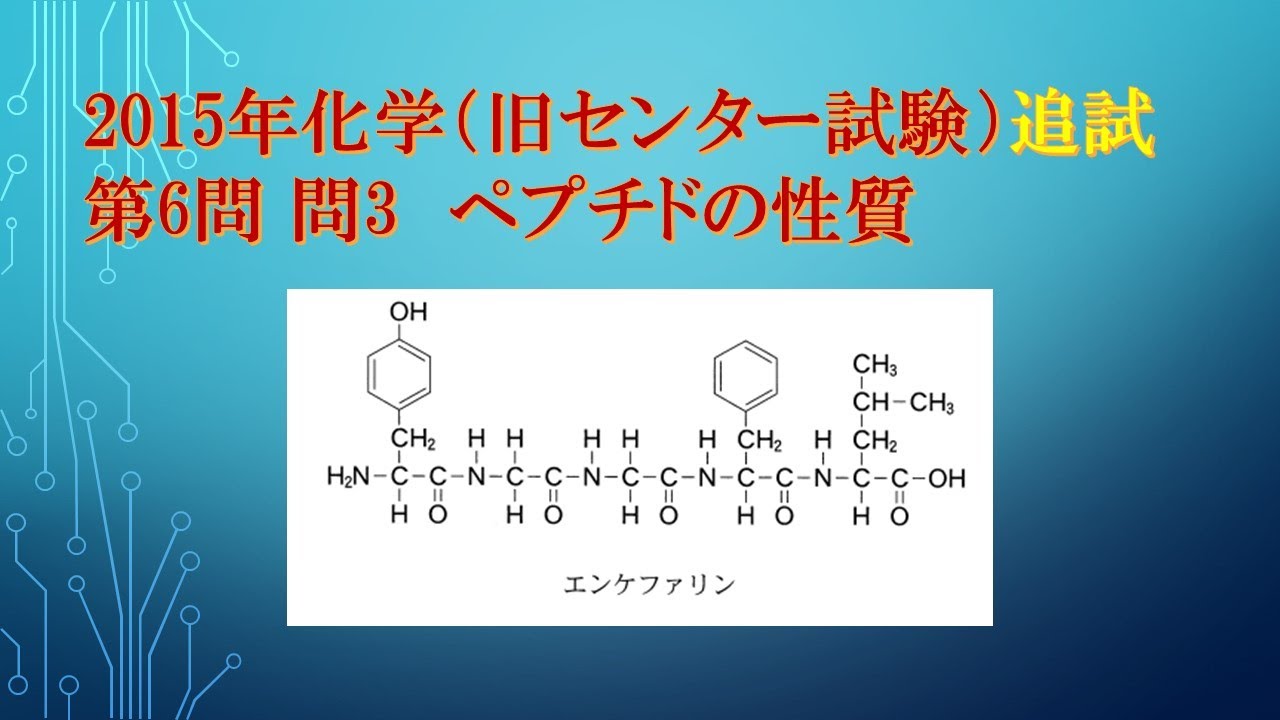
次の構造式で示される化合物エンケファリンは、脳内鎮痛ペプチドである。
この化合物に対して実験Ⅰおよび実験Ⅱを行った。
これらの実験の結果として 最も適当なものを、下の①~⑤のうちから一つずつ選べ。
ただし、同じものを 選んでもよい。
実験Ⅰ:水酸化ナトリウム水溶液と少量の薄い硫酸銅(Ⅱ) 水溶液を加えた。
実験Ⅰの結果 $\boxed{ 3 }$
実験Ⅱ:濃硝酸を加えて加熱した。
実験Ⅱの結果 $\boxed{ 4 }$
① 赤紫色になった。
② 黄色になった。
③ 黒色沈殿を生じた。
④ 白色沈殿を生じた。
⑤ 色の変化はなく、沈殿も生じなかった。
※図は動画内参照
この動画を見る
次の構造式で示される化合物エンケファリンは、脳内鎮痛ペプチドである。
この化合物に対して実験Ⅰおよび実験Ⅱを行った。
これらの実験の結果として 最も適当なものを、下の①~⑤のうちから一つずつ選べ。
ただし、同じものを 選んでもよい。
実験Ⅰ:水酸化ナトリウム水溶液と少量の薄い硫酸銅(Ⅱ) 水溶液を加えた。
実験Ⅰの結果 $\boxed{ 3 }$
実験Ⅱ:濃硝酸を加えて加熱した。
実験Ⅱの結果 $\boxed{ 4 }$
① 赤紫色になった。
② 黄色になった。
③ 黒色沈殿を生じた。
④ 白色沈殿を生じた。
⑤ 色の変化はなく、沈殿も生じなかった。
※図は動画内参照


