 化学理論
化学理論
 化学理論
化学理論
1分で解いてほしい化学計算問題 (25) 鉛蓄電池の放電による質量変化

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023年 愛知工業大学(改)〕
鉛蓄電池の構成は、次のように表される。
$\begin{array}{c|c}
(-)Pb & H_2SO_{4aq} &PbO_2(+) \\
\\
\end{array}$
この電池の両極を外部回路に接続し、$2.0A$の一定電流で1時間20分25秒間放電させたとき、この放電による負極の質量の変化を$+,-$をつけて有効数字2桁で答えなさい。
(原子量:H 1 O 16 S 32 Pb 207 $,ファデラー定数 9.65 \times 10^4C/mol$)
この動画を見る
〔2023年 愛知工業大学(改)〕
鉛蓄電池の構成は、次のように表される。
$\begin{array}{c|c}
(-)Pb & H_2SO_{4aq} &PbO_2(+) \\
\\
\end{array}$
この電池の両極を外部回路に接続し、$2.0A$の一定電流で1時間20分25秒間放電させたとき、この放電による負極の質量の変化を$+,-$をつけて有効数字2桁で答えなさい。
(原子量:H 1 O 16 S 32 Pb 207 $,ファデラー定数 9.65 \times 10^4C/mol$)
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問2 メタンハイドレート

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
将来のエネルギー資源として期待されているメタンハイドレートは、水分子 が形成するかご状構造の中にメタン分子が取り込まれた固体物質として海底な どに存在する。メタン1分子あたり平均$5.8$個の水分子で構成されるメタンハ イドレート $1.2kg$から、メタンを気体としてすべて取り出して完全燃焼させる。
次の問い(a・b)に答えよ。
原子量
$H1 C 12 Ο 16$
a 燃焼で消費される酸素の物質量は何$mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$5.0$ ②$10$ ③$20$ ④$65$ ⑤$75$ ⑥$130$
b このとき発生する熱量は何$kJ$か。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
ただし、気体のメタンの燃焼熱は$890 kJ/mol$とする。
①$8.9 \times 10^2$
②$4.5 \times 10^3$
③$5.8 \times 10^3$
④$8.9 \times 10^3$
⑤$4.5 \times 10^4$
⑥$5.8 \times 10^4$
この動画を見る
将来のエネルギー資源として期待されているメタンハイドレートは、水分子 が形成するかご状構造の中にメタン分子が取り込まれた固体物質として海底な どに存在する。メタン1分子あたり平均$5.8$個の水分子で構成されるメタンハ イドレート $1.2kg$から、メタンを気体としてすべて取り出して完全燃焼させる。
次の問い(a・b)に答えよ。
原子量
$H1 C 12 Ο 16$
a 燃焼で消費される酸素の物質量は何$mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$5.0$ ②$10$ ③$20$ ④$65$ ⑤$75$ ⑥$130$
b このとき発生する熱量は何$kJ$か。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
ただし、気体のメタンの燃焼熱は$890 kJ/mol$とする。
①$8.9 \times 10^2$
②$4.5 \times 10^3$
③$5.8 \times 10^3$
④$8.9 \times 10^3$
⑤$4.5 \times 10^4$
⑥$5.8 \times 10^4$
【この一本でバッチリ!!】化学反応と触媒(活性化エネルギー活性化状態均一系触媒・不均一系触媒)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#化学反応の速さ#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
化学反応と触媒について解説します。
活性化エネルギー活性化状態均一系触媒・不均一系触媒
この動画を見る
化学反応と触媒について解説します。
活性化エネルギー活性化状態均一系触媒・不均一系触媒
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第2問 問1 熱化学方程式

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
アンモニア(気)と塩化水素(気)から塩化アンモニウム(固)が生成する反応の反応熱は$176 kJ/mol$である。
塩化アンモニウム(固)の生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑧のうちから一つ選べ。
ただし、アンモニア(気) および塩化水素(気)の生成熱は、
それぞれ$46 kJ/mol$ および$92 kJ/mol$である。
①$-314$ ②$-176$ ③$-138$ ④$-38$ ⑤$38$ ⑥$138$ ⑦$176$ ⑧$314$
この動画を見る
アンモニア(気)と塩化水素(気)から塩化アンモニウム(固)が生成する反応の反応熱は$176 kJ/mol$である。
塩化アンモニウム(固)の生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑧のうちから一つ選べ。
ただし、アンモニア(気) および塩化水素(気)の生成熱は、
それぞれ$46 kJ/mol$ および$92 kJ/mol$である。
①$-314$ ②$-176$ ③$-138$ ④$-38$ ⑤$38$ ⑥$138$ ⑦$176$ ⑧$314$
1分で解いてほしい化学計算問題 (23) 状態変化と熱量

単元:
#化学#化学理論#物質の変化と熱・光#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
20$^{ \circ }$の水180gを加熱して100$^{ \circ }$の水蒸気にしたい。
必要な熱量[kJ]として、最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、液体の水1gを1K温度上昇させるのに必要な熱量は4.2J、水100$^{ \circ }$での蒸発熱は41kJ/molである。
水の分子量:18[2021年 成蹊大学]
①$60$
②$80$
③$1.0\times10^2$
④$4.1\times10^2$
⑤$4.7\times10^2$
⑥$5.3\times10^2$
この動画を見る
20$^{ \circ }$の水180gを加熱して100$^{ \circ }$の水蒸気にしたい。
必要な熱量[kJ]として、最も適当なものを下の①~⑥のうちから一つ選べ。
ただし、液体の水1gを1K温度上昇させるのに必要な熱量は4.2J、水100$^{ \circ }$での蒸発熱は41kJ/molである。
水の分子量:18[2021年 成蹊大学]
①$60$
②$80$
③$1.0\times10^2$
④$4.1\times10^2$
⑤$4.7\times10^2$
⑥$5.3\times10^2$
ナメクジが塩で溶ける理由

【この一本でバッチリ!!】反応速度を変える条件〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#化学反応の速さ#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
反応速度
反応速度を変える条件について解説します。
1.0mol/L過酸化水素水10mLに少量の塩化鉄(III)水溶液を加えると、過酸化水素が分解して酸素が発生した。
また、過酸化水素の濃度は、反応開始から2分後に0.64mol/Lになった。
この間の過酸化水素の分解速度は何mol/(L・s)か。
また、酸素の発生速度は何mol/sか。
この動画を見る
反応速度
反応速度を変える条件について解説します。
1.0mol/L過酸化水素水10mLに少量の塩化鉄(III)水溶液を加えると、過酸化水素が分解して酸素が発生した。
また、過酸化水素の濃度は、反応開始から2分後に0.64mol/Lになった。
この間の過酸化水素の分解速度は何mol/(L・s)か。
また、酸素の発生速度は何mol/sか。
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問5 気体の溶解(ヘンリーの法則)

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
この動画を見る
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
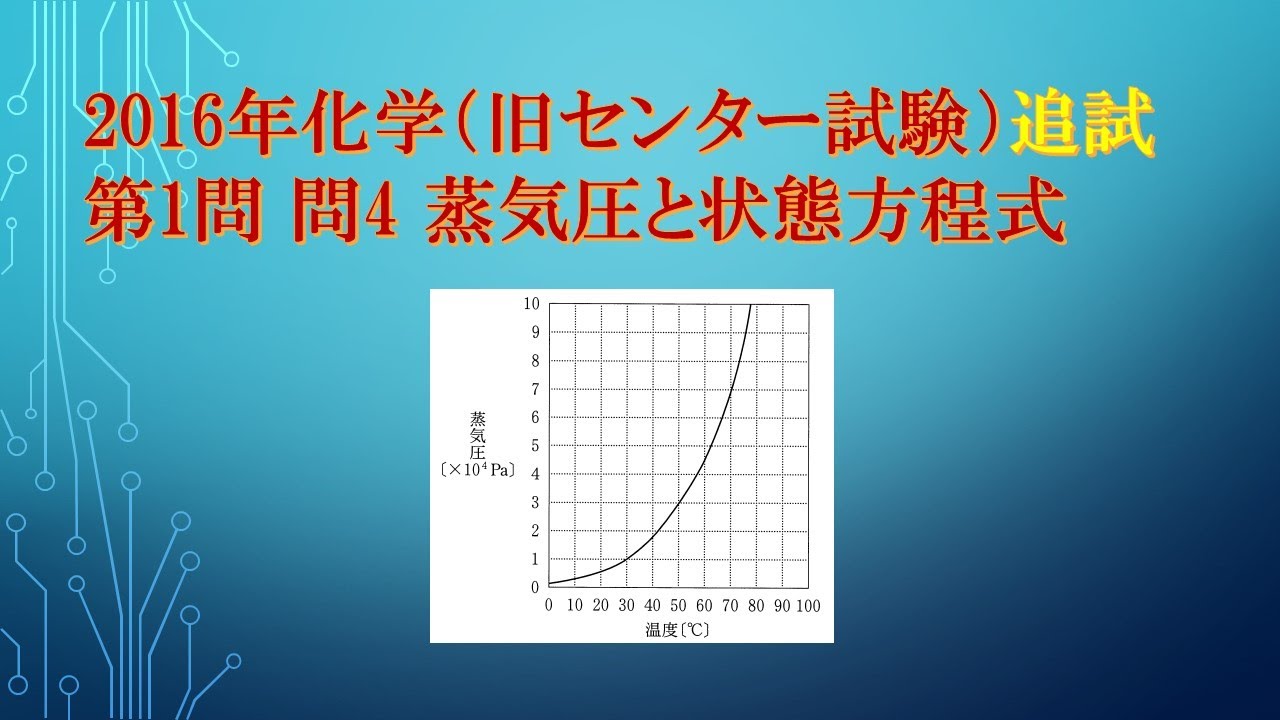
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問4 蒸気圧と状態方程式
単元:
#化学#化学理論#大学入試過去問(化学)#化学平衡と平衡移動#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
図2はエタノールの蒸気圧曲線である。
容積 $1.0L$の密閉容器に $0.010 mol$ のエタノールのみが入っている。
容器の温度が$40℃$および$60℃$のとき、容器内の圧力はそれぞれ何か、圧力の値の組合せとして最も適当なものを、下の①~⑦のうちから一つ選べ。
ただし、気体定数は $R = 8.3 × 10^2 Pa-L/(K・mol)$とする。
また、容器内での液体の体積は無視できるものとする。
※表・図は動画内参照
この動画を見る
図2はエタノールの蒸気圧曲線である。
容積 $1.0L$の密閉容器に $0.010 mol$ のエタノールのみが入っている。
容器の温度が$40℃$および$60℃$のとき、容器内の圧力はそれぞれ何か、圧力の値の組合せとして最も適当なものを、下の①~⑦のうちから一つ選べ。
ただし、気体定数は $R = 8.3 × 10^2 Pa-L/(K・mol)$とする。
また、容器内での液体の体積は無視できるものとする。
※表・図は動画内参照
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第6問 問3 理想気体と実在気体

単元:
#化学#化学理論#大学入試過去問(化学)#気体の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
理想気体と実在気体に関する記述として下線部に誤りを含むものを、次の ①~⑤のうちから一つ選べ。
① 理想気体では、物質量と温度が一定であれば、圧力を変化させても圧力と 体積の積は変化しない。
② 理想気体では、体積一定のまま温度を下げると圧力は単調に減少する。
③ 理想気体では、気体分子自身の体積はないものと仮定している。
④ 実在気体は、常圧では温度が低いほど理想気体に近いふるまいをする。
⑤ 実在気体であるアンモニア$1mol$の体積が、標準状態において$22.4L$より小さいのは、アンモニア分子間に分子間力がはたらいているためである。
この動画を見る
理想気体と実在気体に関する記述として下線部に誤りを含むものを、次の ①~⑤のうちから一つ選べ。
① 理想気体では、物質量と温度が一定であれば、圧力を変化させても圧力と 体積の積は変化しない。
② 理想気体では、体積一定のまま温度を下げると圧力は単調に減少する。
③ 理想気体では、気体分子自身の体積はないものと仮定している。
④ 実在気体は、常圧では温度が低いほど理想気体に近いふるまいをする。
⑤ 実在気体であるアンモニア$1mol$の体積が、標準状態において$22.4L$より小さいのは、アンモニア分子間に分子間力がはたらいているためである。
【この一本でバッチリ!!】鉛蓄電池の計算問題〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
Q.鉛蓄電池を放電して、$3.86×10^3$Cの電気量を取り出した。
このとき、負極、正極、電解質溶液の質量変化をそれぞれ求めよ。
H:$1.0$,0:$16$,S:$32$,Pb:$207$, ファラデー定数F:$9.65×10^4$
この動画を見る
Q.鉛蓄電池を放電して、$3.86×10^3$Cの電気量を取り出した。
このとき、負極、正極、電解質溶液の質量変化をそれぞれ求めよ。
H:$1.0$,0:$16$,S:$32$,Pb:$207$, ファラデー定数F:$9.65×10^4$
【この一本でバッチリ!!】電気分解まとめ(電気分解基礎・計算・陽イオン交換膜法・銅の電解精錬・アルミニウムの溶融塩電解)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
電気分解についてまとめました。
電気分解基礎・計算・陽イオン交換膜法・銅の電解精錬・アルミニウムの溶融塩電解
この動画を見る
電気分解についてまとめました。
電気分解基礎・計算・陽イオン交換膜法・銅の電解精錬・アルミニウムの溶融塩電解
【この一本でバッチリ!!】電池まとめ(ダニエル電池・ボルタ電池・鉛蓄電池・燃料電池・実用電池・リチウムイオン・電池計算)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
電池についてまとめました。
ダニエル電池・ボルタ電池・鉛蓄電池・燃料電池・実用電池・リチウムイオン電池
この動画を見る
電池についてまとめました。
ダニエル電池・ボルタ電池・鉛蓄電池・燃料電池・実用電池・リチウムイオン電池
空が青い理由

化学基礎の教科書を解説する動画 第63回 電池(ダニエル電池)

1分で解いてほしい化学計算問題 (12) 圧平衡定数

単元:
#化学#化学理論#化学平衡と平衡移動#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 京都産業大学(改)〕
密閉容器中、温度$1000K$で、次の反応が平衛状態となっている。
$CO_2$(気)$+C$(固)$⇄2CO$(気)
全圧は$1.0 \times 10^5Pa,CO$の体積百分率は$80%$であった。
このときの圧平衛定数を単位をつけて有効数字2桁で求めよ。
この動画を見る
〔2023 京都産業大学(改)〕
密閉容器中、温度$1000K$で、次の反応が平衛状態となっている。
$CO_2$(気)$+C$(固)$⇄2CO$(気)
全圧は$1.0 \times 10^5Pa,CO$の体積百分率は$80%$であった。
このときの圧平衛定数を単位をつけて有効数字2桁で求めよ。
1分で解いてほしい化学計算問題 (11) 過酸化水素の平均分解速度

単元:
#化学#化学理論#化学反応の速さ#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2022 金城学院大学(改)〕
ある濃度の過酸化水素水に、ある濃度の塩化鉄(Ⅲ)水溶液を加え$100mL$とした。
反応開始から発生した酸素物質量を、時間を追って測定したところ、次の表に示す結果が得られた。
最初に$20$秒間において、混合水溶液中の過酸化水素の平均分解速度は何$moL/(L・S)$か、有効数字2桁で答えよ。
※表は動画内参照
この動画を見る
〔2022 金城学院大学(改)〕
ある濃度の過酸化水素水に、ある濃度の塩化鉄(Ⅲ)水溶液を加え$100mL$とした。
反応開始から発生した酸素物質量を、時間を追って測定したところ、次の表に示す結果が得られた。
最初に$20$秒間において、混合水溶液中の過酸化水素の平均分解速度は何$moL/(L・S)$か、有効数字2桁で答えよ。
※表は動画内参照
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第3問 問4 鉱石中の元素の存在比

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
銅と鉄と硫黄のみからなる鉱石$6.72kg$に高温で空気を吹き込むと、反応が完全に進行し、銅、二酸化硫黄および酸化鉄のみが生成した。
このとき、銅は$1.28kg$得られた。
二酸化硫黄はセッコウ($CaSO_4・2H_2O$ 式量172)$17.2kg$とあいて回収された。
鉱石中の銅と鉄の原子数の比(銅:鉄)として最も適当なものを、次の①~⑥のうちから一つ選べ。
① $1:1$ ② $1:2$ ③ $1:3$ ④ $2:1$ ⑤ $2:3$ ⑥ $3:1$
原子量:$S 32 Fe 56 Cu 64$
この動画を見る
銅と鉄と硫黄のみからなる鉱石$6.72kg$に高温で空気を吹き込むと、反応が完全に進行し、銅、二酸化硫黄および酸化鉄のみが生成した。
このとき、銅は$1.28kg$得られた。
二酸化硫黄はセッコウ($CaSO_4・2H_2O$ 式量172)$17.2kg$とあいて回収された。
鉱石中の銅と鉄の原子数の比(銅:鉄)として最も適当なものを、次の①~⑥のうちから一つ選べ。
① $1:1$ ② $1:2$ ③ $1:3$ ④ $2:1$ ⑤ $2:3$ ⑥ $3:1$
原子量:$S 32 Fe 56 Cu 64$
1分で解いてほしい化学計算問題 (6) ボイルの法則

単元:
#化学#化学理論#大学入試過去問(化学)#気体の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2022 麻布大学 (改)〕
一定温度で$2.00 × 10^5\,\rm{Pa}$の圧力を示す一定量の気体を祖の体積が$500\,\rm{mL}$だけ小さくなるまで圧縮すると、気体の圧力が$2.50 × 10^5\,\rm{Pa}$に上昇した。
圧縮前の気体が占めていた体積〔$\rm{L}$〕を求めなさい。
この動画を見る
〔2022 麻布大学 (改)〕
一定温度で$2.00 × 10^5\,\rm{Pa}$の圧力を示す一定量の気体を祖の体積が$500\,\rm{mL}$だけ小さくなるまで圧縮すると、気体の圧力が$2.50 × 10^5\,\rm{Pa}$に上昇した。
圧縮前の気体が占めていた体積〔$\rm{L}$〕を求めなさい。
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第3問 問3 気体の捕集法

単元:
#化学#化学理論#大学入試過去問(化学)#気体の性質#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
表1に示す2種類の薬品の反応によって発生する気体ア~オのうち、水上置換で捕集できないものの組合せを、下の①~⑤のうちから一つ選べ。
① アとイ
② イとウ
③ ウとエ
④ エとオ
⑤ アとオ
※表は動画内参照
この動画を見る
表1に示す2種類の薬品の反応によって発生する気体ア~オのうち、水上置換で捕集できないものの組合せを、下の①~⑤のうちから一つ選べ。
① アとイ
② イとウ
③ ウとエ
④ エとオ
⑤ アとオ
※表は動画内参照
これなに?

1分で解いてほしい化学計算問題 (2) 混合気体の全圧

単元:
#化学#化学理論#気体の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023星薬科大学(推薦・改)〕
一定温度のもとで、$1.2×10^5Pa$のヘリウム$3.0L$と$2.6×10^5Pa$の窒素$2.0L$を混合し、混合気体の体積を$4.0L$とした。
この混合気体全圧〔$Pa$〕を有効数字2桁で求めなさい。
この動画を見る
〔2023星薬科大学(推薦・改)〕
一定温度のもとで、$1.2×10^5Pa$のヘリウム$3.0L$と$2.6×10^5Pa$の窒素$2.0L$を混合し、混合気体の体積を$4.0L$とした。
この混合気体全圧〔$Pa$〕を有効数字2桁で求めなさい。
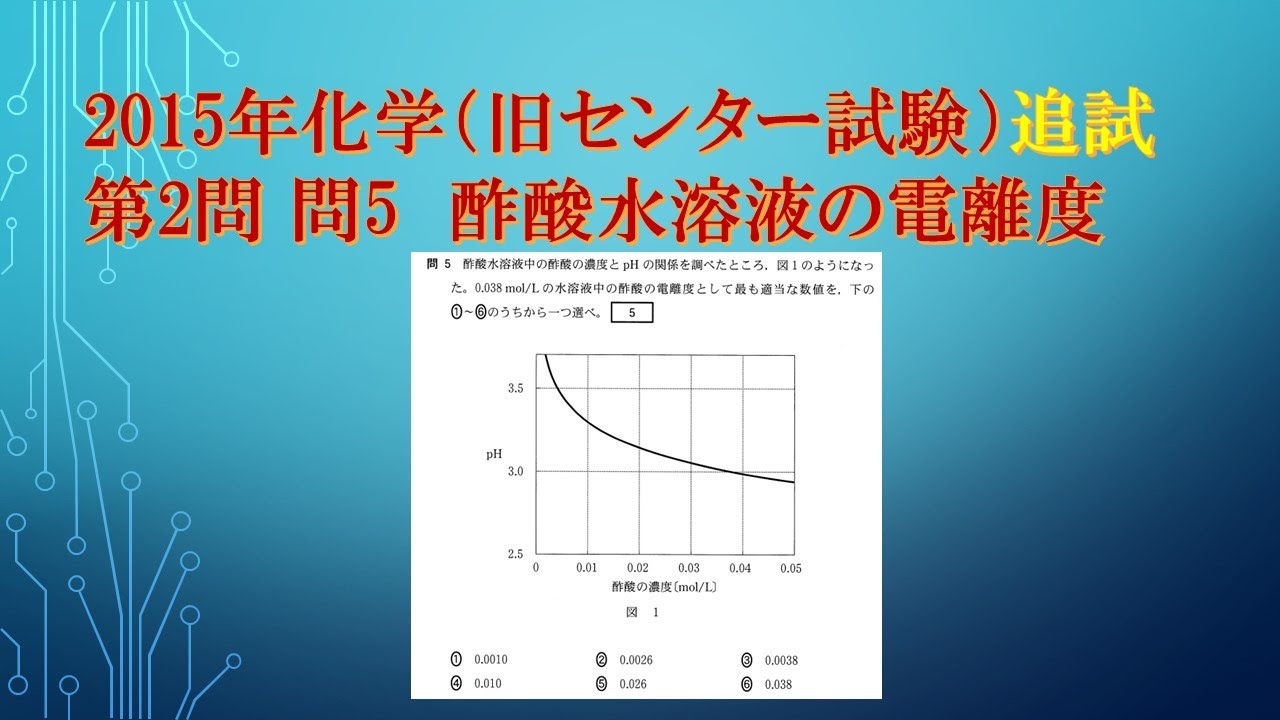
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第2問 問5 酢酸水溶液の電離度
単元:
#化学#化学理論#化学平衡と平衡移動#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
酢酸水溶液中の酢酸の濃度と$pH$の関係を調べたところ、図1のようになっ た。
$0.038 mol/L$の水溶液中の酢酸の電離度として最も適当な数値を、
下の ①~⑥のうちから一つ選べ。
①$0.0010$ ②$0.0026$ ③$0.0038$
④$0.010$ ⑤$0.026$ ⑥$0.038$
※図は動画内参照
この動画を見る
酢酸水溶液中の酢酸の濃度と$pH$の関係を調べたところ、図1のようになっ た。
$0.038 mol/L$の水溶液中の酢酸の電離度として最も適当な数値を、
下の ①~⑥のうちから一つ選べ。
①$0.0010$ ②$0.0026$ ③$0.0038$
④$0.010$ ⑤$0.026$ ⑥$0.038$
※図は動画内参照
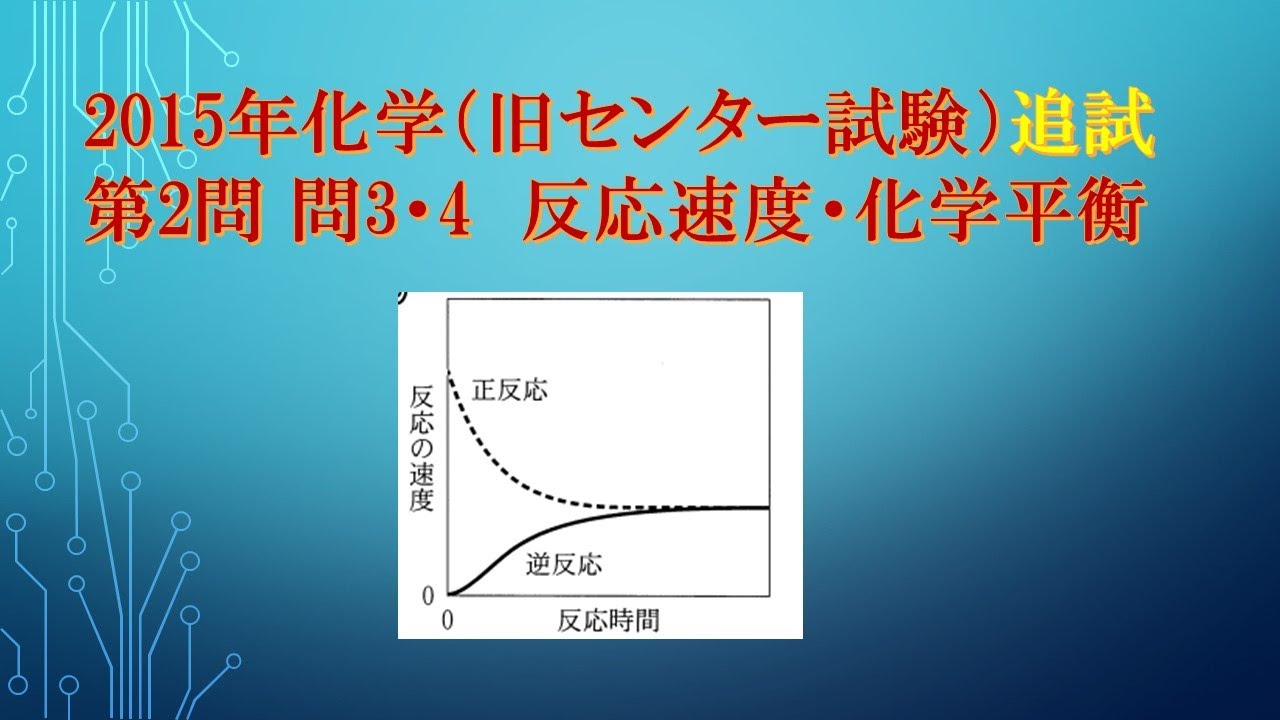
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第2問 問3・4 反応速度・化学平衡
単元:
#化学#化学理論#化学平衡と平衡移動#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
一定温度,一定体積の密閉容器内で、$H_2$(気)と$I_2$(気)を混合したところ、 $HI$ (気)が生成して平衡状態に達した。
混合してから平衡状態に達するまでの 正反応(破線)と逆反応(実線)の速度の変化として最も適当なものを、次の①~ ⑥のうちから一つ選べ。
ただし、正反応の速度の変化(破線)はすべての選択肢で同じである。
※図は動画内参照
平衡反応における触媒の作用に関する一般的記述として誤りを含むものを、 次の①~⑤のうちから一つ選べ。
① 触媒を加えても、正反応の反応速度は変化しない。
② 触媒を加えても、反応熱は変化しない。
③ 触媒を加えると、正反応の活性化エネルギーは小さくなる。
④ 触媒を加えると、逆反応の活性化エネルギーは小さくなる。
⑤ 反応が平衡に達したのちに触媒を加えても、平衡は移動しない。
この動画を見る
一定温度,一定体積の密閉容器内で、$H_2$(気)と$I_2$(気)を混合したところ、 $HI$ (気)が生成して平衡状態に達した。
混合してから平衡状態に達するまでの 正反応(破線)と逆反応(実線)の速度の変化として最も適当なものを、次の①~ ⑥のうちから一つ選べ。
ただし、正反応の速度の変化(破線)はすべての選択肢で同じである。
※図は動画内参照
平衡反応における触媒の作用に関する一般的記述として誤りを含むものを、 次の①~⑤のうちから一つ選べ。
① 触媒を加えても、正反応の反応速度は変化しない。
② 触媒を加えても、反応熱は変化しない。
③ 触媒を加えると、正反応の活性化エネルギーは小さくなる。
④ 触媒を加えると、逆反応の活性化エネルギーは小さくなる。
⑤ 反応が平衡に達したのちに触媒を加えても、平衡は移動しない。
これなんで?

お酒が凍らない理由とは?

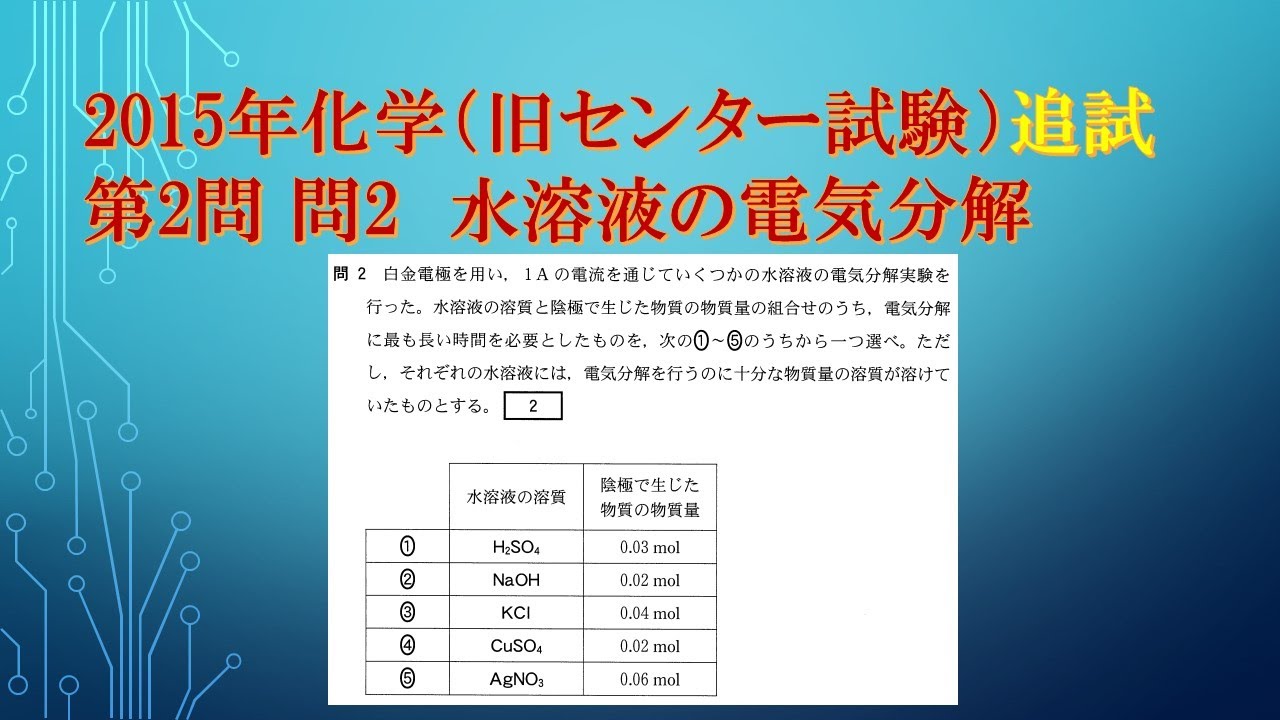
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第2問 問2 水溶液の電気分解
単元:
#化学#化学理論#電池と電気分解#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
白金電極を用い、1Aの電流を通じていくつかの水溶液の電気分解実験を行った。
水溶液の溶質と陰極で生じた物質の物質量の組合せのうち、
電気分解に最も長い時間を必要としたものを、次の①~⑤のうちから一つ選べ。
ただ し、それぞれの水溶液には、電気分解を行うのに十分な物質量の溶質が溶けて いたものとする。
※表は動画内参照
この動画を見る
白金電極を用い、1Aの電流を通じていくつかの水溶液の電気分解実験を行った。
水溶液の溶質と陰極で生じた物質の物質量の組合せのうち、
電気分解に最も長い時間を必要としたものを、次の①~⑤のうちから一つ選べ。
ただ し、それぞれの水溶液には、電気分解を行うのに十分な物質量の溶質が溶けて いたものとする。
※表は動画内参照
凍らせたスポーツドリンクが濃い理由とは?

単元:
#化学#化学理論#物質の三態と状態変化#理科(高校生)
指導講師:
【楽しい授業動画】あきとんとん
問題文全文(内容文):
凍らせたスポーツドリンクの溶けだしたものが濃い理由について解説
この動画を見る
凍らせたスポーツドリンクの溶けだしたものが濃い理由について解説
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第2問 問1 熱化学

単元:
#化学#化学理論#物質の変化と熱・光#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ベンゼン $2.00 mol$と水素 $6.00 mol$から
シクロヘキサン $2.00 mol$ が生成するときに
発生する熱量は$410kJ$であった。
ペンゼンの生成熱を$-49kJ/mol$とすると、シクロヘキサンの生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$156$ ②$254$ ③$312$
④$361$⑤$459$⑥$508$
この動画を見る
ベンゼン $2.00 mol$と水素 $6.00 mol$から
シクロヘキサン $2.00 mol$ が生成するときに
発生する熱量は$410kJ$であった。
ペンゼンの生成熱を$-49kJ/mol$とすると、シクロヘキサンの生成熱は何$kJ/mol$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$156$ ②$254$ ③$312$
④$361$⑤$459$⑥$508$
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第1問 問6 溶解度曲線
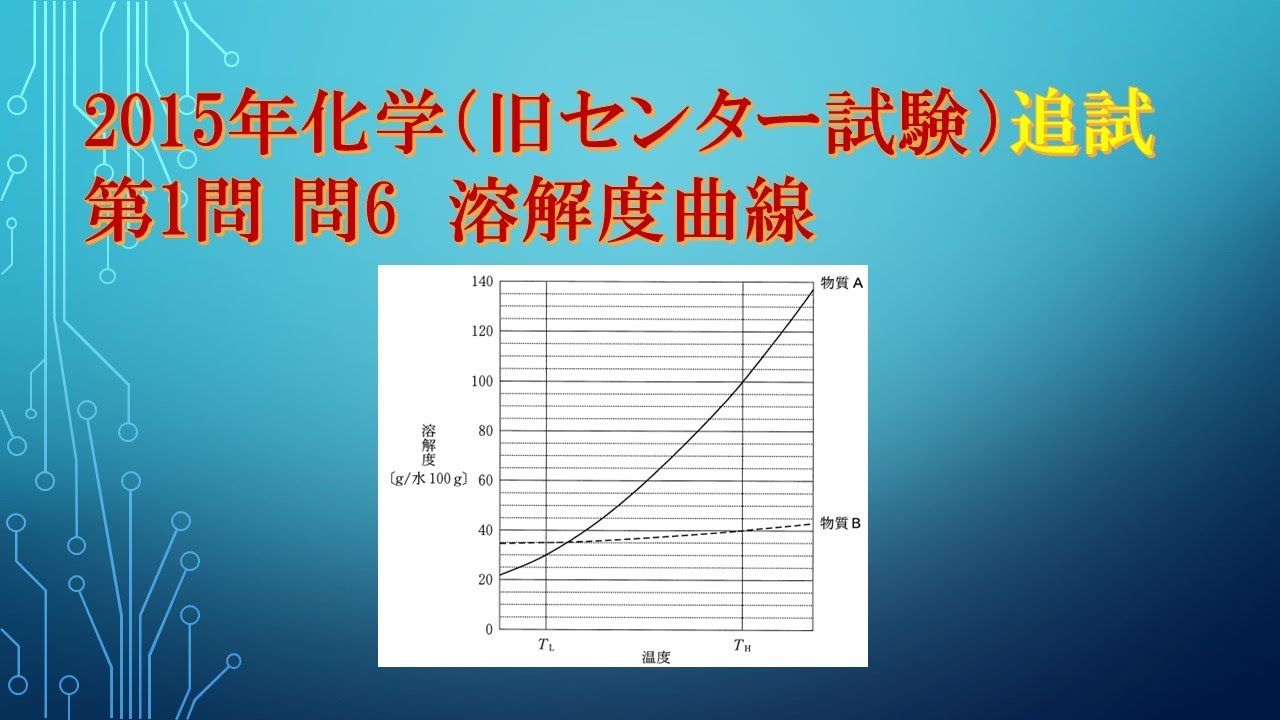
単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
図1は物質Aと物質Bの溶解度曲線を示している。
Aを140gとBを20g含む混合物を温度$T_H$の水100gに加えて十分にかきまぜた後、温度を$T_H$に保ったままでろ過した。
ろ液を温度$T_L$まで冷却したとき、AとBはそれぞれ何g析出するか。
最も適当な組合せを、下の①~⑥のうちから一つ選べ。
ただし、AとBは互いの溶解度に影響せず、いずれも水和水(結晶水)をもたない物質とする。
※図・表は動画内参照
この動画を見る
図1は物質Aと物質Bの溶解度曲線を示している。
Aを140gとBを20g含む混合物を温度$T_H$の水100gに加えて十分にかきまぜた後、温度を$T_H$に保ったままでろ過した。
ろ液を温度$T_L$まで冷却したとき、AとBはそれぞれ何g析出するか。
最も適当な組合せを、下の①~⑥のうちから一つ選べ。
ただし、AとBは互いの溶解度に影響せず、いずれも水和水(結晶水)をもたない物質とする。
※図・表は動画内参照
