 化学基礎2ー物質の変化
化学基礎2ー物質の変化
 化学基礎2ー物質の変化
化学基礎2ー物質の変化
1分で解いてほしい化学計算問題 (18) 陽イオン交換樹脂

単元:
#化学#化学基礎2ー物質の変化#酸と塩基・水素イオン濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2022年 明星大学(改)]
濃度不明の塩化カルシウム$CaCl_2$水溶液$25mL$を、十分な量の陽イオン 交換樹脂に通した。
$25mL$の流出液を$0.10mol/L$の水酸化ナトリウム $NaOH$水溶液で滴定したところ、$20mL$加えたところで中和が完了し た。
この$CaCl_2$水溶液の濃度は何$mol/L$か。
有効数字2桁で答えなさい。
この動画を見る
[2022年 明星大学(改)]
濃度不明の塩化カルシウム$CaCl_2$水溶液$25mL$を、十分な量の陽イオン 交換樹脂に通した。
$25mL$の流出液を$0.10mol/L$の水酸化ナトリウム $NaOH$水溶液で滴定したところ、$20mL$加えたところで中和が完了し た。
この$CaCl_2$水溶液の濃度は何$mol/L$か。
有効数字2桁で答えなさい。
【短時間で演習!!】量的関係計算・化学反応式演習〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
新課程対応 演習編
量的関係計算
標準状態で5.6Lのエタンが燃焼するとき必要な二酸化炭素は何Lか?
この動画を見る
新課程対応 演習編
量的関係計算
標準状態で5.6Lのエタンが燃焼するとき必要な二酸化炭素は何Lか?
1分で解いてほしい化学計算問題 (17) 電解質水溶液の凝固点

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2022 千葉大学(改)]
塩化ナトリウム$5.85g$を水$500g$に溶かした水溶液の凝固点は何$℃$か答 えなさい。計算過程も示し、有効数字2けたで答えなさい。
ただし、水のモル凝固点降下を$1.85K・kg/mol$とし、塩化ナトリウムはすべて電離 するものとする。
($NaCI$の式量は$58.5$)
この動画を見る
[2022 千葉大学(改)]
塩化ナトリウム$5.85g$を水$500g$に溶かした水溶液の凝固点は何$℃$か答 えなさい。計算過程も示し、有効数字2けたで答えなさい。
ただし、水のモル凝固点降下を$1.85K・kg/mol$とし、塩化ナトリウムはすべて電離 するものとする。
($NaCI$の式量は$58.5$)
1分で解いてほしい化学計算問題 (16) シュウ酸水溶液の調製

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023 中京大学(改)]
$5.00 ×10-2mol/L$のシュウ酸水溶液をつくるため、シュウ酸二水和物の結晶を$W [mg]$ 、少量の純水に溶かした後、$100mL$のメスフラスコに入れ標線まで純水を加えた。
$W$の値を有効数字3桁で求めよ。
(原子量: $H 1.0 C12 Ο 16$)
この動画を見る
[2023 中京大学(改)]
$5.00 ×10-2mol/L$のシュウ酸水溶液をつくるため、シュウ酸二水和物の結晶を$W [mg]$ 、少量の純水に溶かした後、$100mL$のメスフラスコに入れ標線まで純水を加えた。
$W$の値を有効数字3桁で求めよ。
(原子量: $H 1.0 C12 Ο 16$)
化学基礎の教科書を解説する動画 第64回 電池(燃料電池)

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎の教科書を解説する動画 電池(燃料電池)
この動画を見る
化学基礎の教科書を解説する動画 電池(燃料電池)
【違いは何!?】化学の基本法則(質量保存の法則・定比例の法則・倍数比例の法則・原子説・気体反応の法則・分子説)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
化学の基本法則について解説します。
質量保存の法則・定比例の法則・倍数比例の法則・原子説・気体反応の法則・分子説
この動画を見る
化学の基本法則について解説します。
質量保存の法則・定比例の法則・倍数比例の法則・原子説・気体反応の法則・分子説
1分で解いてほしい化学計算問題 (14) ヘンリーの法則

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021 東京理科大学(改)]
窒素は$20℃ 1.0 \times 10^5Pa$, 水$1.0L$に$7.1×10{-4}mol$溶ける。
$20℃, 1.0 \times 10^5Pa$において空気が水に接しているとき、$10L$の水に溶解している窒素$〔g〕$の質量を有効数字2桁で求めよ。
ただし、空気は窒素と酸素を体積の比$4:1$で混合した気体とする。
原子量 $N 28$
この動画を見る
[2021 東京理科大学(改)]
窒素は$20℃ 1.0 \times 10^5Pa$, 水$1.0L$に$7.1×10{-4}mol$溶ける。
$20℃, 1.0 \times 10^5Pa$において空気が水に接しているとき、$10L$の水に溶解している窒素$〔g〕$の質量を有効数字2桁で求めよ。
ただし、空気は窒素と酸素を体積の比$4:1$で混合した気体とする。
原子量 $N 28$
【連立方程式を使う!!】量的関係計算の演習〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
化学基礎 モル計算演習
メタンとプロパンの混合気体を、十分な酸素存在下で完全燃焼させると、標準状態で156.8mLの二酸化炭素と0.198gの水が得られた。
この燃焼を行うのに消費された酸素の体積は標準状態で何mL?
この動画を見る
化学基礎 モル計算演習
メタンとプロパンの混合気体を、十分な酸素存在下で完全燃焼させると、標準状態で156.8mLの二酸化炭素と0.198gの水が得られた。
この燃焼を行うのに消費された酸素の体積は標準状態で何mL?
化学基礎の教科書を解説する動画 第62回 金属の反応(2) 金属と酸の反応

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎の教科書を解説する動画
〔金属の反応(2) 金属と酸の反応〕
この動画を見る
化学基礎の教科書を解説する動画
〔金属の反応(2) 金属と酸の反応〕
【化学反応式から計算!?】量的関係計算〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
Q1 窒素1.12Lと水素を燃焼したとき、発生したアンモニアは何Lか?
Q2 亜鉛6.5gと過不足なく反応する塩化水素は何gか?
Q3 メタンとプロパンの混合気体を、完全燃焼させると、標準状態で156.8mLの二酸化炭素と0.198gの水が得られた。消費された酸素は標準状態で何mL?
Q4 酸素ガス中で無声放電を行うと、一部がオゾンに変化する。1000mLの酸素中で放電したら、一部がオゾンに変化して、全体積が970mLになった。反応した酸素は何mLか?
Q5 気体のエチレン1.4gに、標準状態で5.6Lの酸素を混合して点火すると一方の気体の一部が未反応のまま残った。未反応のまま残った気体の質量は?
この動画を見る
Q1 窒素1.12Lと水素を燃焼したとき、発生したアンモニアは何Lか?
Q2 亜鉛6.5gと過不足なく反応する塩化水素は何gか?
Q3 メタンとプロパンの混合気体を、完全燃焼させると、標準状態で156.8mLの二酸化炭素と0.198gの水が得られた。消費された酸素は標準状態で何mL?
Q4 酸素ガス中で無声放電を行うと、一部がオゾンに変化する。1000mLの酸素中で放電したら、一部がオゾンに変化して、全体積が970mLになった。反応した酸素は何mLか?
Q5 気体のエチレン1.4gに、標準状態で5.6Lの酸素を混合して点火すると一方の気体の一部が未反応のまま残った。未反応のまま残った気体の質量は?
1分で解いてほしい化学計算問題 (10) 質量モル濃度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2021 神戸薬科大学〕
質量パーセント濃度$60%$の酢酸化水溶液$50g$に水を加えて希釈して、
質量モル濃度$2.0mol/kg$の酢酸水溶液を作った。
このとき、加えた水の質量$〔g〕$はいくらか。
最も近い値を選べ。
(酢酸の分子量:$60$)
(1)$200$ (2)$230$ (3)$250$
(4)$320$ (5)$450$ (6)$480$
(7)$500$ (8)$550$ (9)$620$
この動画を見る
〔2021 神戸薬科大学〕
質量パーセント濃度$60%$の酢酸化水溶液$50g$に水を加えて希釈して、
質量モル濃度$2.0mol/kg$の酢酸水溶液を作った。
このとき、加えた水の質量$〔g〕$はいくらか。
最も近い値を選べ。
(酢酸の分子量:$60$)
(1)$200$ (2)$230$ (3)$250$
(4)$320$ (5)$450$ (6)$480$
(7)$500$ (8)$550$ (9)$620$
化学基礎の教科書を解説する動画 第61回 金属の反応(1)

【短時間でマスター!?】苦手な人の多い化学反応式の係数合わせの方法をマスター(目算法・未定係数法)〔現役講師解説、高校化学、化学基礎、2023年度版〕

1分で解いてほしい化学計算問題 (9) 酸化還元反応

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021 関西医科大学(改)]
$0.020mol/L$のシュウ酸水溶液$25mL$をコニカルビーカーにとり希硫酸を加えた。
この水溶液を温めた後に濃度がわからない過マンガン酸カリ ウム水溶液を加えていったところ、$20mL$加えたところで反応の終点をむかえた。
過マンガン酸カリウム水溶液のモル濃度は何$mol/L$か。
有効数字2桁で求めよ。
$MnO_4^{-} + 8H^{+} + 5e^{-} → Mn^{2+} + 4H_2O$
$H_2C_2O_4 → 2CO_2 + 2H^{+} + 2e^{-}$
この動画を見る
[2021 関西医科大学(改)]
$0.020mol/L$のシュウ酸水溶液$25mL$をコニカルビーカーにとり希硫酸を加えた。
この水溶液を温めた後に濃度がわからない過マンガン酸カリ ウム水溶液を加えていったところ、$20mL$加えたところで反応の終点をむかえた。
過マンガン酸カリウム水溶液のモル濃度は何$mol/L$か。
有効数字2桁で求めよ。
$MnO_4^{-} + 8H^{+} + 5e^{-} → Mn^{2+} + 4H_2O$
$H_2C_2O_4 → 2CO_2 + 2H^{+} + 2e^{-}$
【今年からの新しい単元!!】反応エンタルピーの種類(燃焼エンタルピー・生成エンタルピー・溶解エンタルピー・中和エンタルピー)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
新課程対応
反応エンタルピーについて解説します。
燃焼エンタルピー・生成エンタルピー・溶解エンタルピー・中和エンタルピー
この動画を見る
新課程対応
反応エンタルピーについて解説します。
燃焼エンタルピー・生成エンタルピー・溶解エンタルピー・中和エンタルピー
化学基礎の教科書を解説する動画 第60回 金属のイオン化傾向

【よく出る!?】よく出るマーク式のモル計算〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度
指導講師:
3rd School
問題文全文(内容文):
Q.次のうち含まれる酸素原子の物質量が最も小さいのは?
①0°C, 1.013×105Paの状態で体積が22.4Lの酸素
② 水が18gに含まれる酸素
③ 過酸化水素1.0molに含まれる酸素
④ 黒鉛12gの完全燃焼で発生する二酸化炭素に含まれる酸素
この動画を見る
Q.次のうち含まれる酸素原子の物質量が最も小さいのは?
①0°C, 1.013×105Paの状態で体積が22.4Lの酸素
② 水が18gに含まれる酸素
③ 過酸化水素1.0molに含まれる酸素
④ 黒鉛12gの完全燃焼で発生する二酸化炭素に含まれる酸素
1分で解いてほしい化学計算問題 (8) 濃度の変換

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 東京薬科大学 (改)〕
質量パーセント濃度が$18%$の水酸化ナトリウム水溶液(密度$1.2g/cm^3$)
のモル濃度$〔mol/L〕$を有効数字2桁で求めなさい。
原子量:$H 1 O 16 Na 23$
この動画を見る
〔2023 東京薬科大学 (改)〕
質量パーセント濃度が$18%$の水酸化ナトリウム水溶液(密度$1.2g/cm^3$)
のモル濃度$〔mol/L〕$を有効数字2桁で求めなさい。
原子量:$H 1 O 16 Na 23$
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第3問 問5 組成式の決定
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#化学変化と化学反応式#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
有機化合物A(ジメチルグリオキシム)は、ニッケル(Ⅱ)イオンに配位し、
エタノールに不溶な赤い化合物として沈殿する。
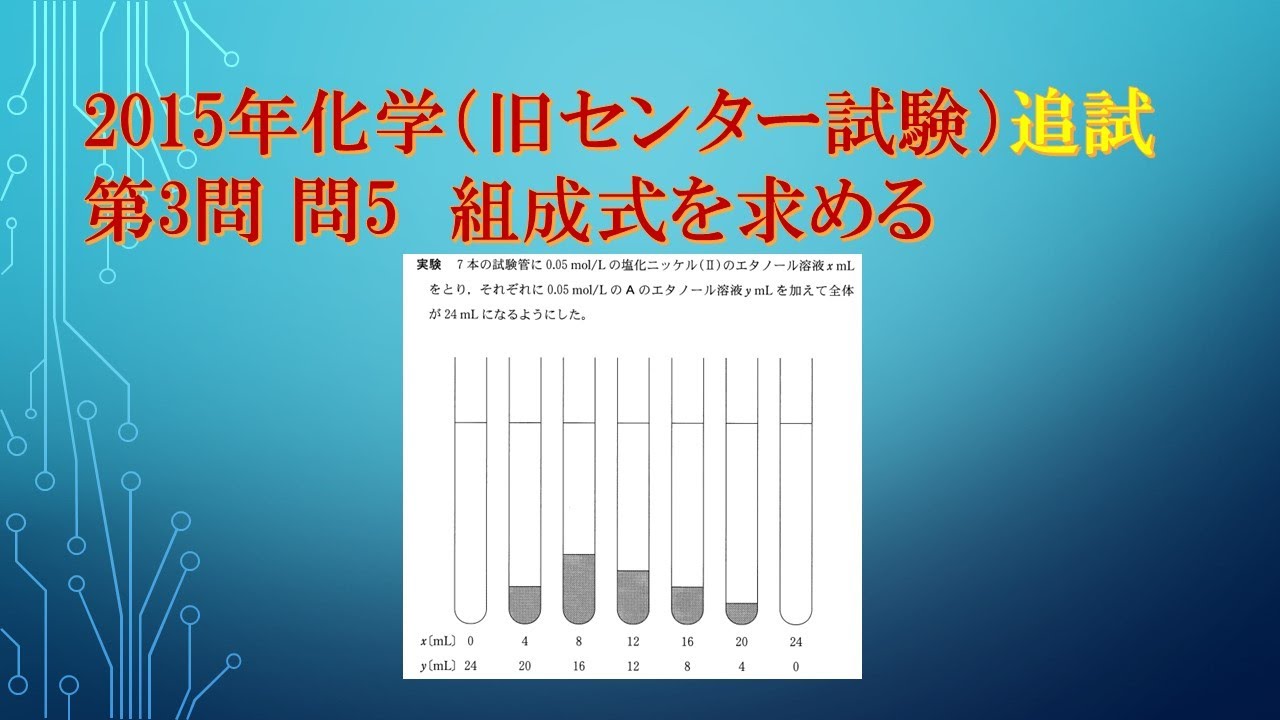
この化合物中のニッケル(Ⅱ)とAの物質量の比を決めるために次の実験を行ったところ、
生成した沈殿の量は図1のようになった。
ここで図中の灰色部分は沈殿を表している。
この化合物中のニッケル(Ⅱ)とAの物質量の比(ニッケル(Ⅱ):A)として
最も適当なものを、下の①~⑤のうちから一つ選べ。
実験 7本の試験管に$0.05mol/L$の塩化ニッケル(Ⅱ)のエタノール溶液$x mL$をとり、それぞれ$0.05mol/L$のAのエタノール溶液$y mL$を加えて全体が$24mL$になるようにした。
① $3:1$ ② $2:1$ ③ $1:1$ ④ $1:2$ ⑤ $1:3$
※図は動画内参照
この動画を見る
有機化合物A(ジメチルグリオキシム)は、ニッケル(Ⅱ)イオンに配位し、
エタノールに不溶な赤い化合物として沈殿する。
この化合物中のニッケル(Ⅱ)とAの物質量の比を決めるために次の実験を行ったところ、
生成した沈殿の量は図1のようになった。
ここで図中の灰色部分は沈殿を表している。
この化合物中のニッケル(Ⅱ)とAの物質量の比(ニッケル(Ⅱ):A)として
最も適当なものを、下の①~⑤のうちから一つ選べ。
実験 7本の試験管に$0.05mol/L$の塩化ニッケル(Ⅱ)のエタノール溶液$x mL$をとり、それぞれ$0.05mol/L$のAのエタノール溶液$y mL$を加えて全体が$24mL$になるようにした。
① $3:1$ ② $2:1$ ③ $1:1$ ④ $1:2$ ⑤ $1:3$
※図は動画内参照
化学基礎の教科書を解説する動画 第59回 COD滴定

【化学】比だけで物質量計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
molを使った計算方法の1つの解説です。
主に『公式が分からない』『公式が使えない』という方向けになっています。
炭素Cが2.4gあるときの物質量と原子の個数を求めよ
この動画を見る
molを使った計算方法の1つの解説です。
主に『公式が分からない』『公式が使えない』という方向けになっています。
炭素Cが2.4gあるときの物質量と原子の個数を求めよ
【公式要らずでマスター!?】モル計算(計算方法・平均分子量の求め方)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度
指導講師:
3rd School
問題文全文(内容文):
新課程対応
モル計算
計算方法・平均分子量
Q1 銅原子Cu$3.0 \times 10^{24}$個は何mol?
Q2 マグネシウム原子Mg(Mg:$24$)$7.2$gは何mol?
Q3 標準状態で$67.2$Lの塩化水素HClは何mol?
Q4 $0.30$molの水分子は何個?
Q5 水素(H:$1$)$5.0$は標準状態で何L?
Q6 標準状態で$11.2$Lの水素H$_2$に含まれている水素分子は何個?
Q7 塩化カルシウムCaCl$_21.11$gに含まれるCl$^-$のmol?
この動画を見る
新課程対応
モル計算
計算方法・平均分子量
Q1 銅原子Cu$3.0 \times 10^{24}$個は何mol?
Q2 マグネシウム原子Mg(Mg:$24$)$7.2$gは何mol?
Q3 標準状態で$67.2$Lの塩化水素HClは何mol?
Q4 $0.30$molの水分子は何個?
Q5 水素(H:$1$)$5.0$は標準状態で何L?
Q6 標準状態で$11.2$Lの水素H$_2$に含まれている水素分子は何個?
Q7 塩化カルシウムCaCl$_21.11$gに含まれるCl$^-$のmol?
【化学】物質量の定義が変わりました

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
物質量の定義が改訂されているのですが,あまり広く認識されていないためその動画です。
特に計算方法が大きくかかわるということはないものの,今後過去の資料と最新の資料で見比べるときのために活用を!
この動画を見る
物質量の定義が改訂されているのですが,あまり広く認識されていないためその動画です。
特に計算方法が大きくかかわるということはないものの,今後過去の資料と最新の資料で見比べるときのために活用を!
1分で解いてほしい化学計算問題 (5) 溶液の濃度計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023愛知学院大学(改)]
原子量 $\ce{H} 1 \ce{O} 16 \ce{S} 32 \ce{Cu} 64$
$30\,\rm{g}$の硫酸銅(II)五水和物$\ce{CuSO4}・5\ce{H2O}$を水に溶かし、$400\,\rm{mL}$とした。
この水溶液のモル濃度は何$\rm{mol/L}$ですか。
有効数字2桁で答えなさい。
この動画を見る
[2023愛知学院大学(改)]
原子量 $\ce{H} 1 \ce{O} 16 \ce{S} 32 \ce{Cu} 64$
$30\,\rm{g}$の硫酸銅(II)五水和物$\ce{CuSO4}・5\ce{H2O}$を水に溶かし、$400\,\rm{mL}$とした。
この水溶液のモル濃度は何$\rm{mol/L}$ですか。
有効数字2桁で答えなさい。
化学基礎の教科書を解説する動画 第58回 ヨウ素滴定

1分で解いてほしい化学計算問題 (4) 固体の溶解度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 大阪医科薬科大学(薬・改)〕
硝酸カリウムの水への溶解度〔$g/100g$水〕は、$60℃$のとき$110、40℃$のとき$64$である。
$60℃$の硝酸カリウム飽和水溶液$100g$を$40℃$に冷却したとき、何$g$の硝酸カリウムの結晶が析出するか、整数で答えなさい。
この動画を見る
〔2023 大阪医科薬科大学(薬・改)〕
硝酸カリウムの水への溶解度〔$g/100g$水〕は、$60℃$のとき$110、40℃$のとき$64$である。
$60℃$の硝酸カリウム飽和水溶液$100g$を$40℃$に冷却したとき、何$g$の硝酸カリウムの結晶が析出するか、整数で答えなさい。
1分で解いてほしい化学計算問題 (3) 原子量

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
〔2023 北里大学(理・改)〕
自然界の銅$Cu$には相対質量$62.93$の$^{63}Cu$と$64.93$の$^{65}Cu$が存在し、
$^{63}Cu$の天然存在比は( )%であるので、原子量は$63.55$である。
※空欄にあてはまる数値を整数で求めてください。
この動画を見る
〔2023 北里大学(理・改)〕
自然界の銅$Cu$には相対質量$62.93$の$^{63}Cu$と$64.93$の$^{65}Cu$が存在し、
$^{63}Cu$の天然存在比は( )%であるので、原子量は$63.55$である。
※空欄にあてはまる数値を整数で求めてください。
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第2問 問6 酸化還元反応の量的関係
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
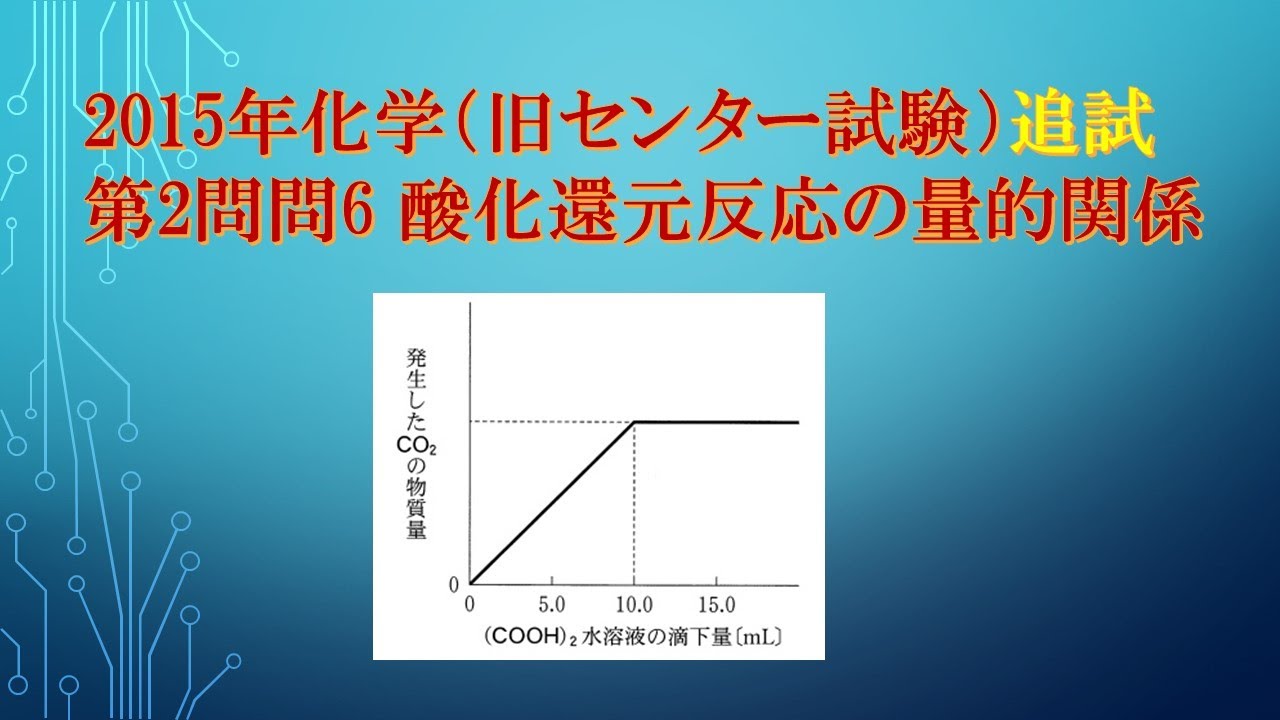
濃度不明の$K_2Cr_2O_7$の硫酸酸性水溶液$5.00mL$に$0.150mol/L$の$(COOH)_2$水溶液を加えていった。
このとき、発生した$CO_2$の物質量と$(COOH)_2$水溶液の滴下量の関係は図2のようになった。
この反応における$K_2Cr_2O_7$と$(COOH)_2$のはたらきは、電子を含む次のイオン反応式で表される。
$C3_2O_7^{-2} + 14H^{+} +6e^{-}→2Cr^{3+} + 7H_2O$
$(COOH)_2→2CO_2 + 2H^{+} + 2e^{-}$
$K_2Cr_2O_7$水溶液の濃度は何$mol/L$か。
最も適当な数値を、下の①~⑥のうちから一つ選べ。
①$0.0500$ ②$0.100$ ③$0.150$
④$0.200$ ⑤$0.300$⑥$0.900$
※表は動画内参照
この動画を見る
濃度不明の$K_2Cr_2O_7$の硫酸酸性水溶液$5.00mL$に$0.150mol/L$の$(COOH)_2$水溶液を加えていった。
このとき、発生した$CO_2$の物質量と$(COOH)_2$水溶液の滴下量の関係は図2のようになった。
この反応における$K_2Cr_2O_7$と$(COOH)_2$のはたらきは、電子を含む次のイオン反応式で表される。
$C3_2O_7^{-2} + 14H^{+} +6e^{-}→2Cr^{3+} + 7H_2O$
$(COOH)_2→2CO_2 + 2H^{+} + 2e^{-}$
$K_2Cr_2O_7$水溶液の濃度は何$mol/L$か。
最も適当な数値を、下の①~⑥のうちから一つ選べ。
①$0.0500$ ②$0.100$ ③$0.150$
④$0.200$ ⑤$0.300$⑥$0.900$
※表は動画内参照
化学基礎の教科書を解説する動画 第57回 酸化還元滴定

1分で解いてほしい化学計算問題 (1) 硫酸を薄める問題

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2022愛知学院大学]
質量パーセント濃度$98%$の濃硫酸$H_2SO_4$は、密度が$1.8g/cm^3$である。
濃硫酸を水でうすめて$2.0mol/L$の希硫酸を$25mL$つくりたい。
濃硫酸は何$mL$必要ですか。
有効数字2桁で答えなさい。
$H_2SO_4$の分子量98
この動画を見る
[2022愛知学院大学]
質量パーセント濃度$98%$の濃硫酸$H_2SO_4$は、密度が$1.8g/cm^3$である。
濃硫酸を水でうすめて$2.0mol/L$の希硫酸を$25mL$つくりたい。
濃硫酸は何$mL$必要ですか。
有効数字2桁で答えなさい。
$H_2SO_4$の分子量98
