 化学
化学
 化学
化学
【究極】令和版、炎色反応の語呂の覚え方はこれだ!〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#無機#イオンの反応と分離#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
今回は化学ではお馴染みの炎色反応の動画です!
学校の定期テストはもちろん受験(特に共通テスト)にもよく出るのですぐに覚えましょう!
そんな炎色反応の語呂を今回は独特な覚え方で紹介しています!
この動画を見る
今回は化学ではお馴染みの炎色反応の動画です!
学校の定期テストはもちろん受験(特に共通テスト)にもよく出るのですぐに覚えましょう!
そんな炎色反応の語呂を今回は独特な覚え方で紹介しています!
【この1本で沈殿と色覚えられます!】語呂と技を使って無機化学の沈殿とその色を覚えよう!※訂正概要欄を確認してください〔現役塾講師解説、高校化学、化学基礎〕

【2つの違いは何!?】組成式と分子式の違いをイメージで理解できる動画!〔現役塾講師解説、高校化学基礎、化学〕

歴史と科学をコラボする新シリーズ【社会人のための世界史class】文系目線で科学を学んでみたい!ゆきお先生が生徒になり、化学のカリスマ講師が文系頭のために授業をしてくれる企画のオープニング対談動

単元:
#化学#世界史#その他
指導講師:
世界史予備校講師佐藤幸夫 Yukio Sato チャンネル
問題文全文(内容文):
歴史と科学をコラボする新シリーズ文系目線で科学を学んでみたい!
ゆきお先生が生徒になり、「化学のカリスマ講師が文系頭のために授業をしてくれる企画」のオープニング対談動画です。
この動画を見る
歴史と科学をコラボする新シリーズ文系目線で科学を学んでみたい!
ゆきお先生が生徒になり、「化学のカリスマ講師が文系頭のために授業をしてくれる企画」のオープニング対談動画です。
【化学基礎の序盤の知識で入試問題が解ける!?】モル(mol)計算の演習をしよう!〔現役塾講師解説、高校化学、化学基礎〕〔日大理系2020化学第2問〕

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
Q1
$3.6\times10^{23}$個の水素原子を含むエタン$C_2H_6$の質量は?
Q2
質量%濃度5.00%の過酸化水素水$H_2O_2$水溶液(密度$1.02g/cm^3$)のモル濃度は?
Q3
$8.40g$の鉄をすべて酸化して得られる酸化鉄$(Ⅲ)$の質量は?
出典:2020年日本大学 入試問題
この動画を見る
Q1
$3.6\times10^{23}$個の水素原子を含むエタン$C_2H_6$の質量は?
Q2
質量%濃度5.00%の過酸化水素水$H_2O_2$水溶液(密度$1.02g/cm^3$)のモル濃度は?
Q3
$8.40g$の鉄をすべて酸化して得られる酸化鉄$(Ⅲ)$の質量は?
出典:2020年日本大学 入試問題
【第2日程共通テスト化学基礎解答解説】やや難化した第二日程の問題を現役塾講師による詳しい解説と講評 !短時間で解ける方法も解説しています!!

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
3rd School
問題文全文(内容文):
第2日程共通テスト化学基礎解答解説動画です
この動画を見る
第2日程共通テスト化学基礎解答解説動画です
【化学電池】ダニエル電池とボルタ電池の出るところを全て解説〔現役塾講師解説、高校化学、化学基礎〕

【高校化学】有機化学を合計6時間で解説する動画【後編】

単元:
#化学#有機#芳香族化合物#理科(高校生)
指導講師:
受験メモ山本
問題文全文(内容文):
有機化学の芳香族をまとめて解説!
ベンゼンの基礎、ベンゼンの反応、フェノールの反応、フェノールの製法、芳香族カルボン酸、 芳香族アミン、ジアゾ化・カップリング、アニリンの製法、芳香族化合物の分離
この動画を見る
有機化学の芳香族をまとめて解説!
ベンゼンの基礎、ベンゼンの反応、フェノールの反応、フェノールの製法、芳香族カルボン酸、 芳香族アミン、ジアゾ化・カップリング、アニリンの製法、芳香族化合物の分離
【苦手な人必見】化学結合と結晶の周辺論点がこれ一本で全部おさらいできます!(電気陰性度)〔現役塾講師解説、高校化学、化学基礎〕

【テンプレート化できるのです!】苦手な人必見!!モル(mol)計算の文章題(量的関係計算)を比を使わずにたった3分で解説する動画〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
プロパン$C_3H_8$の気体が完全燃焼すると、二酸化炭素と水が生じた。
二酸化炭素が264g発生した時、燃焼したプロパンは何Lか?
この動画を見る
プロパン$C_3H_8$の気体が完全燃焼すると、二酸化炭素と水が生じた。
二酸化炭素が264g発生した時、燃焼したプロパンは何Lか?
【化学基礎を救いたい】化学苦手な人へ。共通テストの化学、化学基礎をみて思ったこと

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
化学を理解するための学習について説明動画です
この動画を見る
化学を理解するための学習について説明動画です
【共通テスト化学基礎2021】質問が多かった第2問問2aを周辺知識を含め詳しく解説!〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#酸と塩基・水素イオン濃度#共通テスト#中和と塩#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
3rd School
問題文全文(内容文):
(a)の$CaCl_2$水溶液と$pH$と最も近い$pH$の値を持つ水溶液を、次の1~4のうちから一つ選べ。
ただし、混合する酸および塩基の水溶液はすべて、濃度が$0.100mol/L$,体積は$10.0ml$とする。
1.希硫酸と水酸化カリウム水溶液を混合した水溶液
2.塩酸と水酸化カリウム水溶液を混合した水溶液
3.塩酸とアンモニア水を混合した水溶液
4.塩酸と水酸化バリウム水溶液を混合した水溶液
この動画を見る
(a)の$CaCl_2$水溶液と$pH$と最も近い$pH$の値を持つ水溶液を、次の1~4のうちから一つ選べ。
ただし、混合する酸および塩基の水溶液はすべて、濃度が$0.100mol/L$,体積は$10.0ml$とする。
1.希硫酸と水酸化カリウム水溶液を混合した水溶液
2.塩酸と水酸化カリウム水溶液を混合した水溶液
3.塩酸とアンモニア水を混合した水溶液
4.塩酸と水酸化バリウム水溶液を混合した水溶液
【化学】無機化学:入試直前!これさえ覚えれば沈殿生成反応は満点②

単元:
#化学#無機#イオンの反応と分離#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
これさえ覚えれば沈殿生成反応は満点②
硫化物イオンによる沈澱、水酸化物による沈澱。
硫化物イオンの色は基本的に黒色、水酸化物イオンの沈澱は基本的に白色になります。それ以外の色は暗記。覚え方も動画内で解説。
この動画を見る
これさえ覚えれば沈殿生成反応は満点②
硫化物イオンによる沈澱、水酸化物による沈澱。
硫化物イオンの色は基本的に黒色、水酸化物イオンの沈澱は基本的に白色になります。それ以外の色は暗記。覚え方も動画内で解説。
【化学】無機化学:入試直前!これさえ覚えれば沈殿生成反応は満点①

単元:
#化学#無機#イオンの反応と分離#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
これさえ覚えれば沈殿生成反応は満点①
初めに銅イオン、鉄(II)イオン、鉄(Ⅲ)イオン、過マンガン酸イオンの色を覚えて、沈殿の規則を抑えよう。
塩化物イオンとの沈澱、硫酸イオンの沈澱、炭酸イオンの沈澱。色は全て白色!
この動画を見る
これさえ覚えれば沈殿生成反応は満点①
初めに銅イオン、鉄(II)イオン、鉄(Ⅲ)イオン、過マンガン酸イオンの色を覚えて、沈殿の規則を抑えよう。
塩化物イオンとの沈澱、硫酸イオンの沈澱、炭酸イオンの沈澱。色は全て白色!
共通テスト化学を解説・講評【2021共通テスト】

【最速!共通テスト化学基礎解答解説】現役塾講師による詳しい解説と講評 !10分で解いた解き方で解説しています!!

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#理科(高校生)#大学入試解答速報#化学#共通テスト
指導講師:
3rd School
問題文全文(内容文):
①
空気、メタン、オゾンの分類で正しいものを動画内の図より選びなさい
②
次のうち含まれる酸素原子の物質量が最も小さいのは?
③-a
動画内の図で正しい組み合わせは?
③-b
質量数が最も多い原子の質量数は?
M殻に電子がないもので原子番号が一番大きいのは?
④
動画内でただしい組み合わせは?
⑤
高温水蒸気と反応するのは?
1.$Al$
2.$Mg$
3.$Pt$
4.$Al,Mg$
5.$Al,Pt$
6.$Mg,Pt$
7.$Al,Mg,Pt$
⑥
酸化剤として働いているのは?
1.$CO → CO_2$
2.$NH_4Cl → NH_3$
3.$Na_2CO_3 → NaHCO_3$
4.Br_2 → Kbr
⑦
質量パーセント濃度$x(%)$,密度$d(g/cm^2)$の溶液が$100mL$である。
この溶液に含まれる溶質のモル質量が$M(g/mol)$であるとき、溶質の物質量を表す式として最も適当なものを、次の1~8から一つ選べ。
1.$\displaystyle \frac{xd}{M}$
2.$\displaystyle \frac{xd}{100M}$
3.$\displaystyle \frac{10xd}{M}$
4.$\displaystyle \frac{100xd}{M}$
5.$\displaystyle \frac{M}{xd}$
6.$\displaystyle \frac{100M}{xd}$
7.$\displaystyle \frac{M}{10xd}$
8.$\displaystyle \frac{M}{100xd}$
⑧
正極 $O_2+4H^+4e^-$ → $2H_2O$
負極 $H_2$ → $2H^++2e^-$
この燃料電池の放電で、$2.0mol$の電子が流れたときに生成する水の質量と、消費される水素の質量はそれぞれ何gか。
質量の数値の組み合わせとして最も適当なものを、動画内の選択肢のうちから一つ選べ。
ただし、流れた電子はすべて水の生成に使われるものとする
⑨
$NaCl$は正塩だが、正塩が出ないものは?
1.$CuSO_4$
2.$Na_2SO_4$
3.$NaHSO_4$
4.$NH_4Cl$
⑩
同じモル濃度、同じ体積の水溶液ア~エをそれぞれ、陽イオン交換樹脂に通し、陽イオンがすべて水素イオンに交換された水溶液を得た。
得られた水溶液中の水素イオンの物質量が最も大きいものはア~エのどれか。
最も適当なものを、次の1~4のうちから一つ選べ。
ア $KCI$水溶液
イ $NaOH$水溶液
ウ $MgCl_2水溶液
エ $CH_3COONa$水溶液
1.ア
2.イ
3.ウ
4.エ
⑪
(a)の$CaCl_2$水溶液と$pH$と最も近い$pH$の値を持つ水溶液を、次の1~4のうちから一つ選べ。
ただし、混合する酸および塩基の水溶液はすべて、濃度が$0.100mol/L$,体積は$10.0ml$とする。
1.希硫酸と水酸化カリウム水溶液を混合した水溶液
2.塩酸と水酸化カリウム水溶液を混合した水溶液
3.塩酸とアンモニア水を混合した水溶液
4.塩酸と水酸化バリウム水溶液を混合した水溶液
⑫
器具の正しい使い方は?
1.得られた塩酸をビーカーで$50.0mL$はかりとり、そこに水を加えて$500mL$にする
2.得られた塩酸をすべてメスフラスコに移し、水を加えて$500mL$にする
3.得られた塩酸をホールピペットで$50.0mL$とり、メスシリンダーにうつし、水を加えて$500mL$にする
4.得られた塩酸をすべてメスシリンダーに移し、水を加えて$500mL$にする
⑬
試料$A11.5g$に含まれる水の質量は?
この動画を見る
①
空気、メタン、オゾンの分類で正しいものを動画内の図より選びなさい
②
次のうち含まれる酸素原子の物質量が最も小さいのは?
③-a
動画内の図で正しい組み合わせは?
③-b
質量数が最も多い原子の質量数は?
M殻に電子がないもので原子番号が一番大きいのは?
④
動画内でただしい組み合わせは?
⑤
高温水蒸気と反応するのは?
1.$Al$
2.$Mg$
3.$Pt$
4.$Al,Mg$
5.$Al,Pt$
6.$Mg,Pt$
7.$Al,Mg,Pt$
⑥
酸化剤として働いているのは?
1.$CO → CO_2$
2.$NH_4Cl → NH_3$
3.$Na_2CO_3 → NaHCO_3$
4.Br_2 → Kbr
⑦
質量パーセント濃度$x(%)$,密度$d(g/cm^2)$の溶液が$100mL$である。
この溶液に含まれる溶質のモル質量が$M(g/mol)$であるとき、溶質の物質量を表す式として最も適当なものを、次の1~8から一つ選べ。
1.$\displaystyle \frac{xd}{M}$
2.$\displaystyle \frac{xd}{100M}$
3.$\displaystyle \frac{10xd}{M}$
4.$\displaystyle \frac{100xd}{M}$
5.$\displaystyle \frac{M}{xd}$
6.$\displaystyle \frac{100M}{xd}$
7.$\displaystyle \frac{M}{10xd}$
8.$\displaystyle \frac{M}{100xd}$
⑧
正極 $O_2+4H^+4e^-$ → $2H_2O$
負極 $H_2$ → $2H^++2e^-$
この燃料電池の放電で、$2.0mol$の電子が流れたときに生成する水の質量と、消費される水素の質量はそれぞれ何gか。
質量の数値の組み合わせとして最も適当なものを、動画内の選択肢のうちから一つ選べ。
ただし、流れた電子はすべて水の生成に使われるものとする
⑨
$NaCl$は正塩だが、正塩が出ないものは?
1.$CuSO_4$
2.$Na_2SO_4$
3.$NaHSO_4$
4.$NH_4Cl$
⑩
同じモル濃度、同じ体積の水溶液ア~エをそれぞれ、陽イオン交換樹脂に通し、陽イオンがすべて水素イオンに交換された水溶液を得た。
得られた水溶液中の水素イオンの物質量が最も大きいものはア~エのどれか。
最も適当なものを、次の1~4のうちから一つ選べ。
ア $KCI$水溶液
イ $NaOH$水溶液
ウ $MgCl_2水溶液
エ $CH_3COONa$水溶液
1.ア
2.イ
3.ウ
4.エ
⑪
(a)の$CaCl_2$水溶液と$pH$と最も近い$pH$の値を持つ水溶液を、次の1~4のうちから一つ選べ。
ただし、混合する酸および塩基の水溶液はすべて、濃度が$0.100mol/L$,体積は$10.0ml$とする。
1.希硫酸と水酸化カリウム水溶液を混合した水溶液
2.塩酸と水酸化カリウム水溶液を混合した水溶液
3.塩酸とアンモニア水を混合した水溶液
4.塩酸と水酸化バリウム水溶液を混合した水溶液
⑫
器具の正しい使い方は?
1.得られた塩酸をビーカーで$50.0mL$はかりとり、そこに水を加えて$500mL$にする
2.得られた塩酸をすべてメスフラスコに移し、水を加えて$500mL$にする
3.得られた塩酸をホールピペットで$50.0mL$とり、メスシリンダーにうつし、水を加えて$500mL$にする
4.得られた塩酸をすべてメスシリンダーに移し、水を加えて$500mL$にする
⑬
試料$A11.5g$に含まれる水の質量は?
【史上最速3分でわかるの?わかります!】モル(mol)計算がたった3分で解けるようになる動画 〔現役塾講師解説、高校化学・化学基礎〕

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
①銅原子$Cu$ $3.0\times10^{24}$個は何$mol$?
②水素$(H:1)5.0g$は標準状態で何$L$?
この動画を見る
①銅原子$Cu$ $3.0\times10^{24}$個は何$mol$?
②水素$(H:1)5.0g$は標準状態で何$L$?
【一撃必殺!】受験生が苦手なモル濃度、質量パーセント濃度の換算の計算方法をたった2分で解説します!〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
ブドウ糖(グルコース、分子量180)の質量パーセント濃度$5.0$%水溶液は点滴に用いられている。
この水溶液のモル濃度は何$mol/L$か。
ただし、この水溶液の密度は$1.0g/cm^3$とする。
この動画を見る
ブドウ糖(グルコース、分子量180)の質量パーセント濃度$5.0$%水溶液は点滴に用いられている。
この水溶液のモル濃度は何$mol/L$か。
ただし、この水溶液の密度は$1.0g/cm^3$とする。
【強酸、強塩基しか勝たん】現役塾講師解説!暗記最小限!?酸・塩基の基礎を秒で学べる動画 (酸・塩基基礎マスター①)

【高校化学】有機化学を合計6時間で解説する動画【前編】

単元:
#化学#有機#有機化合物の特徴と構造#脂肪族炭化水素#酸素を含む脂肪族化合物#理科(高校生)
指導講師:
受験メモ山本
問題文全文(内容文):
有機化学をまとめて解説します。
有機物の基本から官能基、結合まで
アルカン 、シクロアルカン、アルケン、アルキン 、アルコール、エーテル、アルデヒド、ケトン、カルボン酸 、エステル
この動画を見る
有機化学をまとめて解説します。
有機物の基本から官能基、結合まで
アルカン 、シクロアルカン、アルケン、アルキン 、アルコール、エーテル、アルデヒド、ケトン、カルボン酸 、エステル
【共通テスト対策化学おまけ】自作問題作ったから暇な人は解いて。

【共通テスト対策化学】2018年度試行調査第5問解説【実践編⑤】

【共通テスト対策化学】2018年度試行調査第4問解説【実践編④】

〔現役塾講師解説〕金を溶かす王水とは一体...テスト直前でも間に合う!短時間でイオン化傾向を学ぶ 酸化還元基礎マスター③ 高校化学基礎

【共通テスト対策化学】2018年度試行調査第3問解説【実践編③】

【共通テスト対策化学】2018年度試行調査第2問解説【実践編②】

〔現役塾講師解説〕テスト直前でも間に合う!短時間で学べる酸化還元反応② 反応式編 高校化学基礎 〔理論化学〕

【共通テスト対策化学】2018年度試行調査第1問解説【実践編①】

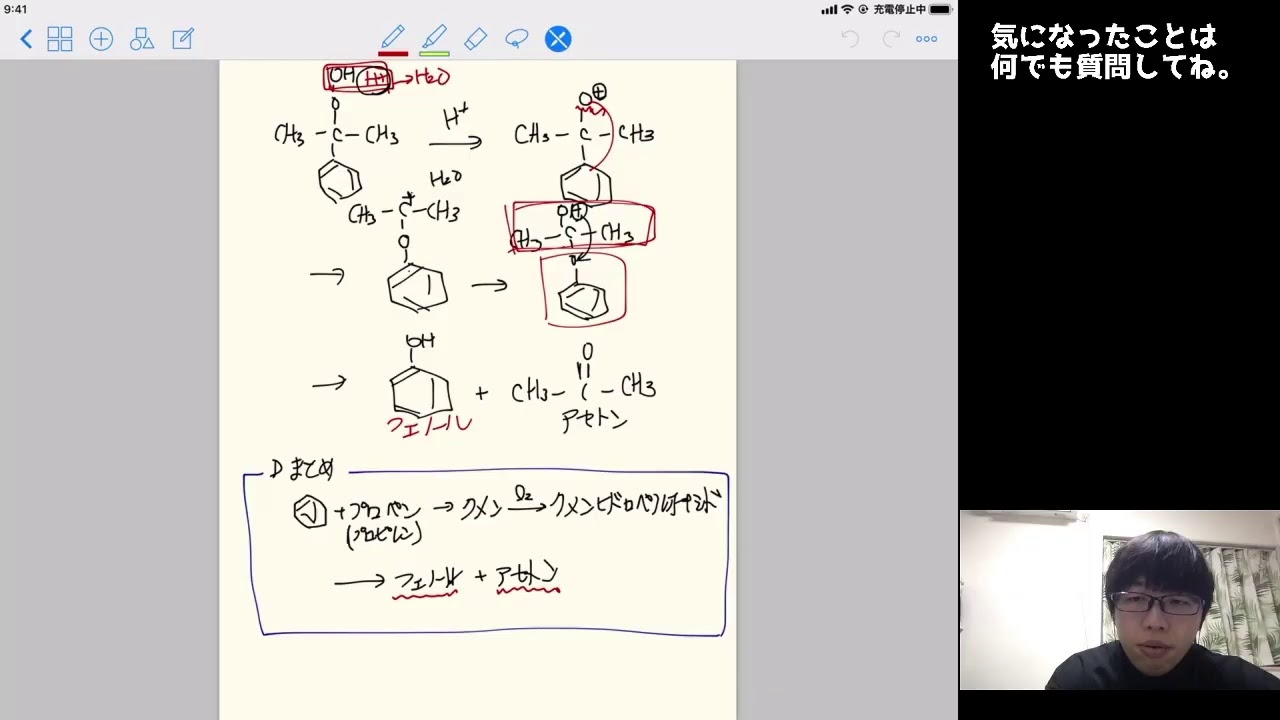
【Live】第2回有機化学基礎講座【※授業進度が遅い人向け】
単元:
#化学#有機#有機化合物の特徴と構造#脂肪族炭化水素#酸素を含む脂肪族化合物#芳香族化合物#有機化合物と人間生活#理科(高校生)
指導講師:
受験メモ山本
問題文全文(内容文):
有機化学基礎講座動画です
この動画を見る
有機化学基礎講座動画です
〔現役塾講師解説〕テスト直前でも間に合う!短時間で学べる酸化還元反応① 酸化数編 高校化学基礎 〔理論化学〕

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
①$NH_3$の$N$の酸化数は?
②$KM_nO_4$の$M_n$の酸化数は?
③$SO_4^{2-}$の$S$の酸化数は?
④$NH_4NO_3$の$N$の酸化数は?
この動画を見る
①$NH_3$の$N$の酸化数は?
②$KM_nO_4$の$M_n$の酸化数は?
③$SO_4^{2-}$の$S$の酸化数は?
④$NH_4NO_3$の$N$の酸化数は?
