 物質量と濃度
物質量と濃度
 物質量と濃度
物質量と濃度
【高校化学】モル質量 M[g/mol] の物質Xをw[g] はかり取り、有機溶媒に溶かして体積を V[mL]にした。この溶液 v[mL] を静かに水面に滴下し、溶媒を蒸発させたところ棒状の分子が水面に

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
モル質量 M[g/mol] の物質Xをw[g] はかり取り、有機溶媒に溶かして体積を V[mL]にした。 この溶液 v[mL] を静かに水面に滴下し、溶媒を蒸発させたところ棒状の分子が水面にすき間なく並び、 1層の膜でできた単分子膜を形成した。 この膜の全体の面積を測定したところ、S[cm²] であった。 次の各問いに文字式で答えよ。 (1) 単分子膜を形成した物質Xの物質量は何molか。 (2)1分子の物質Xの断面積がS₁[cm²]であるとき、単分子膜中の分数は何個か。 (3)この実験から求められるアボガドロ定数 N [/mol] はいくらか。 (4) 単分子膜の密度をd[g/cm³] とすると、物質Xの分子の長さ(単分子膜の厚み)は何cmか
この動画を見る
モル質量 M[g/mol] の物質Xをw[g] はかり取り、有機溶媒に溶かして体積を V[mL]にした。 この溶液 v[mL] を静かに水面に滴下し、溶媒を蒸発させたところ棒状の分子が水面にすき間なく並び、 1層の膜でできた単分子膜を形成した。 この膜の全体の面積を測定したところ、S[cm²] であった。 次の各問いに文字式で答えよ。 (1) 単分子膜を形成した物質Xの物質量は何molか。 (2)1分子の物質Xの断面積がS₁[cm²]であるとき、単分子膜中の分数は何個か。 (3)この実験から求められるアボガドロ定数 N [/mol] はいくらか。 (4) 単分子膜の密度をd[g/cm³] とすると、物質Xの分子の長さ(単分子膜の厚み)は何cmか
【高校化学】(1)質量数12のC原子1個の質量は何gか。 有効数字2桁で求めよ。(2) 水素の同位体¹H、²H、 ³H の、 炭素12(¹²C) を基準としたときの相対質量はそれぞれ1.00785、

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
(1)質量数12のC原子1個の質量は何gか。 有効数字2桁で求めよ。
(2) 水素の同位体¹H、²H、 ³H の、 炭素12(¹²C) を基準としたときの
相対質量はそれぞれ1.00785、 2014102、 3.010440である。
このうち³Hは放射性同位体で、自然界にはこの3種の水素の同位体が
それぞれ99.9885%、 0.0115%、 および極微量存在する。
水素の原子量を小数点以下3桁まで求めよ。
(3)自然界に存在する水素分子には、質量の異なるものが
何種類存在すると考えられるか。
(4) 質量の異なる水素分子の中で、最も多く存在する分子と、
2番目に多く存在する分
子の数の比を有効数字2桁で求めよ。
この動画を見る
(1)質量数12のC原子1個の質量は何gか。 有効数字2桁で求めよ。
(2) 水素の同位体¹H、²H、 ³H の、 炭素12(¹²C) を基準としたときの
相対質量はそれぞれ1.00785、 2014102、 3.010440である。
このうち³Hは放射性同位体で、自然界にはこの3種の水素の同位体が
それぞれ99.9885%、 0.0115%、 および極微量存在する。
水素の原子量を小数点以下3桁まで求めよ。
(3)自然界に存在する水素分子には、質量の異なるものが
何種類存在すると考えられるか。
(4) 質量の異なる水素分子の中で、最も多く存在する分子と、
2番目に多く存在する分
子の数の比を有効数字2桁で求めよ。
【高校化学】(1)天然の銅は、質量数63と65の同位体が、ある一定の比率で混じり合っている。銅の原子量を63.5として、各同位体の天然存在比 [%] を有効数字2桁で求めよ。

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
各原子の相対質量は、その質量数に等しいものとして、次の各問いに答えよ。
(1)天然の銅は、質量数63と65の同位体が、ある一定の比率で混じり合っている。銅の
原子量を63.5として、各同位体の天然存在比 [%] を有効数字2桁で求めよ。
(2)天然の同位体比の原子で構成された、硝酸銀 AgNO 水溶液と臭化ナトリウム
NaBr 水溶液がある。 これらを混合し、 臭化銀AgBr を沈殿させた。 沈殿した臭化銀
の「質量」 分布を示せ。
BrとAgの各同位体の天然存在中「質量」存在比[%]はそれぞれ
Brは質量数79質量数:81=(存在比)50:50 、Agは質量数107:質量数109=50:50 とする
また、イオン結晶の「質量」 とは、その組成式を構成する各原子の相対質量の和とする。
この動画を見る
各原子の相対質量は、その質量数に等しいものとして、次の各問いに答えよ。
(1)天然の銅は、質量数63と65の同位体が、ある一定の比率で混じり合っている。銅の
原子量を63.5として、各同位体の天然存在比 [%] を有効数字2桁で求めよ。
(2)天然の同位体比の原子で構成された、硝酸銀 AgNO 水溶液と臭化ナトリウム
NaBr 水溶液がある。 これらを混合し、 臭化銀AgBr を沈殿させた。 沈殿した臭化銀
の「質量」 分布を示せ。
BrとAgの各同位体の天然存在中「質量」存在比[%]はそれぞれ
Brは質量数79質量数:81=(存在比)50:50 、Agは質量数107:質量数109=50:50 とする
また、イオン結晶の「質量」 とは、その組成式を構成する各原子の相対質量の和とする。
【高校化学】(1)50gの水に 50gの物質Aを加えて加熱した。 Aが完全に溶解する温度は何℃か。(2)10gのBを含む水溶液50gがある。この水溶液を冷却したとき、 何℃で結晶が析出するか。

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
図(図は動画中)は物質 A、B、Cの溶解度曲線である。
次の各問いに答えよ。
(1)50gの水に 50gの物質Aを加えて加熱した。
Aが完全に溶解する温度は何℃か。
(2)10gのBを含む水溶液50gがある。この水溶液
を冷却したとき、 何℃で結晶が析出するか。
(3)物質A、B、Cのうち、 再結晶で物質を精製する
場合、この方法が適さないのはどれか。
この動画を見る
図(図は動画中)は物質 A、B、Cの溶解度曲線である。
次の各問いに答えよ。
(1)50gの水に 50gの物質Aを加えて加熱した。
Aが完全に溶解する温度は何℃か。
(2)10gのBを含む水溶液50gがある。この水溶液
を冷却したとき、 何℃で結晶が析出するか。
(3)物質A、B、Cのうち、 再結晶で物質を精製する
場合、この方法が適さないのはどれか。
【高校化学】(1)50gの水に 50gの物質Aを加えて加熱した。 Aが完全に溶解する温度は何℃か。(2)10gのBを含む水溶液50gがある。この水溶液を冷却したとき、 何℃で結晶が析出するか

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
図(図は動画中)は物質 A、B、Cの溶解度曲線である。
次の各問いに答えよ。
(1)50gの水に 50gの物質Aを加えて加熱した。
Aが完全に溶解する温度は何℃か。
(2)10gのBを含む水溶液50gがある。この水溶液
を冷却したとき、 何℃で結晶が析出するか。
(3)物質A、B、Cのうち、 再結晶で物質を精製する
場合、この方法が適さないのはどれか。
この動画を見る
図(図は動画中)は物質 A、B、Cの溶解度曲線である。
次の各問いに答えよ。
(1)50gの水に 50gの物質Aを加えて加熱した。
Aが完全に溶解する温度は何℃か。
(2)10gのBを含む水溶液50gがある。この水溶液
を冷却したとき、 何℃で結晶が析出するか。
(3)物質A、B、Cのうち、 再結晶で物質を精製する
場合、この方法が適さないのはどれか。
【高校化学】アボガドロ定数をN[/mol]、0℃、 1.013×10 Pa における気体のモル体積をVm[L/mol]として、次の各問いに答えよ。(1)密度dlg/cm³の、ある金属a[cm³]中には

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
アボガドロ定数をN[/mol]、0℃、 1.013×10 Pa における
気体のモル体積をVm[L/mol]として、次の各問いに答えよ。
(1)密度dlg/cm³の、ある金属a[cm³]中にはn個の原子が含まれていた。
この金属のモル質量を求めよ。
(2)モル質量 M[g/mol] の気体の質量がw [g] であるとき、
この気体の0℃、1.013 × 105 Pa における体積は何Lか。
また、この気体の分子数は何個か。
(3)モル質量 M[g/mol] の物質 w [g] を水に溶解させて体積をV[L]とした。
この水溶液のモル濃度 [mol/L] はいくらか。
この動画を見る
アボガドロ定数をN[/mol]、0℃、 1.013×10 Pa における
気体のモル体積をVm[L/mol]として、次の各問いに答えよ。
(1)密度dlg/cm³の、ある金属a[cm³]中にはn個の原子が含まれていた。
この金属のモル質量を求めよ。
(2)モル質量 M[g/mol] の気体の質量がw [g] であるとき、
この気体の0℃、1.013 × 105 Pa における体積は何Lか。
また、この気体の分子数は何個か。
(3)モル質量 M[g/mol] の物質 w [g] を水に溶解させて体積をV[L]とした。
この水溶液のモル濃度 [mol/L] はいくらか。
【高校化学】実験動物(マウス、体重 30 g)に、ある薬剤(分子量 270)を静脈から血液中に投与し、血液中での薬剤濃度を 1.0×10⁻⁴ mol/L にしたい。このマウスの血液量が体重の 7.0%

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
溶液の濃度
実験動物(マウス、体重 30 g)に、ある薬剤(分子量 270)を静脈から血液中に投与し、血液中での薬剤濃度を 1.0×10⁻⁴ mol/L にしたい。このマウスの血液量が体重の 7.0%とすると、この薬剤を何 mg 投与すればよいか。ただし、この薬剤は投与後に全身に均等に分布し、血液の密度は 1.0 g/mL であるものとする。また、薬剤投与による血液の体積変化は無視できるものとする。
この動画を見る
溶液の濃度
実験動物(マウス、体重 30 g)に、ある薬剤(分子量 270)を静脈から血液中に投与し、血液中での薬剤濃度を 1.0×10⁻⁴ mol/L にしたい。このマウスの血液量が体重の 7.0%とすると、この薬剤を何 mg 投与すればよいか。ただし、この薬剤は投与後に全身に均等に分布し、血液の密度は 1.0 g/mL であるものとする。また、薬剤投与による血液の体積変化は無視できるものとする。
【高校化学】濃硫酸は、質量パーセント濃度が 98.0%で、密度が 1.84 g/cm³ である。H₂SO₄ の分子量を 98.0 として、次の各問いに答えよ。(1)濃硫酸のモル濃度は何 mol/L か

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
溶液の希釈
濃硫酸は、質量パーセント濃度が 98.0%で、密度が 1.84 g/cm³ である。H₂SO₄ の分子量を 98.0 として、次の各問いに答えよ。
(1)濃硫酸のモル濃度は何 mol/L か。
(2)濃硫酸を水で希釈して 3.00 mol/L の希硫酸(密度 1.18 g/cm³)を 300 mL つくりたい。必要な濃硫酸の体積は何 mL か。また、加える水の質量は何 g か。
この動画を見る
溶液の希釈
濃硫酸は、質量パーセント濃度が 98.0%で、密度が 1.84 g/cm³ である。H₂SO₄ の分子量を 98.0 として、次の各問いに答えよ。
(1)濃硫酸のモル濃度は何 mol/L か。
(2)濃硫酸を水で希釈して 3.00 mol/L の希硫酸(密度 1.18 g/cm³)を 300 mL つくりたい。必要な濃硫酸の体積は何 mL か。また、加える水の質量は何 g か。
【高校化学】硫酸銅(Ⅱ)水溶液を調製する方法として正しいものを、次の①〜④から1つ選べ。ただし、CuSO₄の式量は160、水の密度は1.0 g/cm³とする。① 2.5%の水溶液をつくるため、硫酸銅

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
溶液の調製 硫酸銅(Ⅱ)水溶液を調製する方法として正しいものを、次の①〜④から1つ選べ。ただし、CuSO₄の式量は160、水の密度は1.0 g/cm³とする。 ① 2.5%の水溶液をつくるため、硫酸銅(Ⅱ)五水和物 2.5 g を水 97.5 g に溶かした。 ② 2.0%の水溶液をつくるため、5.0%の硫酸銅(Ⅱ)水溶液 8.0 g に 20 mL の水を加えた。 ③ 0.20 mol/L の水溶液をつくるため、硫酸銅(Ⅱ)五水和物 16 g を水に溶かして 500 mL とした。 ④ 5.0×10⁻³ mol/L の水溶液をつくるため、2.0×10⁻² mol/L の硫酸銅(Ⅱ)水溶液 25 mL に水を加えて 100 mL とした。
この動画を見る
溶液の調製 硫酸銅(Ⅱ)水溶液を調製する方法として正しいものを、次の①〜④から1つ選べ。ただし、CuSO₄の式量は160、水の密度は1.0 g/cm³とする。 ① 2.5%の水溶液をつくるため、硫酸銅(Ⅱ)五水和物 2.5 g を水 97.5 g に溶かした。 ② 2.0%の水溶液をつくるため、5.0%の硫酸銅(Ⅱ)水溶液 8.0 g に 20 mL の水を加えた。 ③ 0.20 mol/L の水溶液をつくるため、硫酸銅(Ⅱ)五水和物 16 g を水に溶かして 500 mL とした。 ④ 5.0×10⁻³ mol/L の水溶液をつくるため、2.0×10⁻² mol/L の硫酸銅(Ⅱ)水溶液 25 mL に水を加えて 100 mL とした。
【高校化学】次の文章を読み,下の各問いに答えよ。1894年,レイリーとラムゼーは,空気から酸素などを取り除いて得た窒素の密度が,純粋な窒素の密度よりも,0℃,1.013×10⁵ Pa において

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
気体の密度とモル質量
次の文章を読み,下の各問いに答えよ。 1894年,レイリーとラムゼーは,空気から酸素などを取り除いて得た窒素の密度が,純粋な窒素の密度よりも,0℃,1.013×10⁵ Pa において 0.500%大きいことから,窒素よりも密度の大きい気体が空気に含まれると考え,アルゴン Ar を発見した。ここで,空気から酸素などを取り除いて得た窒素には,窒素とアルゴンが含まれるものとする。 (1)空気から酸素などを取り除いて得た窒素中のアルゴンの物質量の割合を x,窒素の物質量の割合を 1−x とするとき,x はいくらか。有効数字2桁で求めよ。 (2)空気中の窒素の物質量の割合を 79%とすると,空気中のアルゴンの物質量の割合は何%か。有効数字2桁で求めよ。
この動画を見る
気体の密度とモル質量
次の文章を読み,下の各問いに答えよ。 1894年,レイリーとラムゼーは,空気から酸素などを取り除いて得た窒素の密度が,純粋な窒素の密度よりも,0℃,1.013×10⁵ Pa において 0.500%大きいことから,窒素よりも密度の大きい気体が空気に含まれると考え,アルゴン Ar を発見した。ここで,空気から酸素などを取り除いて得た窒素には,窒素とアルゴンが含まれるものとする。 (1)空気から酸素などを取り除いて得た窒素中のアルゴンの物質量の割合を x,窒素の物質量の割合を 1−x とするとき,x はいくらか。有効数字2桁で求めよ。 (2)空気中の窒素の物質量の割合を 79%とすると,空気中のアルゴンの物質量の割合は何%か。有効数字2桁で求めよ。
【高校化学】次の各問いに答えよ。(1)ある元素Yの単体A[g]を空気中で強く熱したところ,すべて反応して酸化物YOがB[g]生成した。Oのモル質量を MOM_OMO[g/mol]として

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
金属の原子量
次の各問いに答えよ。 (1)ある元素Yの単体A[g]を空気中で強く熱したところ,すべて反応して酸化物YOがB[g]生成した。Oのモル質量を MOM_OMO[g/mol]として,この元素Yのモル質量[g/mol]をA,B,MOM_OMO を用いて表せ。 (2)ある金属Xの塩化物は組成式 XCl2・2H2OXCl_2・2H_2OXCl2・2H2O の水和物をつくる。この水和物882 mgを加熱して無水物にしたところ,666 mgになった。この金属Xの原子量を求めよ。
この動画を見る
金属の原子量
次の各問いに答えよ。 (1)ある元素Yの単体A[g]を空気中で強く熱したところ,すべて反応して酸化物YOがB[g]生成した。Oのモル質量を MOM_OMO[g/mol]として,この元素Yのモル質量[g/mol]をA,B,MOM_OMO を用いて表せ。 (2)ある金属Xの塩化物は組成式 XCl2・2H2OXCl_2・2H_2OXCl2・2H2O の水和物をつくる。この水和物882 mgを加熱して無水物にしたところ,666 mgになった。この金属Xの原子量を求めよ。
【高校化学】(1) 質量パーセントを求めよ(ア)SO₂ 【S】(イ) C₆H₁₂O₆ 【C】(2)ある金属元素Mの酸化物MO₂17.4gを還元するとMの単体が11.0g得られた金属元素の原子量を求めよ

【高校化学】(1) 3.0molの水は何gか(2) 3.2gのメタノールは何molか。そこに含まれる水素原子は何molか(3) 3.4gのアンモニアは何molか。そこに含まれる水素原子は何molか

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
理数個別チャンネル
問題文全文(内容文):
次の問いに答えよ
(1) 3.0molの水は何gか
(2) 3.2gのメタノールは何molか。そこに含まれる水素原子は何molか
(3) 3.4gのアンモニアは何molか。そこに含まれる水素原子は何molか
(4) 0.50molの硝酸マグネシウムに含まれる硝酸イオンは何molか。
そこに含まれる酸素原子は何か。
この動画を見る
次の問いに答えよ
(1) 3.0molの水は何gか
(2) 3.2gのメタノールは何molか。そこに含まれる水素原子は何molか
(3) 3.4gのアンモニアは何molか。そこに含まれる水素原子は何molか
(4) 0.50molの硝酸マグネシウムに含まれる硝酸イオンは何molか。
そこに含まれる酸素原子は何か。
【高校化学】ネオン0.5molの重さ、圧力、体積を求めよ。カルシウム1.2×10²³PAのmol、重さ、体積を求めよ。二酸化炭素6.6gのmol、圧力、体積を求めよ。

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
ネオン0.5molの重さ、圧力、体積を求めよ
カルシウム1.2×10²³PAのmol、重さ、体積を求めよ
二酸化炭素6.6gのmol、圧力、体積を求めよ
この動画を見る
ネオン0.5molの重さ、圧力、体積を求めよ
カルシウム1.2×10²³PAのmol、重さ、体積を求めよ
二酸化炭素6.6gのmol、圧力、体積を求めよ
【高校化学】(1) - (6)の分子量、式量を求めよ(1)窒素(2)塩化水素(3)硫化水素(4) 硫酸イオン (5) 炭酸水素イオン(6)硫酸銅(II)·五水和物

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
(1) - (6)の分子量、式量を求めよ
(1)窒素
(2)塩化水素
(3)硫化水素
(4) 硫酸イオン (5) 炭酸水素イオン
(6)硫酸銅(II)·五水和物
この動画を見る
(1) - (6)の分子量、式量を求めよ
(1)窒素
(2)塩化水素
(3)硫化水素
(4) 硫酸イオン (5) 炭酸水素イオン
(6)硫酸銅(II)·五水和物
【高校化学】(1)銅には質量数63の銅69.2%と質量数65の銅が30.8% がある。銅の原子量を求めよ(2)銀には質量数107の銀と質量数109の銀が存在する。 原子量107.9であるとき、銀が何個

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
次の問いに答えよ。質量数=相対質量とする。
(1)銅には質量数63の銅69.2%と質量数65の銅が30.8% がある。銅の原子量を求めよ
(2)銀には質量数107の銀と質量数109の銀が存在する。 原子量107.9であるとき、銀原子1000個中には銀質量数107の銀が何個あるか
この動画を見る
次の問いに答えよ。質量数=相対質量とする。
(1)銅には質量数63の銅69.2%と質量数65の銅が30.8% がある。銅の原子量を求めよ
(2)銀には質量数107の銀と質量数109の銀が存在する。 原子量107.9であるとき、銀原子1000個中には銀質量数107の銀が何個あるか
【高校化学】●次の文中の( )に適当な文字式,数値を記せ。H₂SO₄=98.0 とする。10% 硫酸水溶液を水でうすめて 0.50 mol/L の水溶液を 100 mL つくりたい。10% 硫酸水溶

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
次の文中の( )に適当な文字式,数値を記せ。H₂SO₄=98.0 とする。
10% 硫酸水溶液を水でうすめて 0.50 mol/L の水溶液を 100 mL つくりたい。10% 硫酸水溶液を x [g] 用いるとすると,この中に溶けている溶質 H₂SO₄ の質量は,10% なので(ア)と表される。
また,0.50 mol/L 硫酸水溶液 100 mL 中の溶質 H₂SO₄ の質量は(イ)g である。うすめても溶質の量は変化しないので,式(ウ)が成り立ち必要な 10% 硫酸水溶液の質量は(エ)g と求められる。
この動画を見る
次の文中の( )に適当な文字式,数値を記せ。H₂SO₄=98.0 とする。
10% 硫酸水溶液を水でうすめて 0.50 mol/L の水溶液を 100 mL つくりたい。10% 硫酸水溶液を x [g] 用いるとすると,この中に溶けている溶質 H₂SO₄ の質量は,10% なので(ア)と表される。
また,0.50 mol/L 硫酸水溶液 100 mL 中の溶質 H₂SO₄ の質量は(イ)g である。うすめても溶質の量は変化しないので,式(ウ)が成り立ち必要な 10% 硫酸水溶液の質量は(エ)g と求められる。
【高校化学】●次の各問いに答えよ。ただし,H₂SO₄=98.0 とする。(1) 98.0% 硫酸水溶液(密度 1.84 g/cm³)のモル濃度は何 mol/L か。(2) 0.200 mol/L 硫酸

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
●次の各問いに答えよ。ただし,H₂SO₄=98.0 とする。
(1) 98.0% 硫酸水溶液(密度 1.84 g/cm³)のモル濃度は何 mol/L か。
(2) 0.200 mol/L 硫酸水溶液(密度 1.05 g/cm³)の質量パーセント濃度は何 % か。
この動画を見る
●次の各問いに答えよ。ただし,H₂SO₄=98.0 とする。
(1) 98.0% 硫酸水溶液(密度 1.84 g/cm³)のモル濃度は何 mol/L か。
(2) 0.200 mol/L 硫酸水溶液(密度 1.05 g/cm³)の質量パーセント濃度は何 % か。
【高校化学】●次の各問いに答えよ。(1) 9.0 g のグルコース C₆H₁₂O₆ を水に溶かして 200 mL にした水溶液は何 mol/L か。(2) 0.25 mol/L の水酸化ナトリウム

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
●次の各問いに答えよ。
(1) 9.0 g のグルコース C₆H₁₂O₆ を水に溶かして 200 mL にした水溶液は何 mol/L か。
(2) 0.25 mol/L の水酸化ナトリウム NaOH 水溶液 200 mL 中に、NaOH は何 mol 含まれるか。また、含まれる NaOH の質量は何 g か。
(3) 12 mol/L の塩酸(塩化水素 HCl の水溶液)を水でうすめて 2.0 mol/L の塩酸を 150 mL つくりたい。
12 mol/L の塩酸は何 mL 必要か。
(4) 0.10 mol/L の硫酸水溶液 100 mL と 0.20 mol/L の硫酸水溶液 400 mL を混合した水溶液 500 mL のモル濃度は何 mol/L か。
この動画を見る
●次の各問いに答えよ。
(1) 9.0 g のグルコース C₆H₁₂O₆ を水に溶かして 200 mL にした水溶液は何 mol/L か。
(2) 0.25 mol/L の水酸化ナトリウム NaOH 水溶液 200 mL 中に、NaOH は何 mol 含まれるか。また、含まれる NaOH の質量は何 g か。
(3) 12 mol/L の塩酸(塩化水素 HCl の水溶液)を水でうすめて 2.0 mol/L の塩酸を 150 mL つくりたい。
12 mol/L の塩酸は何 mL 必要か。
(4) 0.10 mol/L の硫酸水溶液 100 mL と 0.20 mol/L の硫酸水溶液 400 mL を混合した水溶液 500 mL のモル濃度は何 mol/L か。
【高校化学】●次の各問いに答えよ。(1) 尿素 5.0 g を水 45 g に溶かした水溶液の質量パーセント濃度は何 % か。(2) 5.0% の尿素水溶液 120 g に含まれる尿素は何 g か。

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
●次の各問いに答えよ。
(1) 尿素 5.0 g を水 45 g に溶かした水溶液の質量パーセント濃度は何 % か。
(2) 5.0% の尿素水溶液 120 g に含まれる尿素は何 g か。
(3) 10% の塩化ナトリウム水溶液 180 g と 20% の塩化ナトリウム水溶液 120 g を混合した
水溶液の質量パーセント濃度は何 % か。
この動画を見る
●次の各問いに答えよ。
(1) 尿素 5.0 g を水 45 g に溶かした水溶液の質量パーセント濃度は何 % か。
(2) 5.0% の尿素水溶液 120 g に含まれる尿素は何 g か。
(3) 10% の塩化ナトリウム水溶液 180 g と 20% の塩化ナトリウム水溶液 120 g を混合した
水溶液の質量パーセント濃度は何 % か。
1分で解いてほしい化学計算問題 (87) 水溶液の調製

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
0.100mol/L 塩化鉄(III)水溶液を 200mL 調製するには、塩化鉄(III)六水和物の結晶を何gはかりとる必要があるか。有効数字3桁で答えなさい。
$\mathrm{Fe Cl_3}$: 162.3 $\mathrm{H_2 O}$: 18
この動画を見る
0.100mol/L 塩化鉄(III)水溶液を 200mL 調製するには、塩化鉄(III)六水和物の結晶を何gはかりとる必要があるか。有効数字3桁で答えなさい。
$\mathrm{Fe Cl_3}$: 162.3 $\mathrm{H_2 O}$: 18
絶対に落としてはいけない計算 シュウ酸溶液の調製の計算問題
単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
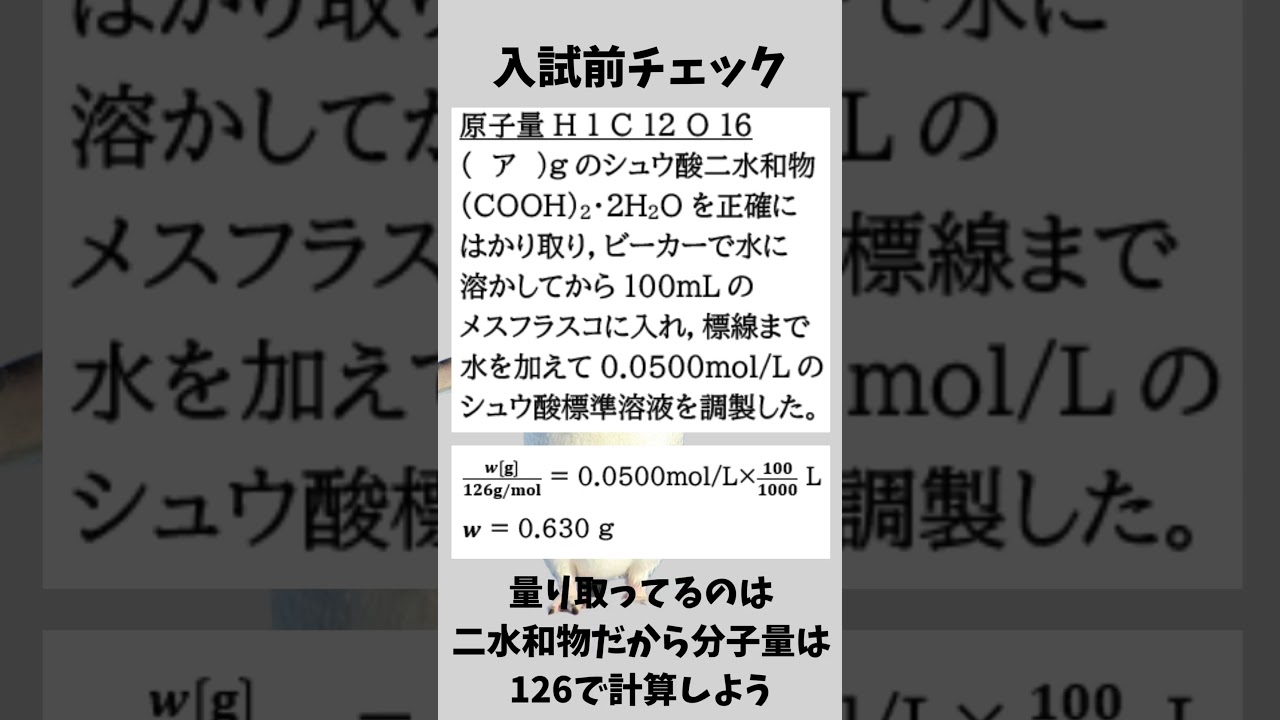
原子量H:1 C:12 O:16
(ア)gのシュウ酸二水和物$(COOH)_2・2H_2O$を正確にはかり取り,ビーカーで水に溶かしてから100 mLのメスフラスコに入れ,標線まで水を加えて0.0500 mol/Lのシュウ酸標準溶液を調整した
空欄アに入る数値を有効数字3桁で答えよ。
この動画を見る
原子量H:1 C:12 O:16
(ア)gのシュウ酸二水和物$(COOH)_2・2H_2O$を正確にはかり取り,ビーカーで水に溶かしてから100 mLのメスフラスコに入れ,標線まで水を加えて0.0500 mol/Lのシュウ酸標準溶液を調整した
空欄アに入る数値を有効数字3桁で答えよ。
【旧センター試験化学】2020追試 第1問 問5 凝固点降下度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
物質A,B,Cについて,それぞれ質量モル濃度0.10mol/kgの水溶液をつくり,凝固点降下度を測定した。その結果を表3に示す。(※表は動画内参照)ただし,物質A,B,Cは2種類の電解質(電解質1)と1種類の非電解質である。この実験結果から推測される記述として,誤りを含むものを,下の①~④のうちから一つ選べ。
①0.010mol/kgのグルコース水溶液の凝固点降下度は0.019Kである。
②0.010mol/kgの酢酸水溶液の凝固点降下度は0.038Kである。
③0.010mol/kgの塩化カリウム水溶液の凝固点降下度は0.038Kである。
④0.010mol/kgの塩化マグネシウム水溶液の凝固点降下度は0.057Kである。
この動画を見る
物質A,B,Cについて,それぞれ質量モル濃度0.10mol/kgの水溶液をつくり,凝固点降下度を測定した。その結果を表3に示す。(※表は動画内参照)ただし,物質A,B,Cは2種類の電解質(電解質1)と1種類の非電解質である。この実験結果から推測される記述として,誤りを含むものを,下の①~④のうちから一つ選べ。
①0.010mol/kgのグルコース水溶液の凝固点降下度は0.019Kである。
②0.010mol/kgの酢酸水溶液の凝固点降下度は0.038Kである。
③0.010mol/kgの塩化カリウム水溶液の凝固点降下度は0.038Kである。
④0.010mol/kgの塩化マグネシウム水溶液の凝固点降下度は0.057Kである。
理論化学基礎演習24 ¹²C = 12が ¹²C = 120に変更され,120gの¹²Cが1molになったらどうなるか?

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#物質量と濃度
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
仮に,相対質量の基準値を¹²C=12から¹²C=120に変更し,さらに¹²C 1molの質量を12gから120gに変更した場合,
①質量パーセント濃度が1.80%のグルコース水溶液におけるモル凝固点降下
②4.00g/Lの水溶液のpH
それぞれどうなるか。以下の選択肢から選びなさい。(変更前のNaOHの式量は40)
100倍になる,10倍になる,1増加する,1減少する,10分の1になる,100分の1になる
この動画を見る
仮に,相対質量の基準値を¹²C=12から¹²C=120に変更し,さらに¹²C 1molの質量を12gから120gに変更した場合,
①質量パーセント濃度が1.80%のグルコース水溶液におけるモル凝固点降下
②4.00g/Lの水溶液のpH
それぞれどうなるか。以下の選択肢から選びなさい。(変更前のNaOHの式量は40)
100倍になる,10倍になる,1増加する,1減少する,10分の1になる,100分の1になる
1分で解いてほしい化学計算問題 (73) 分子の数

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
1gに含まれる分子の数が最も多い物質を選びなさい。
(原子量 H 1 C 12 N 14 O 16 Ne 20 Cl 35.5 アボガドロ定数 6.0×10²³ /mol)
①塩素 ②酸素 ③窒素 ④二酸化炭素
⑤水 ⑥アンモニア ⑦ネオン ⑧メタン
この動画を見る
1gに含まれる分子の数が最も多い物質を選びなさい。
(原子量 H 1 C 12 N 14 O 16 Ne 20 Cl 35.5 アボガドロ定数 6.0×10²³ /mol)
①塩素 ②酸素 ③窒素 ④二酸化炭素
⑤水 ⑥アンモニア ⑦ネオン ⑧メタン
理論化学第29回 蒸気圧降下・沸点上昇・凝固点降下

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
希薄溶液の性質
・蒸気圧降下
・沸点上昇
・凝固点降下
【蒸気圧降下】
気液平衡状態において、気体になっている分子が衝突することで生じる圧力→蒸気圧
蒸気圧降下:溶媒の蒸発による濃度上昇を溶質が妨害することで起こる
同じ$100\,\rm{℃}$の水蒸気でも蒸気圧が純溶媒のときよりわずかに小さい。
氷になっている部分は溶媒ではない。
この動画を見る
希薄溶液の性質
・蒸気圧降下
・沸点上昇
・凝固点降下
【蒸気圧降下】
気液平衡状態において、気体になっている分子が衝突することで生じる圧力→蒸気圧
蒸気圧降下:溶媒の蒸発による濃度上昇を溶質が妨害することで起こる
同じ$100\,\rm{℃}$の水蒸気でも蒸気圧が純溶媒のときよりわずかに小さい。
氷になっている部分は溶媒ではない。
理論化学第28回 質量モル濃度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
質量モル濃度$[\rm{mol/kg}]$
→㎏=溶媒
$1\,\rm{kg}$の溶媒に溶けている物質量。
SはSolvent(溶媒)の頭文字
$\displaystyle \frac{n\,[\rm{mol}]}{S\,[\rm{kg}]}=m\,[\rm{mol/kg}]$
$n\,[\mathrm{mol}]=m\,[\mathrm{mol/kg}] \times S\,[\rm{kg}]$
$1\,\rm{kg}=1000\,\rm{g}$のスモール$s$だった場合式は、
$ m\,[\mathrm{mol/kg}] \times \frac{s}{1000}\,[\rm{kg}]$
になる。
molの公式は$n\,[\rm{mol}]=$の形で覚えよう!
【例題を計算しよう。】
尿素$\ce{(NH2)2CO}~6.0\,\rm{g}$を水$200\,\rm{g}$に溶かした場合
$30$%硫酸$(1.2\,\rm{g/cm^3})$のモル濃度・質量を求めよ。
この動画を見る
質量モル濃度$[\rm{mol/kg}]$
→㎏=溶媒
$1\,\rm{kg}$の溶媒に溶けている物質量。
SはSolvent(溶媒)の頭文字
$\displaystyle \frac{n\,[\rm{mol}]}{S\,[\rm{kg}]}=m\,[\rm{mol/kg}]$
$n\,[\mathrm{mol}]=m\,[\mathrm{mol/kg}] \times S\,[\rm{kg}]$
$1\,\rm{kg}=1000\,\rm{g}$のスモール$s$だった場合式は、
$ m\,[\mathrm{mol/kg}] \times \frac{s}{1000}\,[\rm{kg}]$
になる。
molの公式は$n\,[\rm{mol}]=$の形で覚えよう!
【例題を計算しよう。】
尿素$\ce{(NH2)2CO}~6.0\,\rm{g}$を水$200\,\rm{g}$に溶かした場合
$30$%硫酸$(1.2\,\rm{g/cm^3})$のモル濃度・質量を求めよ。
理論化学第27回 溶液の濃度(質量パーセント濃度とモル濃度の復習)

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
・質量パーセント濃度
・モル濃度$(\rm{mol/L})$
・質量モル濃度$(\rm{mol/kg})$
【例題を求めてみよう】
$100\,\rm{g}$の水に$25\,\rm{g}$の$\ce{NaCl}$を溶かした。
何%か?
溶液$1\,\rm{L}$中に溶ける溶質の物質量は$(\rm{mol})$
$2.0\,\rm{g}$の$\ce{NaOH}$を水に溶かし、$200\,\rm{mL}$の水溶液をつくった。
$0.100\,\rm{mol/L}$ シュウ酸を$100\,\rm{mL}$つくる。
$\ce{(COOH)_2・2H2O}$は何$\rm{g}$必要?
この動画を見る
・質量パーセント濃度
・モル濃度$(\rm{mol/L})$
・質量モル濃度$(\rm{mol/kg})$
【例題を求めてみよう】
$100\,\rm{g}$の水に$25\,\rm{g}$の$\ce{NaCl}$を溶かした。
何%か?
溶液$1\,\rm{L}$中に溶ける溶質の物質量は$(\rm{mol})$
$2.0\,\rm{g}$の$\ce{NaOH}$を水に溶かし、$200\,\rm{mL}$の水溶液をつくった。
$0.100\,\rm{mol/L}$ シュウ酸を$100\,\rm{mL}$つくる。
$\ce{(COOH)_2・2H2O}$は何$\rm{g}$必要?
1分で復習するモル計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
銅原子$Cu$ $3.0\times10^24$個は何$mol?$
この動画を見る
銅原子$Cu$ $3.0\times10^24$個は何$mol?$
理論化学基礎演習4 質量モル濃度の計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
問題:塩化カルシウム水和物$CaCl_2$・$2H_2O$ $14.7g$を水$1000g$に溶かした水溶液と同じ凝固点を示す。
塩化$NaCI$水溶液を水$1000g$を用いて作るとき、必要な塩化ナトリウムの質量$[g]$の値を有効数字3桁で求めなさい。
ただし、電解質は完全に電離するものとする。
(原子量H10 16 Na 23 CI 35.5 Ca 40)
この動画を見る
問題:塩化カルシウム水和物$CaCl_2$・$2H_2O$ $14.7g$を水$1000g$に溶かした水溶液と同じ凝固点を示す。
塩化$NaCI$水溶液を水$1000g$を用いて作るとき、必要な塩化ナトリウムの質量$[g]$の値を有効数字3桁で求めなさい。
ただし、電解質は完全に電離するものとする。
(原子量H10 16 Na 23 CI 35.5 Ca 40)
