 中和と塩
中和と塩
 中和と塩
中和と塩
2024追試第4問 問4b ステアリン酸単分子膜
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
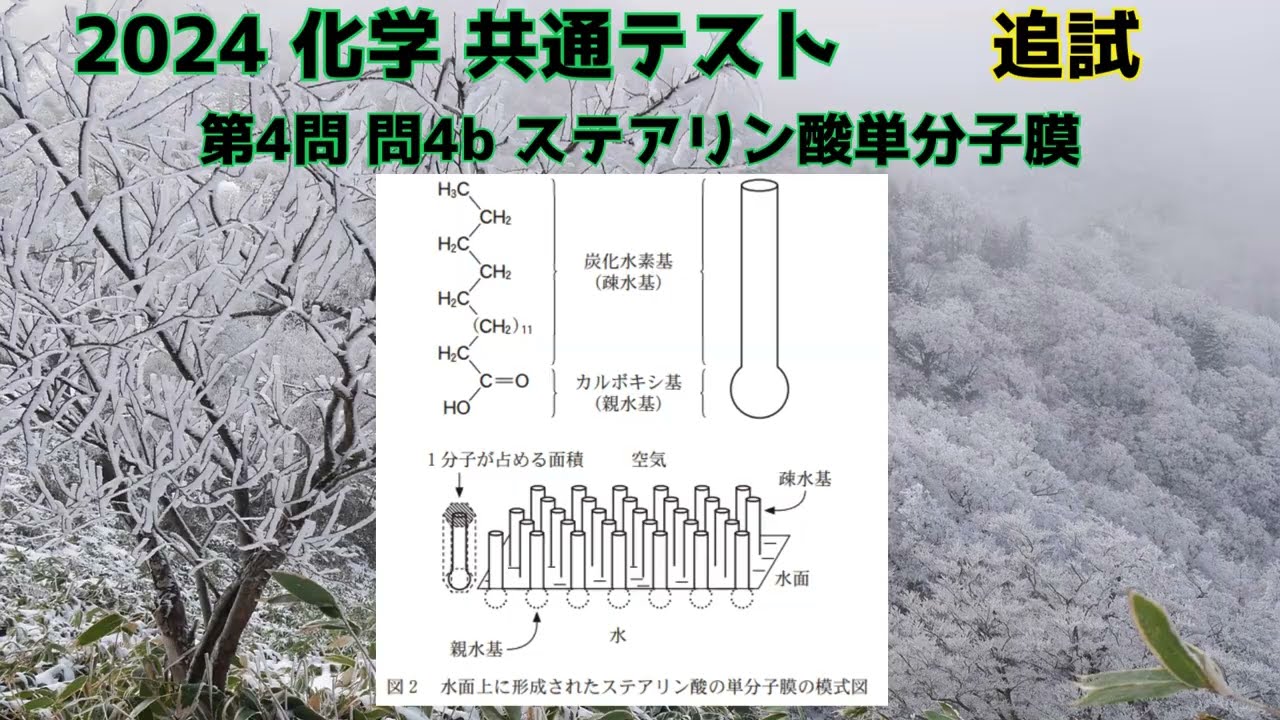
b シクロヘキサンに溶かしたステアリン
酸$\ce{CH3 (CH2)16COOH}$(分子量$284$) を水面に滴下すると、
溶液が水面上に広がる。
シクロヘキサンが十分に揮発すると、図2に示すように、
ステアリン酸分子は親水性のカルボキシ基を水 中に向け、
疎水性の炭化水素基を空気側に向けた状態で単分子膜を形成する。
濃度$0.568\,\rm{g/L}$のステアリン酸のシクロヘキサン溶液$0.100\,\rm{mL}$を水面に 滴下した、シクロヘキサンが十分に揮発した後、
単分子膜の面積は$252\rm{cm^2} $であった。
ステアリン酸分子が水面をすき間なく覆っているとすると、ステ アリン酸1分子が水面上で占める面積の平均値は何$\rm{cm^2}$か。
最も適当な数 値を、後の①~⑥のうちから一つ選べ。
ただし、アボガドロ定数を $6.0 \times 10^{23}\,\rm{/mol}$とする。
①$2.1 \times 10^{-15}$
②$2.3 \times 10^{-15}$
③$2.4 \times 10^{-15}$
④$4.2 \times 10^{-15}$
⑤$6.8 \times 10^{-15}$
⑥$7.6 \times 10^{-15}$
※図は動画内参照
この動画を見る
b シクロヘキサンに溶かしたステアリン
酸$\ce{CH3 (CH2)16COOH}$(分子量$284$) を水面に滴下すると、
溶液が水面上に広がる。
シクロヘキサンが十分に揮発すると、図2に示すように、
ステアリン酸分子は親水性のカルボキシ基を水 中に向け、
疎水性の炭化水素基を空気側に向けた状態で単分子膜を形成する。
濃度$0.568\,\rm{g/L}$のステアリン酸のシクロヘキサン溶液$0.100\,\rm{mL}$を水面に 滴下した、シクロヘキサンが十分に揮発した後、
単分子膜の面積は$252\rm{cm^2} $であった。
ステアリン酸分子が水面をすき間なく覆っているとすると、ステ アリン酸1分子が水面上で占める面積の平均値は何$\rm{cm^2}$か。
最も適当な数 値を、後の①~⑥のうちから一つ選べ。
ただし、アボガドロ定数を $6.0 \times 10^{23}\,\rm{/mol}$とする。
①$2.1 \times 10^{-15}$
②$2.3 \times 10^{-15}$
③$2.4 \times 10^{-15}$
④$4.2 \times 10^{-15}$
⑤$6.8 \times 10^{-15}$
⑥$7.6 \times 10^{-15}$
※図は動画内参照
2024追試第4問 問4 界面活性剤

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
界面活性剤の性質に関する記述として下線部に誤りを含むものはどれか。 最も適当なものを、次の①~④のうちから一つ選べ。
① セッケンは水の表面張力を低下させるはたらきをするため、セッケン水 は繊維の内部に浸透することができる。
② セッケンの洗浄力は、硬水中でも低下しない。
③ 陽イオン界面活性剤は洗浄力は弱いが、頭髪用コンディショナー(リンス)などに含まれており、帯電防止効果や柔軟効果を与える。
④ 界面活性剤の乳化作用により、油分をミセル内部に取り込んだ微粒子を 水中に分散させた乳濁液を得ることができ、乳化作用は食品や化粧品など に利用される。
この動画を見る
界面活性剤の性質に関する記述として下線部に誤りを含むものはどれか。 最も適当なものを、次の①~④のうちから一つ選べ。
① セッケンは水の表面張力を低下させるはたらきをするため、セッケン水 は繊維の内部に浸透することができる。
② セッケンの洗浄力は、硬水中でも低下しない。
③ 陽イオン界面活性剤は洗浄力は弱いが、頭髪用コンディショナー(リンス)などに含まれており、帯電防止効果や柔軟効果を与える。
④ 界面活性剤の乳化作用により、油分をミセル内部に取り込んだ微粒子を 水中に分散させた乳濁液を得ることができ、乳化作用は食品や化粧品など に利用される。
2024追試第3問 問3b いわゆる逆滴定の操作方法
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
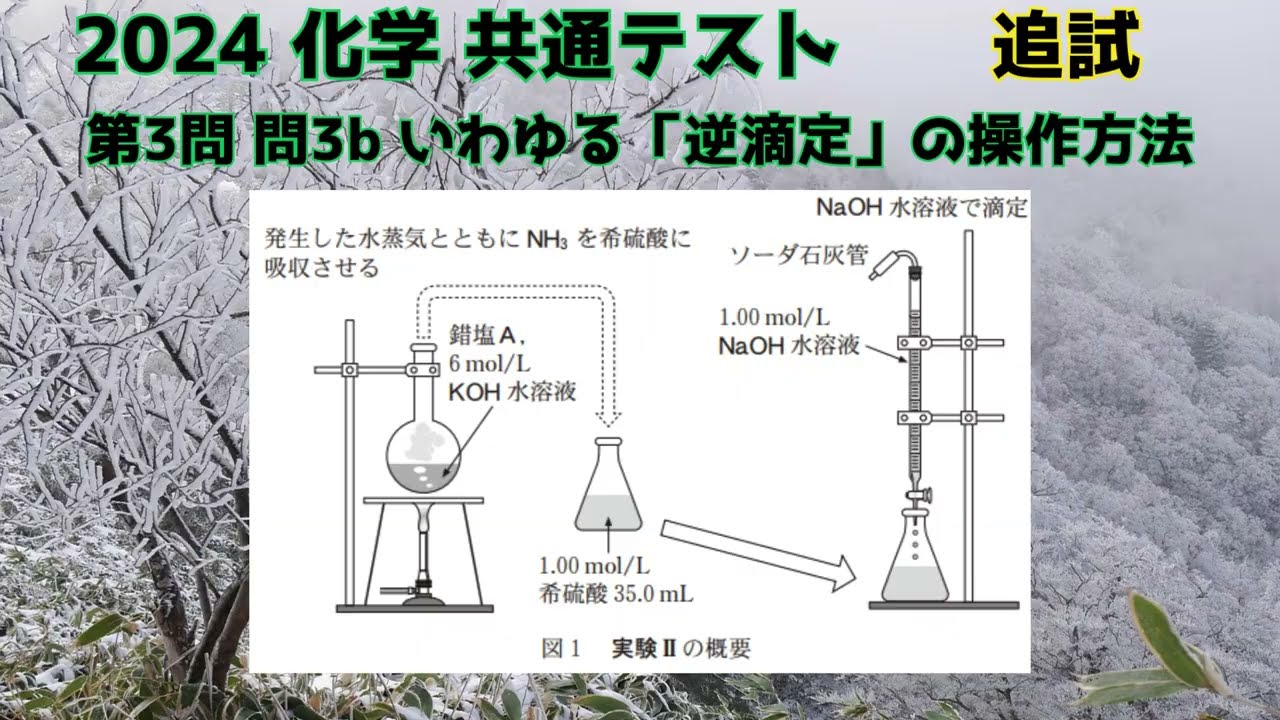
実験II 結果Iに基づき、
$\ce{Co^{3+}}$ を $0.0100\,\rm{mol} $含む$A$をはかり取り、丸底フラ スコに入れ、図1に示すように、$A$中から$\ce{NH3}$を完全に発生させるために十分な体積の$6\,\rm{mol/L} $水酸化カリウム$\ce{KOH}$水溶液を加えて煮沸した。
このとき、発生した水蒸気とともに$\ce{NH3}$を$1.00\,\rm{mol/L}$の希硫酸$ 35.0\,\rm{mL}$にすべて吸収させた。
$\ce{NH3}$を吸収した希硫酸に適切な指示薬$B$を加え、$1.00\,\rm{mol/L}$ の水酸化ナトリウム $\ce{NaOH}$水溶液を使って滴定した。結果 指示薬$B$の変色には$20.00\,\rm{mL}$の$\ce{NaOH}$水溶液が必要であった。
実験までは、$A$が分解されて発生した$\ce{NH3}$を過剰駄の希硫酸に吸収させ、$\ce{NH3}$と反応せずに残った硫酸を$\ce{NaOH}$水溶液により中和滴定することで、発生した$\ce{NH3}$の物質量を求めている。実験目に関する記述として誤りを含むものはどれか、最も適当なものを、次の①~④のうちから一つ選べ。
① $\ce{NH3}$を吸収させる者続能を入れる三月フラスコは、現浄して純水ですすいだ後に、ぬれたまま用いてもよい。
②$\ce{NaOH}$水容液による中和演定で、残った破能と$\ce{NaOH}$が遊不足なく反応した時点では、木容後は中性となる。
③ $\ce{NaOH}$ 水溶液による中和演定では、指示第日としてメチルオレンジを用いる。
③ この清定に用いるビュレットの上部にソーダ管を取り付けているのは、$\ce{NaOH}$ 水浴液が大気中の$\ce{CO2}$を吸収するのを防ぐためである。
※図は動画内参照
この動画を見る
実験II 結果Iに基づき、
$\ce{Co^{3+}}$ を $0.0100\,\rm{mol} $含む$A$をはかり取り、丸底フラ スコに入れ、図1に示すように、$A$中から$\ce{NH3}$を完全に発生させるために十分な体積の$6\,\rm{mol/L} $水酸化カリウム$\ce{KOH}$水溶液を加えて煮沸した。
このとき、発生した水蒸気とともに$\ce{NH3}$を$1.00\,\rm{mol/L}$の希硫酸$ 35.0\,\rm{mL}$にすべて吸収させた。
$\ce{NH3}$を吸収した希硫酸に適切な指示薬$B$を加え、$1.00\,\rm{mol/L}$ の水酸化ナトリウム $\ce{NaOH}$水溶液を使って滴定した。結果 指示薬$B$の変色には$20.00\,\rm{mL}$の$\ce{NaOH}$水溶液が必要であった。
実験までは、$A$が分解されて発生した$\ce{NH3}$を過剰駄の希硫酸に吸収させ、$\ce{NH3}$と反応せずに残った硫酸を$\ce{NaOH}$水溶液により中和滴定することで、発生した$\ce{NH3}$の物質量を求めている。実験目に関する記述として誤りを含むものはどれか、最も適当なものを、次の①~④のうちから一つ選べ。
① $\ce{NH3}$を吸収させる者続能を入れる三月フラスコは、現浄して純水ですすいだ後に、ぬれたまま用いてもよい。
②$\ce{NaOH}$水容液による中和演定で、残った破能と$\ce{NaOH}$が遊不足なく反応した時点では、木容後は中性となる。
③ $\ce{NaOH}$ 水溶液による中和演定では、指示第日としてメチルオレンジを用いる。
③ この清定に用いるビュレットの上部にソーダ管を取り付けているのは、$\ce{NaOH}$ 水浴液が大気中の$\ce{CO2}$を吸収するのを防ぐためである。
※図は動画内参照
2024追試第1問 問1 塩の知識問題

単元:
#物理#化学#大学入試過去問(物理)#化学基礎2ー物質の変化#中和と塩#理科(高校生)#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
次の記述ア・イの両方に当てはまる塩はどれか。
最も適当なものを、後の ①~④のうちから一つ選べ。
ア 水溶液は塩基性を示す。
イ 二重結合をもたない。
① 塩化アンモニウム
② 硫化ナトリウム
③ 乳酸ナトリウム
④ 塩化カルシウム
この動画を見る
次の記述ア・イの両方に当てはまる塩はどれか。
最も適当なものを、後の ①~④のうちから一つ選べ。
ア 水溶液は塩基性を示す。
イ 二重結合をもたない。
① 塩化アンモニウム
② 硫化ナトリウム
③ 乳酸ナトリウム
④ 塩化カルシウム
【化学】古い過去問 センター試験2008年度 第3問 問6 気体の発生反応

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#酸と塩基・水素イオン濃度#化学変化と化学反応式#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
下線の化合物$1mol$がすべて反応したとき、発生する気体が最も少ないものを、次の①~⑤のうちから一つ選べ。
①硫化鉄$FeS$に希硫酸を加える。
②塩素酸カリウム$KCIO_3$に、触媒である酸化マンガン(Ⅳ)を加えて加熱する。
③過酸化水素$H_2O_2$の水溶液を、触媒である酸化マンガン(Ⅳ)を加える。
④炭酸水素ナトリウム$NaHCO_3$に希塩酸を加える。
⑤亜硫酸ナトリウム$NaHSO_3$に希塩酸を加える。
この動画を見る
下線の化合物$1mol$がすべて反応したとき、発生する気体が最も少ないものを、次の①~⑤のうちから一つ選べ。
①硫化鉄$FeS$に希硫酸を加える。
②塩素酸カリウム$KCIO_3$に、触媒である酸化マンガン(Ⅳ)を加えて加熱する。
③過酸化水素$H_2O_2$の水溶液を、触媒である酸化マンガン(Ⅳ)を加える。
④炭酸水素ナトリウム$NaHCO_3$に希塩酸を加える。
⑤亜硫酸ナトリウム$NaHSO_3$に希塩酸を加える。
【化学】古い過去問 センター試験2004年度 第3問 問1 中和の量的関係

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#酸と塩基・水素イオン濃度#共通テスト#中和と塩
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$0.10 mol/l$ のシュウ酸$(COOH)_2$ 水溶液と、濃度未知の塩酸がある。
それぞ れ$10ml$を、ある濃度の水酸化水溶液で滴定したところ、中和に要 した体積は、それぞれ$7.5ml$と$15.0ml$であった。
この塩酸の濃度は何$mol/l$ か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$0.025$
②$0.050$
③$0.10$
④$0.20$
⑤$0.40$
⑥$0.80$
この動画を見る
$0.10 mol/l$ のシュウ酸$(COOH)_2$ 水溶液と、濃度未知の塩酸がある。
それぞ れ$10ml$を、ある濃度の水酸化水溶液で滴定したところ、中和に要 した体積は、それぞれ$7.5ml$と$15.0ml$であった。
この塩酸の濃度は何$mol/l$ か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$0.025$
②$0.050$
③$0.10$
④$0.20$
⑤$0.40$
⑥$0.80$
グラフ問題19 滴定曲線(2)

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
滴定実験における滴定曲線の概形として最も適切なものはどれか。
下の中からそれぞれ選びなさい。
ただし、各水溶液中の溶質の濃度はいずれも$0.10mol/L$とする。
・炭酸水溶液を塩酸で滴定した。
・炭酸ナトリウムと炭酸水素ナトリウムの混合水溶液を塩酸で滴定した。
※グラフは動画内参照
この動画を見る
滴定実験における滴定曲線の概形として最も適切なものはどれか。
下の中からそれぞれ選びなさい。
ただし、各水溶液中の溶質の濃度はいずれも$0.10mol/L$とする。
・炭酸水溶液を塩酸で滴定した。
・炭酸ナトリウムと炭酸水素ナトリウムの混合水溶液を塩酸で滴定した。
※グラフは動画内参照
グラフ問題12 中和と電気伝導率の変化

単元:
#化学#化学基礎2ー物質の変化#化学理論#化学平衡と平衡移動#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ビーカーに$0.100mol/L$の塩酸を$10.00mL$入れ、
ここに電極間の距離が固定されている2本の白金電極を浸して、それらの電極からの導線を電流計と定電圧電源に接続した(図1)。
この状態で定電圧電源のスイッチを入れ、電流値を測定した。
次にこの塩酸の入ったビーカーに$0.100mol/L$の水酸化ナトリウム水溶液を滴下しながら、その都度一定の電圧をかけ、その時の電流 値を記録した。
この操作を水酸化ナトリウム水溶液の滴下量が $20.0mL$になるまで行った。
通電は電流値の測定時にだけ極めて 短時間行うものとし、
いずれの電極においても水の電気分解や 気体の発生などの
酸化還元反応、液温の変化などは無視できるものとする。
また全てのイオンにおいて、電流値への寄与は等 しいものとする。
実験結果を、横軸を水酸化ナトリウム水溶液の滴下量$〔mL〕$、縦軸を電流$ 〔A〕 $としたグラフで表すと
どのようになるか。
最も適切なグラフを図2の$A~F$から一つ選べ。
ただし、これらの全てのグラフでは目盛りは同一である。
($0.100mol/L$の塩酸$10.00mL$に$0.100mol/L$
の水酸化ナトリウム水溶液を加えている)
※図・グラフは動画内参照
この動画を見る
ビーカーに$0.100mol/L$の塩酸を$10.00mL$入れ、
ここに電極間の距離が固定されている2本の白金電極を浸して、それらの電極からの導線を電流計と定電圧電源に接続した(図1)。
この状態で定電圧電源のスイッチを入れ、電流値を測定した。
次にこの塩酸の入ったビーカーに$0.100mol/L$の水酸化ナトリウム水溶液を滴下しながら、その都度一定の電圧をかけ、その時の電流 値を記録した。
この操作を水酸化ナトリウム水溶液の滴下量が $20.0mL$になるまで行った。
通電は電流値の測定時にだけ極めて 短時間行うものとし、
いずれの電極においても水の電気分解や 気体の発生などの
酸化還元反応、液温の変化などは無視できるものとする。
また全てのイオンにおいて、電流値への寄与は等 しいものとする。
実験結果を、横軸を水酸化ナトリウム水溶液の滴下量$〔mL〕$、縦軸を電流$ 〔A〕 $としたグラフで表すと
どのようになるか。
最も適切なグラフを図2の$A~F$から一つ選べ。
ただし、これらの全てのグラフでは目盛りは同一である。
($0.100mol/L$の塩酸$10.00mL$に$0.100mol/L$
の水酸化ナトリウム水溶液を加えている)
※図・グラフは動画内参照
グラフ問題8 滴定曲線を選ぶ基本問題!

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$25,0℃$で$0.100mol/L$の酢酸$10.0mL$に対し
$0.100mol/L$の水酸化カリウム水溶液を滴下したとき
滴定曲線として適切なのは、(ア)~(エ)のどれか。
適切な記号を1つ選び、それを選択した理由を記せ。
※グラフは動画内参照
この動画を見る
$25,0℃$で$0.100mol/L$の酢酸$10.0mL$に対し
$0.100mol/L$の水酸化カリウム水溶液を滴下したとき
滴定曲線として適切なのは、(ア)~(エ)のどれか。
適切な記号を1つ選び、それを選択した理由を記せ。
※グラフは動画内参照
【短時間で要点チェック!!】イオン化傾向、電池基礎〔現役講師解説、高校化学、化学基礎、2023年度版〕

【化学】古い過去問 センター試験2002年度 第3問 問5 KOHとKClの混合物からKOHの比率を出す計算

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
水酸化カリウムと塩化カリウムとの混合物$10g$を純水に溶かした。
この溶 液を中和するのに、$2.5mol/L$の硫酸$10ml$を要した。
もとの混合物は、水酸化カリウムを質量で何$%$含んでいたか。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
①$7.0$
②$14$
③$28$
④$56$
⑤$72$
⑥$86$
この動画を見る
水酸化カリウムと塩化カリウムとの混合物$10g$を純水に溶かした。
この溶 液を中和するのに、$2.5mol/L$の硫酸$10ml$を要した。
もとの混合物は、水酸化カリウムを質量で何$%$含んでいたか。
最も適当な数値を、次の①~⑥のうち から一つ選べ。
①$7.0$
②$14$
③$28$
④$56$
⑤$72$
⑥$86$
1分で解いてほしい化学計算問題 (44) 逆滴定によるアンモニアの定量

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2023年 崇城大学(薬・改)]
実験で発生したアンモニアを$0.20mol/L$の希硫酸$100mL$に吸収させてアンモニアを完全に反応させた。
残った硫酸を$0.50mol/L$水酸化ナトリウム水溶液で滴定しところ、$20mL$を要した。
吸収されたアンモニアは何$g$か。
有効数字2桁で示せ。
$NH_3$の分子量 $17$
この動画を見る
[2023年 崇城大学(薬・改)]
実験で発生したアンモニアを$0.20mol/L$の希硫酸$100mL$に吸収させてアンモニアを完全に反応させた。
残った硫酸を$0.50mol/L$水酸化ナトリウム水溶液で滴定しところ、$20mL$を要した。
吸収されたアンモニアは何$g$か。
有効数字2桁で示せ。
$NH_3$の分子量 $17$
2024年 共通テスト 化学 出題予想!5つに絞ってみた

単元:
#化学#化学基礎2ー物質の変化#化学理論#無機#有機#大学入試過去問(化学)#物質の三態と状態変化#芳香族化合物#共通テスト#非金属元素の単体と化合物#化学(高分子)#合成樹脂とゴム#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2024年 共通テスト 化学 出題予想!5つに絞ってみた
予想1:滴定曲線(緩衝液)と$pH$
予想2:ボルンハーバーサイクル
予想3:オストワルト法
予想4:芳香族化合物の分離
予想5:合成高分子化合物(ゴム)
※共通テスト対策※
・過去問や模試の復習で知識の穴を減らしていく
・共通テスト形式の問題集で実践練習するとなお良い。
この動画を見る
2024年 共通テスト 化学 出題予想!5つに絞ってみた
予想1:滴定曲線(緩衝液)と$pH$
予想2:ボルンハーバーサイクル
予想3:オストワルト法
予想4:芳香族化合物の分離
予想5:合成高分子化合物(ゴム)
※共通テスト対策※
・過去問や模試の復習で知識の穴を減らしていく
・共通テスト形式の問題集で実践練習するとなお良い。
【化学】古い過去問 センター試験2001年度 第2問 問1 圧力変化のグラフ

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
濃度が$0.10 mol/L$の酸$a・b$を$10ml$ずつ取り、
それぞれを$0.10 mol/l$水酸化ナトリウム水溶液で滴定し、
滴下量と溶液の$pH$との関係を調べた。
図1に示した滴定曲線を与える酸の組合せとして最も適当なものを、下の①~ ⑥のうちから一つ選べ。
※図・表は動画内参照
この動画を見る
濃度が$0.10 mol/L$の酸$a・b$を$10ml$ずつ取り、
それぞれを$0.10 mol/l$水酸化ナトリウム水溶液で滴定し、
滴下量と溶液の$pH$との関係を調べた。
図1に示した滴定曲線を与える酸の組合せとして最も適当なものを、下の①~ ⑥のうちから一つ選べ。
※図・表は動画内参照
【短時間でやり方マスター!!】中和滴定〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
新課程対応
中和滴定について解説します。
滴定曲線・実験器具・計算
この動画を見る
新課程対応
中和滴定について解説します。
滴定曲線・実験器具・計算
【短時間でやり方マスター!!】中和の基礎と塩と液性(酸性・中性・塩基性)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
新課程対応
中和の基礎
塩と液性について解説します。
濃度未知の塩酸10mLを過不足なく中和するのに0.050mol/L水酸化ナトリウム水溶液4.0mLを要した。
この塩酸の濃度は?
この動画を見る
新課程対応
中和の基礎
塩と液性について解説します。
濃度未知の塩酸10mLを過不足なく中和するのに0.050mol/L水酸化ナトリウム水溶液4.0mLを要した。
この塩酸の濃度は?
化学基礎の教科書を解説する動画 第50回 塩の化学反応

化学基礎の教科書を解説する動画 第49回 塩の分類と水溶液の性質

化学基礎の教科書を解説する動画 第48回 滴定曲線 酸塩基の強弱の組み合わせがポイント

単元:
#化学#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎 教科書の解説
〔滴定曲線〕
①$HCℓ+NaOH$
②$CH_3COOH+NaOH$
③$HCℓ+NH_3$
この動画を見る
化学基礎 教科書の解説
〔滴定曲線〕
①$HCℓ+NaOH$
②$CH_3COOH+NaOH$
③$HCℓ+NH_3$
化学基礎の教科書を解説する動画 第47回 中和滴定の実験器具 なぜ共洗いが必要なのか?

化学基礎の教科書を解説する動画 第46回 中和の量的関係(問題演習編)

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学基礎 教科書の解説
〔中和の量的関係(例題解説)〕
$\boxed{ 基本 } H^{+}+OH^{-}→H_2O$
1)希硫酸$10mL$を過不足なく中和するのに
$0.10mol/L NaCH 80mL$を必要とした。
$H_2SO_4$の濃度〔$mol/L$〕は?
2)酢酸$10mL$を$0.10mol/L NaOH$中和するのに$9.6mL$を要した。
酢酸の濃度は?
この動画を見る
化学基礎 教科書の解説
〔中和の量的関係(例題解説)〕
$\boxed{ 基本 } H^{+}+OH^{-}→H_2O$
1)希硫酸$10mL$を過不足なく中和するのに
$0.10mol/L NaCH 80mL$を必要とした。
$H_2SO_4$の濃度〔$mol/L$〕は?
2)酢酸$10mL$を$0.10mol/L NaOH$中和するのに$9.6mL$を要した。
酢酸の濃度は?
化学基礎の教科書を解説する動画 第45回 中和の量的関係

化学基礎の教科書を解説する動画 第44回 中和の反応式

【テーマ別解説】アンモニアの中和の反応式が書けるようになる動画

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
○中和の反応式の書き方
(例) $NaOH, Hcℓ$
(例) $NH_3, Hcℓ$
(例) $KOH, H_2SO_4$
(例) $NH_3, H_2SO_4$
この動画を見る
○中和の反応式の書き方
(例) $NaOH, Hcℓ$
(例) $NH_3, Hcℓ$
(例) $KOH, H_2SO_4$
(例) $NH_3, H_2SO_4$
高校化学の計算問題(問題011・2021大阪医科薬科大学) 炭酸ナトリウムが2段階で中和する理由とは?

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#中和と塩#理科(高校生)#大阪医科薬科大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
必要があれば,次の値を使うこと。
原子量 $H 1.0 C 12 O 16 Na 23$
問 不純物を含む炭酸ナトリウムの粉末 1.0g を純水に溶解して,正確に 200mL の水溶液を調製した。
この水溶液から 20mL をコニカルビーカーにはかり取って,指示薬としてフェノールフタレインを数滴加えた。
はかり取った水溶液を 0.10mol/L の塩酸で滴定したところ,8.0mL 滴下したところで水溶液の色が $\boxed{ア}$ に変化したので,1 回目の中和点とした。
次に,指示薬としてメチルオレンジを数滴加えて,0.10mol/L の塩酸で続けて滴定したところ,さらに $\boxed{A}$ mL 滴下した
ところで,水溶液の色が $\boxed{イ} $に変化したので,2 回目の中和点とした。
次の(1)~(3)に答えなさい。
ただし,不純物は反応に関与しないものとする。
(1) 空欄 $\boxed{ア} , \boxed{イ}$ にあてはまる色の変化の組合せとして正しいものを,次の a~d のうちから一つ選びなさい。
a 赤色から無色(ア) 赤色から黄色(イ)
b 赤色から無色(ア) 黄色から赤色(イ)
c 無色から赤色(ア) 赤色から黄色(イ)
d 無色から赤色(ア) 黄色から赤色(イ)
(2) 空欄 $\boxed{A}$ にあてはまる数値として最も適当なものを,次の a~e のうちから一つ選びなさい。
a 2.0 b 4.0 c 8.0 d 12 e 16
(3) この粉末中の炭酸ナトリウムの純度〔質量%〕は何%か。
有効数字 2 桁で答えなさい。
この動画を見る
必要があれば,次の値を使うこと。
原子量 $H 1.0 C 12 O 16 Na 23$
問 不純物を含む炭酸ナトリウムの粉末 1.0g を純水に溶解して,正確に 200mL の水溶液を調製した。
この水溶液から 20mL をコニカルビーカーにはかり取って,指示薬としてフェノールフタレインを数滴加えた。
はかり取った水溶液を 0.10mol/L の塩酸で滴定したところ,8.0mL 滴下したところで水溶液の色が $\boxed{ア}$ に変化したので,1 回目の中和点とした。
次に,指示薬としてメチルオレンジを数滴加えて,0.10mol/L の塩酸で続けて滴定したところ,さらに $\boxed{A}$ mL 滴下した
ところで,水溶液の色が $\boxed{イ} $に変化したので,2 回目の中和点とした。
次の(1)~(3)に答えなさい。
ただし,不純物は反応に関与しないものとする。
(1) 空欄 $\boxed{ア} , \boxed{イ}$ にあてはまる色の変化の組合せとして正しいものを,次の a~d のうちから一つ選びなさい。
a 赤色から無色(ア) 赤色から黄色(イ)
b 赤色から無色(ア) 黄色から赤色(イ)
c 無色から赤色(ア) 赤色から黄色(イ)
d 無色から赤色(ア) 黄色から赤色(イ)
(2) 空欄 $\boxed{A}$ にあてはまる数値として最も適当なものを,次の a~e のうちから一つ選びなさい。
a 2.0 b 4.0 c 8.0 d 12 e 16
(3) この粉末中の炭酸ナトリウムの純度〔質量%〕は何%か。
有効数字 2 桁で答えなさい。
【式の理由を理解!!】二段階中和〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#化学基礎2ー物質の変化#中和と塩
指導講師:
3rd School
問題文全文(内容文):
化学基礎
二段階中和
Q.濃度不明の$\mathsf{NaOH}$と$\mathsf{Na_2CO_3}$の混合溶液を20mL取り、1.0mol/Lの塩酸を滴下したところ、以下のような滴定曲線になった。この混合溶液20mL中に含まれていた$\mathsf{NaOH}$と$\mathsf{Na_2CO_3}$はそれぞれ何mol?
※図は動画内参照
この動画を見る
化学基礎
二段階中和
Q.濃度不明の$\mathsf{NaOH}$と$\mathsf{Na_2CO_3}$の混合溶液を20mL取り、1.0mol/Lの塩酸を滴下したところ、以下のような滴定曲線になった。この混合溶液20mL中に含まれていた$\mathsf{NaOH}$と$\mathsf{Na_2CO_3}$はそれぞれ何mol?
※図は動画内参照
高校化学の計算問題(問題007)逆滴定の計算はやり取りする水素イオンを数えて対処しよう!

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
必要があれば,定数および原子量は次の値を用いよ。
標準状態は,$0℃,1.0×10^5Pa$ とする。
(定 数) 気体定数 $R=8.3×10^3Pa・L/(K・mol)$
問題 アンモニアを $0.100mol/L$ の硫酸 150mL に吸収させて完全に反応させたのち,この溶液を過不足なく中和するのに$0.500mol/L$ の水酸化ナトリウム水溶液を 20.0mL 要した。
吸収されたアンモニアの標準状態における体積[mL]として適切なものを,次の数値 A~F のうちから1つ選べ。
A:$112$ B;$224$ C:$448$ D:$560$ E :$896$ F :$1.12×10^3$
この動画を見る
必要があれば,定数および原子量は次の値を用いよ。
標準状態は,$0℃,1.0×10^5Pa$ とする。
(定 数) 気体定数 $R=8.3×10^3Pa・L/(K・mol)$
問題 アンモニアを $0.100mol/L$ の硫酸 150mL に吸収させて完全に反応させたのち,この溶液を過不足なく中和するのに$0.500mol/L$ の水酸化ナトリウム水溶液を 20.0mL 要した。
吸収されたアンモニアの標準状態における体積[mL]として適切なものを,次の数値 A~F のうちから1つ選べ。
A:$112$ B;$224$ C:$448$ D:$560$ E :$896$ F :$1.12×10^3$
高校化学の計算問題(問題003)実験でよくやる中和滴定 食酢のパーセント濃度はどうやって求めるのか?

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
必要があれば,原子量は次の値を使いなさい。
$H 1.0 C 12 O 16$
次の問いに答えなさい。
食酢に含まれる酢酸の濃度を調べるため,以下の実験を行った。
食酢の密度は $1.0g/cm^3$であるとし,また,食酢に含まれる酸は酢酸のみであるものとする。
水酸化ナトリウム $NaOH$ 約 0.4g を水に溶かし,100mL の水溶液をつくった(a液とする)。
a 液を用いて,$0.050mol/L$ のシュウ酸$(COOH)_2$ 水溶液 10.0mL を中和滴定したところ,中和点に達するまでに 11.1mL を要した。
食酢を正確に 5 倍にうすめてつくった水溶液(b 液とする)10.0mL を a 液で中和滴定したところ,中和点に達するまでに 15.8mL を要した。
問 1 a液のモル濃度は何 $mol/L$ か。
最も適当な数値を,次の1~6から一つ選びなさい。
① 0.030 ② 0.045 ③ 0.056 ④ 0.090 ⑤ 0.099 ⑥ 0.18
問 2 b液のモル濃度は何 mol/L か。最も適当な数値を,次の1~6から一つ選びなさい。
① 0.12 ② 0.14 ③ 0.20 ④ 0.28 ⑤ 0.57 ⑥ 0.71
問 3 薄める前の食酢に含まれる酢酸の質量パーセント濃度は何%か。最も適当な数値を,次の
1~6から一つ選びなさい。
① 0.85 ② 2.1 ③ 3.4 ④ 4.3 ⑤ 7.2 ⑥ 9.6
この動画を見る
必要があれば,原子量は次の値を使いなさい。
$H 1.0 C 12 O 16$
次の問いに答えなさい。
食酢に含まれる酢酸の濃度を調べるため,以下の実験を行った。
食酢の密度は $1.0g/cm^3$であるとし,また,食酢に含まれる酸は酢酸のみであるものとする。
水酸化ナトリウム $NaOH$ 約 0.4g を水に溶かし,100mL の水溶液をつくった(a液とする)。
a 液を用いて,$0.050mol/L$ のシュウ酸$(COOH)_2$ 水溶液 10.0mL を中和滴定したところ,中和点に達するまでに 11.1mL を要した。
食酢を正確に 5 倍にうすめてつくった水溶液(b 液とする)10.0mL を a 液で中和滴定したところ,中和点に達するまでに 15.8mL を要した。
問 1 a液のモル濃度は何 $mol/L$ か。
最も適当な数値を,次の1~6から一つ選びなさい。
① 0.030 ② 0.045 ③ 0.056 ④ 0.090 ⑤ 0.099 ⑥ 0.18
問 2 b液のモル濃度は何 mol/L か。最も適当な数値を,次の1~6から一つ選びなさい。
① 0.12 ② 0.14 ③ 0.20 ④ 0.28 ⑤ 0.57 ⑥ 0.71
問 3 薄める前の食酢に含まれる酢酸の質量パーセント濃度は何%か。最も適当な数値を,次の
1~6から一つ選びなさい。
① 0.85 ② 2.1 ③ 3.4 ④ 4.3 ⑤ 7.2 ⑥ 9.6
【現役塾講師による詳しい解説と講評!】2023年共通テスト化学基礎解答解説〔現役塾講師解説、高校化学、化学基礎〕

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#大学入試過去問(化学)#物質の成分と構成元素#原子の構成と元素の周期表#化学結合#物質量と濃度#酸と塩基・水素イオン濃度#共通テスト#化学変化と化学反応式#中和と塩#酸化還元反応#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
2023年共通テスト化学基礎の解答を解説します。
この動画を見る
2023年共通テスト化学基礎の解答を解説します。
【これで計算も知識もバッチリ!!】中和の基礎・計算・中和滴定・塩と液性・弱酸(弱塩基)の遊離・逆滴定〔現役塾講師解説、高校化学、化学基礎、2022年度版〕

単元:
#化学#化学基礎2ー物質の変化#中和と塩#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
化学基礎 2022年版
中和・中和滴定・塩と液性・弱酸の遊離
0.150mol/Lの酢酸水溶液10.0mLを過不足なく中和するのにある濃度の水酸化ナトリウム水溶液を滴下したところ、15.0mLで中和点に達した。この水酸化ナトリウムの濃度は?
この動画を見る
化学基礎 2022年版
中和・中和滴定・塩と液性・弱酸の遊離
0.150mol/Lの酢酸水溶液10.0mLを過不足なく中和するのにある濃度の水酸化ナトリウム水溶液を滴下したところ、15.0mLで中和点に達した。この水酸化ナトリウムの濃度は?
