 化学基礎2ー物質の変化
化学基礎2ー物質の変化
 化学基礎2ー物質の変化
化学基礎2ー物質の変化
1分で解いてほしい化学計算問題 (77) 電子のやり取りは何molか?

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$MnO_2$と$HCl$から,$MnCl_2$,$Cl_2$,および$H_2O$が生成する反応で,0.25 molの$Cl_2$が生成したとき,$Mn$が受け取る電子は何 molか。
①0.25 ②0.50 ③1.0 ④2.0 ⑤4.0 ⑥6.0
この動画を見る
$MnO_2$と$HCl$から,$MnCl_2$,$Cl_2$,および$H_2O$が生成する反応で,0.25 molの$Cl_2$が生成したとき,$Mn$が受け取る電子は何 molか。
①0.25 ②0.50 ③1.0 ④2.0 ⑤4.0 ⑥6.0
【旧センター試験化学】2019追試 第3問 問5 アルミニウムの溶融塩電解
単元:
#化学#無機#大学入試過去問(化学)#酸化還元反応#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
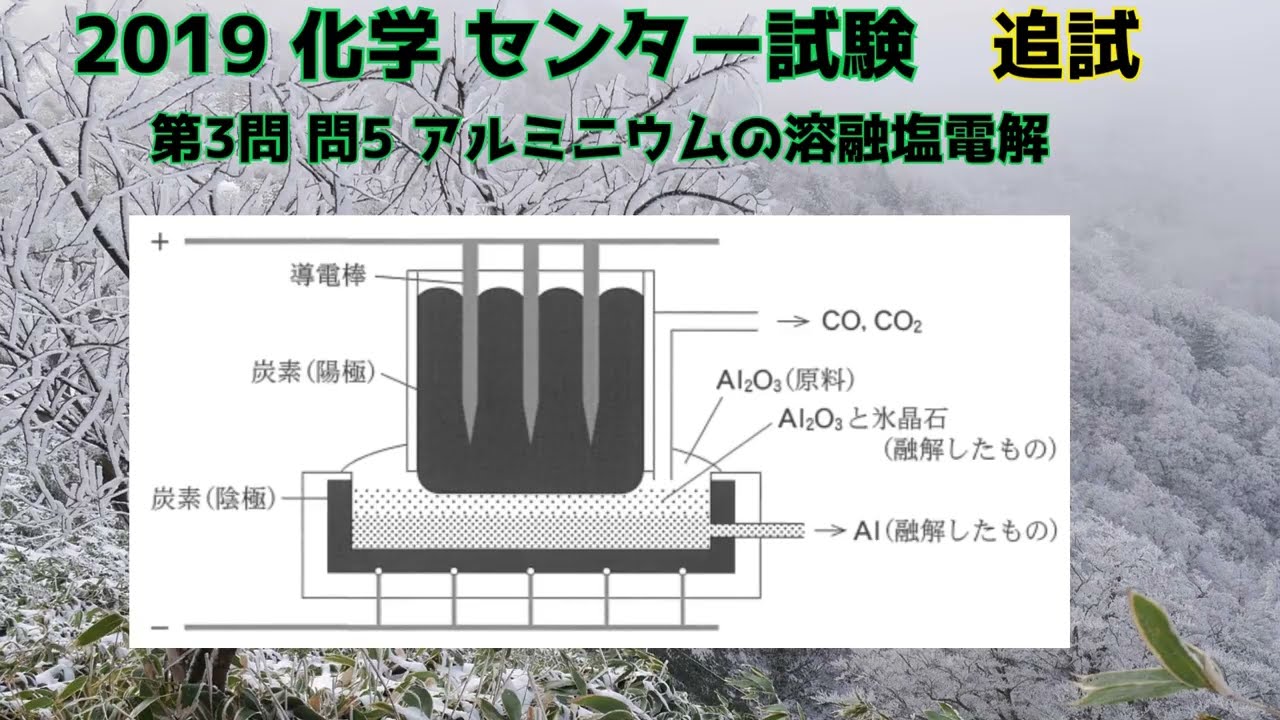
酸化アルミニウムAl₂O₃を原料とした融解塩電解(溶融塩電解)によるアルミニウムAlの製造は,図1のような装置で行われ,陽極の炭素Cは次の反応のいずれかにより酸化される。
C + O²⁻ → CO + 2e⁻
C + 2O²⁻ → CO₂ + 4e⁻
陽極で発生した気体が,CO 14 kgとCO₂ 66 kgの混合気体のとき,陰極側に生成した金属Alの質量は何kgか。最も適当な数値を,下の①~⑥のうちから一つ選べ。ただし,酸化アルミニウムを融解させるために添加された氷晶石の質量は変化せず,反応した酸化アルミニウムに含まれる酸素は,すべて陽極の炭素の酸化に使用されたものとする。
① 18
② 27
③ 32
④ 45
⑤ 54
⑥ 63
この動画を見る
酸化アルミニウムAl₂O₃を原料とした融解塩電解(溶融塩電解)によるアルミニウムAlの製造は,図1のような装置で行われ,陽極の炭素Cは次の反応のいずれかにより酸化される。
C + O²⁻ → CO + 2e⁻
C + 2O²⁻ → CO₂ + 4e⁻
陽極で発生した気体が,CO 14 kgとCO₂ 66 kgの混合気体のとき,陰極側に生成した金属Alの質量は何kgか。最も適当な数値を,下の①~⑥のうちから一つ選べ。ただし,酸化アルミニウムを融解させるために添加された氷晶石の質量は変化せず,反応した酸化アルミニウムに含まれる酸素は,すべて陽極の炭素の酸化に使用されたものとする。
① 18
② 27
③ 32
④ 45
⑤ 54
⑥ 63
理論化学基礎演習24 ¹²C = 12が ¹²C = 120に変更され,120gの¹²Cが1molになったらどうなるか?

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#物質量と濃度
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
仮に,相対質量の基準値を¹²C=12から¹²C=120に変更し,さらに¹²C 1molの質量を12gから120gに変更した場合,
①質量パーセント濃度が1.80%のグルコース水溶液におけるモル凝固点降下
②4.00g/Lの水溶液のpH
それぞれどうなるか。以下の選択肢から選びなさい。(変更前のNaOHの式量は40)
100倍になる,10倍になる,1増加する,1減少する,10分の1になる,100分の1になる
この動画を見る
仮に,相対質量の基準値を¹²C=12から¹²C=120に変更し,さらに¹²C 1molの質量を12gから120gに変更した場合,
①質量パーセント濃度が1.80%のグルコース水溶液におけるモル凝固点降下
②4.00g/Lの水溶液のpH
それぞれどうなるか。以下の選択肢から選びなさい。(変更前のNaOHの式量は40)
100倍になる,10倍になる,1増加する,1減少する,10分の1になる,100分の1になる
1分で解いてほしい化学計算問題 (73) 分子の数

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
1gに含まれる分子の数が最も多い物質を選びなさい。
(原子量 H 1 C 12 N 14 O 16 Ne 20 Cl 35.5 アボガドロ定数 6.0×10²³ /mol)
①塩素 ②酸素 ③窒素 ④二酸化炭素
⑤水 ⑥アンモニア ⑦ネオン ⑧メタン
この動画を見る
1gに含まれる分子の数が最も多い物質を選びなさい。
(原子量 H 1 C 12 N 14 O 16 Ne 20 Cl 35.5 アボガドロ定数 6.0×10²³ /mol)
①塩素 ②酸素 ③窒素 ④二酸化炭素
⑤水 ⑥アンモニア ⑦ネオン ⑧メタン
1分で解いてほしい化学計算問題 (65) メタンの燃焼

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#化学変化と化学反応式
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
メタンCH4を完全燃焼させたところ、18gの水H₂Oが生成した。このとき、生成した二酸化炭素CO2は何gか。最も適当な数値を、次の①~⑤ のうちから一つ選べ。(原子量H1C120 16)
① 9.0② 22 ③33 ④44 ⑤88
この動画を見る
メタンCH4を完全燃焼させたところ、18gの水H₂Oが生成した。このとき、生成した二酸化炭素CO2は何gか。最も適当な数値を、次の①~⑤ のうちから一つ選べ。(原子量H1C120 16)
① 9.0② 22 ③33 ④44 ⑤88
【最も質問の多い問題!!】ヘスの法則と反応エンタルピーの演習〔現役講師解説、高校化学、化学基礎、新課程版〕

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#化学結合#化学変化と化学反応式#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
ヘスの法則と反応エンタルピーに関して解説していきます。
この動画を見る
ヘスの法則と反応エンタルピーに関して解説していきます。
複雑な化学式を語呂で覚える'(ミョウバン・高度さらし粉・さらし粉)#化学 #化学基礎 #授業

単元:
#化学#化学基礎1ー物質の構成#化学基礎2ー物質の変化#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
複雑な化学式の語呂での覚え方を解説していきます。
'(ミョウバン・高度さらし粉・さらし粉)
この動画を見る
複雑な化学式の語呂での覚え方を解説していきます。
'(ミョウバン・高度さらし粉・さらし粉)
理論化学第29回 蒸気圧降下・沸点上昇・凝固点降下

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
希薄溶液の性質
・蒸気圧降下
・沸点上昇
・凝固点降下
【蒸気圧降下】
気液平衡状態において、気体になっている分子が衝突することで生じる圧力→蒸気圧
蒸気圧降下:溶媒の蒸発による濃度上昇を溶質が妨害することで起こる
同じ$100\,\rm{℃}$の水蒸気でも蒸気圧が純溶媒のときよりわずかに小さい。
氷になっている部分は溶媒ではない。
この動画を見る
希薄溶液の性質
・蒸気圧降下
・沸点上昇
・凝固点降下
【蒸気圧降下】
気液平衡状態において、気体になっている分子が衝突することで生じる圧力→蒸気圧
蒸気圧降下:溶媒の蒸発による濃度上昇を溶質が妨害することで起こる
同じ$100\,\rm{℃}$の水蒸気でも蒸気圧が純溶媒のときよりわずかに小さい。
氷になっている部分は溶媒ではない。
2024追試第4問 問4b ステアリン酸単分子膜
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
b シクロヘキサンに溶かしたステアリン
酸$\ce{CH3 (CH2)16COOH}$(分子量$284$) を水面に滴下すると、
溶液が水面上に広がる。
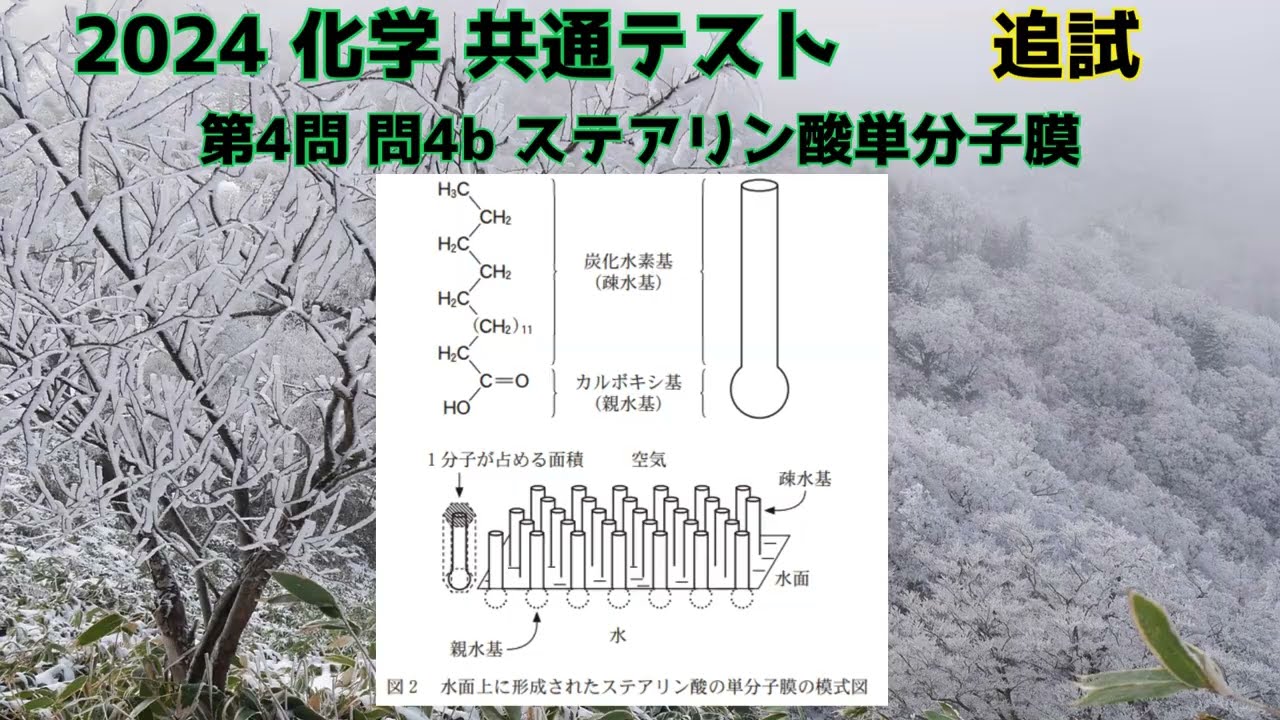
シクロヘキサンが十分に揮発すると、図2に示すように、
ステアリン酸分子は親水性のカルボキシ基を水 中に向け、
疎水性の炭化水素基を空気側に向けた状態で単分子膜を形成する。
濃度$0.568\,\rm{g/L}$のステアリン酸のシクロヘキサン溶液$0.100\,\rm{mL}$を水面に 滴下した、シクロヘキサンが十分に揮発した後、
単分子膜の面積は$252\rm{cm^2} $であった。
ステアリン酸分子が水面をすき間なく覆っているとすると、ステ アリン酸1分子が水面上で占める面積の平均値は何$\rm{cm^2}$か。
最も適当な数 値を、後の①~⑥のうちから一つ選べ。
ただし、アボガドロ定数を $6.0 \times 10^{23}\,\rm{/mol}$とする。
①$2.1 \times 10^{-15}$
②$2.3 \times 10^{-15}$
③$2.4 \times 10^{-15}$
④$4.2 \times 10^{-15}$
⑤$6.8 \times 10^{-15}$
⑥$7.6 \times 10^{-15}$
※図は動画内参照
この動画を見る
b シクロヘキサンに溶かしたステアリン
酸$\ce{CH3 (CH2)16COOH}$(分子量$284$) を水面に滴下すると、
溶液が水面上に広がる。
シクロヘキサンが十分に揮発すると、図2に示すように、
ステアリン酸分子は親水性のカルボキシ基を水 中に向け、
疎水性の炭化水素基を空気側に向けた状態で単分子膜を形成する。
濃度$0.568\,\rm{g/L}$のステアリン酸のシクロヘキサン溶液$0.100\,\rm{mL}$を水面に 滴下した、シクロヘキサンが十分に揮発した後、
単分子膜の面積は$252\rm{cm^2} $であった。
ステアリン酸分子が水面をすき間なく覆っているとすると、ステ アリン酸1分子が水面上で占める面積の平均値は何$\rm{cm^2}$か。
最も適当な数 値を、後の①~⑥のうちから一つ選べ。
ただし、アボガドロ定数を $6.0 \times 10^{23}\,\rm{/mol}$とする。
①$2.1 \times 10^{-15}$
②$2.3 \times 10^{-15}$
③$2.4 \times 10^{-15}$
④$4.2 \times 10^{-15}$
⑤$6.8 \times 10^{-15}$
⑥$7.6 \times 10^{-15}$
※図は動画内参照
2024追試第4問 問4 界面活性剤

単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
界面活性剤の性質に関する記述として下線部に誤りを含むものはどれか。 最も適当なものを、次の①~④のうちから一つ選べ。
① セッケンは水の表面張力を低下させるはたらきをするため、セッケン水 は繊維の内部に浸透することができる。
② セッケンの洗浄力は、硬水中でも低下しない。
③ 陽イオン界面活性剤は洗浄力は弱いが、頭髪用コンディショナー(リンス)などに含まれており、帯電防止効果や柔軟効果を与える。
④ 界面活性剤の乳化作用により、油分をミセル内部に取り込んだ微粒子を 水中に分散させた乳濁液を得ることができ、乳化作用は食品や化粧品など に利用される。
この動画を見る
界面活性剤の性質に関する記述として下線部に誤りを含むものはどれか。 最も適当なものを、次の①~④のうちから一つ選べ。
① セッケンは水の表面張力を低下させるはたらきをするため、セッケン水 は繊維の内部に浸透することができる。
② セッケンの洗浄力は、硬水中でも低下しない。
③ 陽イオン界面活性剤は洗浄力は弱いが、頭髪用コンディショナー(リンス)などに含まれており、帯電防止効果や柔軟効果を与える。
④ 界面活性剤の乳化作用により、油分をミセル内部に取り込んだ微粒子を 水中に分散させた乳濁液を得ることができ、乳化作用は食品や化粧品など に利用される。
理論化学第28回 質量モル濃度

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
質量モル濃度$[\rm{mol/kg}]$
→㎏=溶媒
$1\,\rm{kg}$の溶媒に溶けている物質量。
SはSolvent(溶媒)の頭文字
$\displaystyle \frac{n\,[\rm{mol}]}{S\,[\rm{kg}]}=m\,[\rm{mol/kg}]$
$n\,[\mathrm{mol}]=m\,[\mathrm{mol/kg}] \times S\,[\rm{kg}]$
$1\,\rm{kg}=1000\,\rm{g}$のスモール$s$だった場合式は、
$ m\,[\mathrm{mol/kg}] \times \frac{s}{1000}\,[\rm{kg}]$
になる。
molの公式は$n\,[\rm{mol}]=$の形で覚えよう!
【例題を計算しよう。】
尿素$\ce{(NH2)2CO}~6.0\,\rm{g}$を水$200\,\rm{g}$に溶かした場合
$30$%硫酸$(1.2\,\rm{g/cm^3})$のモル濃度・質量を求めよ。
この動画を見る
質量モル濃度$[\rm{mol/kg}]$
→㎏=溶媒
$1\,\rm{kg}$の溶媒に溶けている物質量。
SはSolvent(溶媒)の頭文字
$\displaystyle \frac{n\,[\rm{mol}]}{S\,[\rm{kg}]}=m\,[\rm{mol/kg}]$
$n\,[\mathrm{mol}]=m\,[\mathrm{mol/kg}] \times S\,[\rm{kg}]$
$1\,\rm{kg}=1000\,\rm{g}$のスモール$s$だった場合式は、
$ m\,[\mathrm{mol/kg}] \times \frac{s}{1000}\,[\rm{kg}]$
になる。
molの公式は$n\,[\rm{mol}]=$の形で覚えよう!
【例題を計算しよう。】
尿素$\ce{(NH2)2CO}~6.0\,\rm{g}$を水$200\,\rm{g}$に溶かした場合
$30$%硫酸$(1.2\,\rm{g/cm^3})$のモル濃度・質量を求めよ。
2024追試第3問 問3b いわゆる逆滴定の操作方法
単元:
#化学#化学基礎2ー物質の変化#大学入試過去問(化学)#共通テスト#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
実験II 結果Iに基づき、
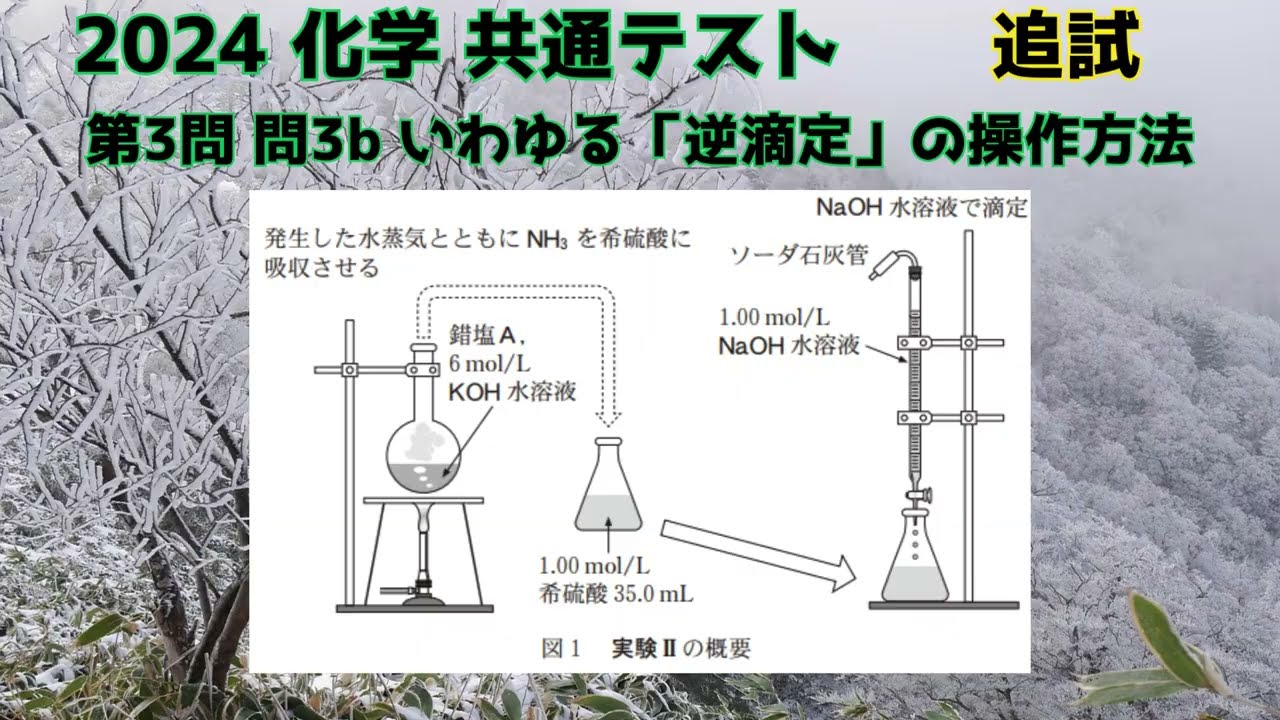
$\ce{Co^{3+}}$ を $0.0100\,\rm{mol} $含む$A$をはかり取り、丸底フラ スコに入れ、図1に示すように、$A$中から$\ce{NH3}$を完全に発生させるために十分な体積の$6\,\rm{mol/L} $水酸化カリウム$\ce{KOH}$水溶液を加えて煮沸した。
このとき、発生した水蒸気とともに$\ce{NH3}$を$1.00\,\rm{mol/L}$の希硫酸$ 35.0\,\rm{mL}$にすべて吸収させた。
$\ce{NH3}$を吸収した希硫酸に適切な指示薬$B$を加え、$1.00\,\rm{mol/L}$ の水酸化ナトリウム $\ce{NaOH}$水溶液を使って滴定した。結果 指示薬$B$の変色には$20.00\,\rm{mL}$の$\ce{NaOH}$水溶液が必要であった。
実験までは、$A$が分解されて発生した$\ce{NH3}$を過剰駄の希硫酸に吸収させ、$\ce{NH3}$と反応せずに残った硫酸を$\ce{NaOH}$水溶液により中和滴定することで、発生した$\ce{NH3}$の物質量を求めている。実験目に関する記述として誤りを含むものはどれか、最も適当なものを、次の①~④のうちから一つ選べ。
① $\ce{NH3}$を吸収させる者続能を入れる三月フラスコは、現浄して純水ですすいだ後に、ぬれたまま用いてもよい。
②$\ce{NaOH}$水容液による中和演定で、残った破能と$\ce{NaOH}$が遊不足なく反応した時点では、木容後は中性となる。
③ $\ce{NaOH}$ 水溶液による中和演定では、指示第日としてメチルオレンジを用いる。
③ この清定に用いるビュレットの上部にソーダ管を取り付けているのは、$\ce{NaOH}$ 水浴液が大気中の$\ce{CO2}$を吸収するのを防ぐためである。
※図は動画内参照
この動画を見る
実験II 結果Iに基づき、
$\ce{Co^{3+}}$ を $0.0100\,\rm{mol} $含む$A$をはかり取り、丸底フラ スコに入れ、図1に示すように、$A$中から$\ce{NH3}$を完全に発生させるために十分な体積の$6\,\rm{mol/L} $水酸化カリウム$\ce{KOH}$水溶液を加えて煮沸した。
このとき、発生した水蒸気とともに$\ce{NH3}$を$1.00\,\rm{mol/L}$の希硫酸$ 35.0\,\rm{mL}$にすべて吸収させた。
$\ce{NH3}$を吸収した希硫酸に適切な指示薬$B$を加え、$1.00\,\rm{mol/L}$ の水酸化ナトリウム $\ce{NaOH}$水溶液を使って滴定した。結果 指示薬$B$の変色には$20.00\,\rm{mL}$の$\ce{NaOH}$水溶液が必要であった。
実験までは、$A$が分解されて発生した$\ce{NH3}$を過剰駄の希硫酸に吸収させ、$\ce{NH3}$と反応せずに残った硫酸を$\ce{NaOH}$水溶液により中和滴定することで、発生した$\ce{NH3}$の物質量を求めている。実験目に関する記述として誤りを含むものはどれか、最も適当なものを、次の①~④のうちから一つ選べ。
① $\ce{NH3}$を吸収させる者続能を入れる三月フラスコは、現浄して純水ですすいだ後に、ぬれたまま用いてもよい。
②$\ce{NaOH}$水容液による中和演定で、残った破能と$\ce{NaOH}$が遊不足なく反応した時点では、木容後は中性となる。
③ $\ce{NaOH}$ 水溶液による中和演定では、指示第日としてメチルオレンジを用いる。
③ この清定に用いるビュレットの上部にソーダ管を取り付けているのは、$\ce{NaOH}$ 水浴液が大気中の$\ce{CO2}$を吸収するのを防ぐためである。
※図は動画内参照
強酸・強塩基の覚え方

理論化学第27回 溶液の濃度(質量パーセント濃度とモル濃度の復習)

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
・質量パーセント濃度
・モル濃度$(\rm{mol/L})$
・質量モル濃度$(\rm{mol/kg})$
【例題を求めてみよう】
$100\,\rm{g}$の水に$25\,\rm{g}$の$\ce{NaCl}$を溶かした。
何%か?
溶液$1\,\rm{L}$中に溶ける溶質の物質量は$(\rm{mol})$
$2.0\,\rm{g}$の$\ce{NaOH}$を水に溶かし、$200\,\rm{mL}$の水溶液をつくった。
$0.100\,\rm{mol/L}$ シュウ酸を$100\,\rm{mL}$つくる。
$\ce{(COOH)_2・2H2O}$は何$\rm{g}$必要?
この動画を見る
・質量パーセント濃度
・モル濃度$(\rm{mol/L})$
・質量モル濃度$(\rm{mol/kg})$
【例題を求めてみよう】
$100\,\rm{g}$の水に$25\,\rm{g}$の$\ce{NaCl}$を溶かした。
何%か?
溶液$1\,\rm{L}$中に溶ける溶質の物質量は$(\rm{mol})$
$2.0\,\rm{g}$の$\ce{NaOH}$を水に溶かし、$200\,\rm{mL}$の水溶液をつくった。
$0.100\,\rm{mol/L}$ シュウ酸を$100\,\rm{mL}$つくる。
$\ce{(COOH)_2・2H2O}$は何$\rm{g}$必要?
2024追試第1問 問1 塩の知識問題

単元:
#物理#化学#大学入試過去問(物理)#化学基礎2ー物質の変化#中和と塩#理科(高校生)#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
次の記述ア・イの両方に当てはまる塩はどれか。
最も適当なものを、後の ①~④のうちから一つ選べ。
ア 水溶液は塩基性を示す。
イ 二重結合をもたない。
① 塩化アンモニウム
② 硫化ナトリウム
③ 乳酸ナトリウム
④ 塩化カルシウム
この動画を見る
次の記述ア・イの両方に当てはまる塩はどれか。
最も適当なものを、後の ①~④のうちから一つ選べ。
ア 水溶液は塩基性を示す。
イ 二重結合をもたない。
① 塩化アンモニウム
② 硫化ナトリウム
③ 乳酸ナトリウム
④ 塩化カルシウム
理論化学基礎演習10 アンモニアと緩衝液のpH

単元:
#化学#化学基礎2ー物質の変化#酸と塩基・水素イオン濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$5.0×10^{-2} \,\rm{mol/L}$のアンモニア水の$\rm{pH}$が$11.0$であった。
水のイオン積 $K_w$ を$1.0 \times 10^{14} \,(\rm{mol/L})^2$ としたとき、次の問いに答えなさい。
$5.0 \times 1.0^{-2}\,\rm{mol/L}$のアンモニア水$150\,\rm{mL}$ に塩化アンモニウム(ア) $\rm{g}$を加えてよく混ぜ、さらに水を加えて全量を$500\,\rm{mL}$にしたところ、この水溶液の$\rm{pH}$は$10.0$であった。
(ア)はいくらか。
最も近い数値を$a~f$から選びなさい。
ただし、塩化アンモニウムの式量は$53.5$とする。
$a 1.8 x10 ^{-2}$
$b 2.7 x10 ^{-2}$
$c 5.4 x 10^{-2}$
$d 6.0 x 10^{-2}$
$e 7.5 x 10^{-2}$
$f 8.0 x 10^{-2}$
この動画を見る
$5.0×10^{-2} \,\rm{mol/L}$のアンモニア水の$\rm{pH}$が$11.0$であった。
水のイオン積 $K_w$ を$1.0 \times 10^{14} \,(\rm{mol/L})^2$ としたとき、次の問いに答えなさい。
$5.0 \times 1.0^{-2}\,\rm{mol/L}$のアンモニア水$150\,\rm{mL}$ に塩化アンモニウム(ア) $\rm{g}$を加えてよく混ぜ、さらに水を加えて全量を$500\,\rm{mL}$にしたところ、この水溶液の$\rm{pH}$は$10.0$であった。
(ア)はいくらか。
最も近い数値を$a~f$から選びなさい。
ただし、塩化アンモニウムの式量は$53.5$とする。
$a 1.8 x10 ^{-2}$
$b 2.7 x10 ^{-2}$
$c 5.4 x 10^{-2}$
$d 6.0 x 10^{-2}$
$e 7.5 x 10^{-2}$
$f 8.0 x 10^{-2}$
【高校化学】酸化還元反応が苦手な原因とその対策

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
【高校化学】酸化還元反応が苦手な原因とその対策
酸化還元反応
陰性→17族 F>0>N>....>H
・酸化数(-)陰性が強い方
この動画を見る
【高校化学】酸化還元反応が苦手な原因とその対策
酸化還元反応
陰性→17族 F>0>N>....>H
・酸化数(-)陰性が強い方
1分で復習するモル計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
銅原子$Cu$ $3.0\times10^24$個は何$mol?$
この動画を見る
銅原子$Cu$ $3.0\times10^24$個は何$mol?$
無機化学基礎演習9 イオン化傾向と金属の反応

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
無機化学基礎演習9 イオン化傾向と金属の反応
それぞれ異なる金属A~Eは、カリウム、銅、亜鉛、銀、スズのいずれかである。
これらの金属について、次のような実験結果(ア)~(カ)を得た。
この結果をもとに金属A~Eを特定せよ。
(ア) Aは常温の水と反応して水素を発生したが、他の金属では発生しなかった。
(イ) Bは希塩酸には溶けなかったが、熱濃硫酸には溶解した。
(ウ) BとCを電極として希硫酸に入れて電池をつくるとCが負極となった。
(エ) Dのイオンを含む水溶液にBを入れ、Dが析出した。
(オ) Dは希塩酸には溶けなかったが、濃硝酸には溶解した。
(カ) 表面にCをめっきした鉄板とEをめっきした鉄板を比較すると、表面に傷をつけた場合、Eを っきしたほうが鉄の腐食が速くなった。
この動画を見る
無機化学基礎演習9 イオン化傾向と金属の反応
それぞれ異なる金属A~Eは、カリウム、銅、亜鉛、銀、スズのいずれかである。
これらの金属について、次のような実験結果(ア)~(カ)を得た。
この結果をもとに金属A~Eを特定せよ。
(ア) Aは常温の水と反応して水素を発生したが、他の金属では発生しなかった。
(イ) Bは希塩酸には溶けなかったが、熱濃硫酸には溶解した。
(ウ) BとCを電極として希硫酸に入れて電池をつくるとCが負極となった。
(エ) Dのイオンを含む水溶液にBを入れ、Dが析出した。
(オ) Dは希塩酸には溶けなかったが、濃硝酸には溶解した。
(カ) 表面にCをめっきした鉄板とEをめっきした鉄板を比較すると、表面に傷をつけた場合、Eを っきしたほうが鉄の腐食が速くなった。
理論化学基礎演習9 水酸化マグネシウム水溶液のpH

単元:
#化学#化学基礎2ー物質の変化#酸と塩基・水素イオン濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
水に溶けた水酸化マグネシウム$Mg(OH)_2$はすべて電離するものとし、$25℃$の溶解度積は$Kps=18 \times 10^{-22}(mol/L)^3$である。
水酸化マグネシウム飽和水溶液の水素イオン濃度$[mol/L]$を
有効数2桁で求め、$pH$はどの間にあるかを①~⑤のうちから選びなさい。
水イオン積:$Kw=1.0 \times 10^{-14}(mol/L)^2$
①8以上9未満
②9以上10未満
③10以上11未満
④11以上12未満
⑤12以上13未満
$^3\sqrt{ 2 }=1.3,^3\sqrt{ 18 }=2.6$
この動画を見る
水に溶けた水酸化マグネシウム$Mg(OH)_2$はすべて電離するものとし、$25℃$の溶解度積は$Kps=18 \times 10^{-22}(mol/L)^3$である。
水酸化マグネシウム飽和水溶液の水素イオン濃度$[mol/L]$を
有効数2桁で求め、$pH$はどの間にあるかを①~⑤のうちから選びなさい。
水イオン積:$Kw=1.0 \times 10^{-14}(mol/L)^2$
①8以上9未満
②9以上10未満
③10以上11未満
④11以上12未満
⑤12以上13未満
$^3\sqrt{ 2 }=1.3,^3\sqrt{ 18 }=2.6$
イオン化エネルギーと電子親和力の違いとイメージ

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
イオン化エネルギーと電子親和力の違いとイメージ解説動画です
この動画を見る
イオン化エネルギーと電子親和力の違いとイメージ解説動画です
理論化学基礎演習4 質量モル濃度の計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
問題:塩化カルシウム水和物$CaCl_2$・$2H_2O$ $14.7g$を水$1000g$に溶かした水溶液と同じ凝固点を示す。
塩化$NaCI$水溶液を水$1000g$を用いて作るとき、必要な塩化ナトリウムの質量$[g]$の値を有効数字3桁で求めなさい。
ただし、電解質は完全に電離するものとする。
(原子量H10 16 Na 23 CI 35.5 Ca 40)
この動画を見る
問題:塩化カルシウム水和物$CaCl_2$・$2H_2O$ $14.7g$を水$1000g$に溶かした水溶液と同じ凝固点を示す。
塩化$NaCI$水溶液を水$1000g$を用いて作るとき、必要な塩化ナトリウムの質量$[g]$の値を有効数字3桁で求めなさい。
ただし、電解質は完全に電離するものとする。
(原子量H10 16 Na 23 CI 35.5 Ca 40)
理論化学基礎演習2 濃度の計算

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$20℃$で塩化ナトリウムを水に溶かし、飽和水溶液を$100g$用意した。
この塩化ナトリウム溶液の質量パーセント濃度、モル濃度,質量モル濃度の値を有効数字$2$桁で単位とともにそれぞれ答えなさい。
塩化ナトリウムの溶解度は、$20℃$で$36g$/$100g$水とする。
また、$20℃$での飽和水溶液の密度を$1.2g/cm^3$とする。
(塩化の式量は$58.5$)
この動画を見る
$20℃$で塩化ナトリウムを水に溶かし、飽和水溶液を$100g$用意した。
この塩化ナトリウム溶液の質量パーセント濃度、モル濃度,質量モル濃度の値を有効数字$2$桁で単位とともにそれぞれ答えなさい。
塩化ナトリウムの溶解度は、$20℃$で$36g$/$100g$水とする。
また、$20℃$での飽和水溶液の密度を$1.2g/cm^3$とする。
(塩化の式量は$58.5$)
化学反応式のこれ知ってた?

原子量の求め方〔現役塾講師解説、高校化学、化学基礎〕

【化学】古い過去問 センター試験2008年度 第3問 問6 気体の発生反応

単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#酸と塩基・水素イオン濃度#化学変化と化学反応式#中和と塩#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
下線の化合物$1mol$がすべて反応したとき、発生する気体が最も少ないものを、次の①~⑤のうちから一つ選べ。
①硫化鉄$FeS$に希硫酸を加える。
②塩素酸カリウム$KCIO_3$に、触媒である酸化マンガン(Ⅳ)を加えて加熱する。
③過酸化水素$H_2O_2$の水溶液を、触媒である酸化マンガン(Ⅳ)を加える。
④炭酸水素ナトリウム$NaHCO_3$に希塩酸を加える。
⑤亜硫酸ナトリウム$NaHSO_3$に希塩酸を加える。
この動画を見る
下線の化合物$1mol$がすべて反応したとき、発生する気体が最も少ないものを、次の①~⑤のうちから一つ選べ。
①硫化鉄$FeS$に希硫酸を加える。
②塩素酸カリウム$KCIO_3$に、触媒である酸化マンガン(Ⅳ)を加えて加熱する。
③過酸化水素$H_2O_2$の水溶液を、触媒である酸化マンガン(Ⅳ)を加える。
④炭酸水素ナトリウム$NaHCO_3$に希塩酸を加える。
⑤亜硫酸ナトリウム$NaHSO_3$に希塩酸を加える。
1分で解いてほしい化学計算問題 (58) 塩素発生の反応

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
[2021年 関西大学(改)]
$MnO_2 26.1g$と12mol/Lの濃塩酸200mLとの反応が十分に進行したとき、
理論上得られる$Cl_2$の$0℃,1.013×10^5Pa$での体積は何$L$になるか有効数字3桁で求めなさい。
(モル体積$22.4L/mol MnO_2$の式量$87$)
この動画を見る
[2021年 関西大学(改)]
$MnO_2 26.1g$と12mol/Lの濃塩酸200mLとの反応が十分に進行したとき、
理論上得られる$Cl_2$の$0℃,1.013×10^5Pa$での体積は何$L$になるか有効数字3桁で求めなさい。
(モル体積$22.4L/mol MnO_2$の式量$87$)
1分で解いてほしい化学計算問題 (56) 気体の平均分子量

単元:
#化学#化学基礎2ー物質の変化#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$1.0mol/L$の水酸化ナトリウム水溶液$100mL$の作り方として正しいものはどれか。
①~⑤から1つ選び、番号で答えなさい。
($NaOH$の式量$40$)
① 水酸化ナトリウムの結晶$4.0g$を$100mL$の水に溶かす。
② 水酸化ナトリウムの結晶$4.0g$を水に溶かして$100mL$にする。
③ 水酸化ナトリウムの結晶$4.0g$を$96.0mL$の水に溶かす。
④ 水酸化ナトリウムの結晶$4.0g$を$96.0g$の水に溶かす。
⑤ 水酸化ナトリウムの結晶$4.0g$を水$100g$に溶かす。
この動画を見る
$1.0mol/L$の水酸化ナトリウム水溶液$100mL$の作り方として正しいものはどれか。
①~⑤から1つ選び、番号で答えなさい。
($NaOH$の式量$40$)
① 水酸化ナトリウムの結晶$4.0g$を$100mL$の水に溶かす。
② 水酸化ナトリウムの結晶$4.0g$を水に溶かして$100mL$にする。
③ 水酸化ナトリウムの結晶$4.0g$を$96.0mL$の水に溶かす。
④ 水酸化ナトリウムの結晶$4.0g$を$96.0g$の水に溶かす。
⑤ 水酸化ナトリウムの結晶$4.0g$を水$100g$に溶かす。
共通テスト(旧センター試験)過去問解説 化学 2017年追試 第3問 問6
単元:
#化学#化学基礎2ー物質の変化#物質量と濃度#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
硫酸銅(Ⅱ)と硫化水素との反応を調べるため、
次の操作Ⅰ・Ⅱを行った。
操作1 $10$本の試験管$A~J$に、$10$種類の異なる濃度の硫酸銅(II)水溶液をそれぞれ10mL採取した。
表1に、各試験管中の硫酸銅(II)の濃度を示した。
$0.05mol/L$の硫化水素水を調製し、上記の各試験管に$10ml$ずつ加え、よくかき混ぜたところ、沈殿が生じた。
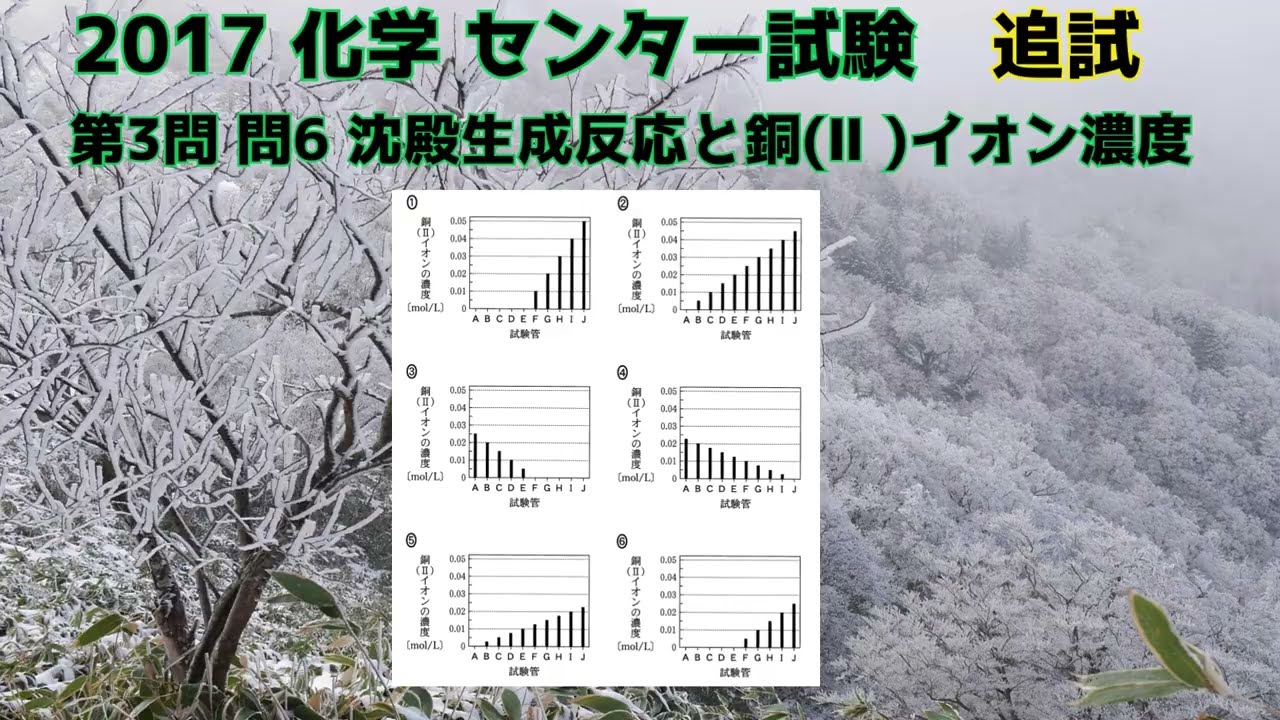
この沈殿生成反応が完了した後、各試験管の水溶液中に沈殿せずに残っている銅(Ⅱ)イオンの濃度を求めた。
このとき、水溶液中の銅(Ⅱ) イオンの濃度を表すグラフとして最も適当なものを、次ページの①~⑥のうちから一つ選べ。
ただし、グラフの棒が表示されていない場合は、銅(II)イオンが検出されなかったことを示している。
※表・グラフは動画内参照
この動画を見る
硫酸銅(Ⅱ)と硫化水素との反応を調べるため、
次の操作Ⅰ・Ⅱを行った。
操作1 $10$本の試験管$A~J$に、$10$種類の異なる濃度の硫酸銅(II)水溶液をそれぞれ10mL採取した。
表1に、各試験管中の硫酸銅(II)の濃度を示した。
$0.05mol/L$の硫化水素水を調製し、上記の各試験管に$10ml$ずつ加え、よくかき混ぜたところ、沈殿が生じた。
この沈殿生成反応が完了した後、各試験管の水溶液中に沈殿せずに残っている銅(Ⅱ)イオンの濃度を求めた。
このとき、水溶液中の銅(Ⅱ) イオンの濃度を表すグラフとして最も適当なものを、次ページの①~⑥のうちから一つ選べ。
ただし、グラフの棒が表示されていない場合は、銅(II)イオンが検出されなかったことを示している。
※表・グラフは動画内参照
共通テスト(旧センター試験)過去問解説 化学 2017年追試 第3問 問5

単元:
#化学#化学基礎2ー物質の変化#化学変化と化学反応式#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
大気中に長期間放置した$Al$粉末の表面では、$Al$が酸化されて$Al_2O_3$が生成していた。
この粉末 $3.61g$を希塩酸に加え、十分にかき混ぜてすべて溶
解させたところ、水素が$0.195 mol$発生した。
この粉末中の物質量の比
$Al: Al_2O_3$として最も適当なものを、次の①~⑥のうちから一つ選べ。
①$3.6:1$
②$13:1$
③$36:1$
④$102:1$
⑤$130:1$
⑥$360:1$
この動画を見る
大気中に長期間放置した$Al$粉末の表面では、$Al$が酸化されて$Al_2O_3$が生成していた。
この粉末 $3.61g$を希塩酸に加え、十分にかき混ぜてすべて溶
解させたところ、水素が$0.195 mol$発生した。
この粉末中の物質量の比
$Al: Al_2O_3$として最も適当なものを、次の①~⑥のうちから一つ選べ。
①$3.6:1$
②$13:1$
③$36:1$
④$102:1$
⑤$130:1$
⑥$360:1$
