 理科(高校生)
理科(高校生)
 理科(高校生)
理科(高校生)
【旧センター試験化学】2019追試 第1問 問6 コロイドの生成実験

単元:
#化学#大学入試過去問(化学)#センター試験
指導講師:
問題文全文(内容文):
センター試験 2019 追試 第1問 問6
塩化鉄(Ⅲ)水溶液を沸騰水に加えて水酸化鉄(Ⅲ)のコロイド溶液を生成させた。このコロイド溶液をセロハンの袋に入れ,図1に示すように純水中で透析した後,次の実験Ⅰ・Ⅱを行った。これらの実験に関する記述として誤りを含むものを,次の①~④のうちから一つ選べ。
実験Ⅰ
(1) 透析後のコロイド溶液を3 mlずつ試験管A・Bにとった。
(2) Aに0.1 mol/Lの$Na_2SO_4$水溶液を加えると,沈殿が生じた。
(3) Bに0.2 mol/Lの$NaCl$水溶液を少量加えても,変化が生じなかった。
実験Ⅱ
(1) 透析後のビーカーに残った水を3 mlずつ試験管C・Dにとった。
(2) Cに硝酸銀水溶液を加えると,白濁した。
(3) DにBTB(ブロモチモールブルー)溶液を加えると,黄色に変色した。
①実験Ⅰより,このコロイド粒子は負に帯電していることがわかる。
②実験Ⅰより,$Na_2SO_4$水溶液の代わりに0.1 mol/Lの$K_2SO_4$水溶液を少量加えても,沈殿が生じることがわかる。
③実験Ⅱより,透析により塩化物イオンがセロハンを通過したことがわかる。
④実験Ⅱより,透析により水素イオンがセロハンを通過したことがわかる。
この動画を見る
センター試験 2019 追試 第1問 問6
塩化鉄(Ⅲ)水溶液を沸騰水に加えて水酸化鉄(Ⅲ)のコロイド溶液を生成させた。このコロイド溶液をセロハンの袋に入れ,図1に示すように純水中で透析した後,次の実験Ⅰ・Ⅱを行った。これらの実験に関する記述として誤りを含むものを,次の①~④のうちから一つ選べ。
実験Ⅰ
(1) 透析後のコロイド溶液を3 mlずつ試験管A・Bにとった。
(2) Aに0.1 mol/Lの$Na_2SO_4$水溶液を加えると,沈殿が生じた。
(3) Bに0.2 mol/Lの$NaCl$水溶液を少量加えても,変化が生じなかった。
実験Ⅱ
(1) 透析後のビーカーに残った水を3 mlずつ試験管C・Dにとった。
(2) Cに硝酸銀水溶液を加えると,白濁した。
(3) DにBTB(ブロモチモールブルー)溶液を加えると,黄色に変色した。
①実験Ⅰより,このコロイド粒子は負に帯電していることがわかる。
②実験Ⅰより,$Na_2SO_4$水溶液の代わりに0.1 mol/Lの$K_2SO_4$水溶液を少量加えても,沈殿が生じることがわかる。
③実験Ⅱより,透析により塩化物イオンがセロハンを通過したことがわかる。
④実験Ⅱより,透析により水素イオンがセロハンを通過したことがわかる。
【高校化学】けん化価とヨウ素価【毎週土曜日16時更新!】

単元:
#化学#有機#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
油脂1gのけん化に要する水酸化カリウムの質量[mg]をけん化価といい,油脂 100g に付加するヨウ素の質量[g] をヨウ素価という。
次の各問いに答えよ。 ただし, KOH の式量を56, I2 の分子量を254とする。
(1) 油脂Xのけん化価は190であった。油脂Xの分子量を有効数字3桁で答えよ。
(2)油脂Xのヨウ素価が86.2であるとき,油脂Xの分子内には,いくつの炭素-炭素二重結合が含まれているか。 ただし, 油脂Xの分子内には,炭素-炭素三重結合は含まれていないものとする。
この動画を見る
油脂1gのけん化に要する水酸化カリウムの質量[mg]をけん化価といい,油脂 100g に付加するヨウ素の質量[g] をヨウ素価という。
次の各問いに答えよ。 ただし, KOH の式量を56, I2 の分子量を254とする。
(1) 油脂Xのけん化価は190であった。油脂Xの分子量を有効数字3桁で答えよ。
(2)油脂Xのヨウ素価が86.2であるとき,油脂Xの分子内には,いくつの炭素-炭素二重結合が含まれているか。 ただし, 油脂Xの分子内には,炭素-炭素三重結合は含まれていないものとする。
【高校物理】単振動とエネルギー【毎週土曜日16時更新!】

単元:
#物理#力学#理科(高校生)
教材:
#中高教材#セミナー物理基礎・物理
指導講師:
理数個別チャンネル
問題文全文(内容文):
質量5.0kgの物体が、周期4.0s、振幅2.0mの単振動をしている。この単振動について、次の各間に答えよ。
(1)角振動数は何 rad/s か。
(2)振動数は何 Hzか。
(3)変位が1.0mの点で、物体が受ける復元力の大きさは何か。
(4)物体が受ける復元力の大きさの最大値は何Nか。
(5)単振動のエネルギーは何Jか。
この動画を見る
質量5.0kgの物体が、周期4.0s、振幅2.0mの単振動をしている。この単振動について、次の各間に答えよ。
(1)角振動数は何 rad/s か。
(2)振動数は何 Hzか。
(3)変位が1.0mの点で、物体が受ける復元力の大きさは何か。
(4)物体が受ける復元力の大きさの最大値は何Nか。
(5)単振動のエネルギーは何Jか。
【旧センター試験化学】2020追試 第1問 問2 メタンハイドレート

単元:
#化学#化学理論#大学入試過去問(化学)#気体の性質#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
センター試験化学 2020追試 第1問 問2
メタン$CH_4$は,定温・高圧下で水分子がつくる網目状構造に取り込まれて固体物質を形成する。この固体物質はメタンハイドレートと呼ばれ,$CH_4$と$H_2O$の質量比が16:104であることが知られている。
メタンハイドレート1.20 gのみが入っている容積1.0 Lの密閉容器を,27 ℃で静置したところ,メタンハイドレートは$CH_4$(気),$H_2O$(気),$H_2O$(液)となった。このとき,容器内の気体の全圧は何 Paか。最も適当な数値を,次の①~⑤のうちから一つ選べ。ただし,気体定数は$R=8.3 × 10^3 Pa・L/(K・mol)$であり,27 ℃における水蒸気圧は$3.6 × 10^3 Pa$である。また,$H_2O$(液)の体積,$H_2O$(液)への$CH_4$(気)の溶解は無視できるものとする。
① $3.6 × 10^3$ ② $2.5 × 10^4$ ③ $2.9 × 10^4$
④ $1.4 × 10^5$ ⑤ $1.7 × 10^5$
この動画を見る
センター試験化学 2020追試 第1問 問2
メタン$CH_4$は,定温・高圧下で水分子がつくる網目状構造に取り込まれて固体物質を形成する。この固体物質はメタンハイドレートと呼ばれ,$CH_4$と$H_2O$の質量比が16:104であることが知られている。
メタンハイドレート1.20 gのみが入っている容積1.0 Lの密閉容器を,27 ℃で静置したところ,メタンハイドレートは$CH_4$(気),$H_2O$(気),$H_2O$(液)となった。このとき,容器内の気体の全圧は何 Paか。最も適当な数値を,次の①~⑤のうちから一つ選べ。ただし,気体定数は$R=8.3 × 10^3 Pa・L/(K・mol)$であり,27 ℃における水蒸気圧は$3.6 × 10^3 Pa$である。また,$H_2O$(液)の体積,$H_2O$(液)への$CH_4$(気)の溶解は無視できるものとする。
① $3.6 × 10^3$ ② $2.5 × 10^4$ ③ $2.9 × 10^4$
④ $1.4 × 10^5$ ⑤ $1.7 × 10^5$
【旧センター試験化学】2020追試 第1問 問1 イオンの総電子数

単元:
#化学#大学入試過去問(化学)#原子の構成と元素の周期表#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
センター試験化学2020追試 第1問 問1
イオン1個に含まれる電子の総数が最も多いものを,次の①~④のうちから一つ選べ。ただし,塩素,カリウム,銅の原子番号はそれぞれ17,19,29である。
① $CO_3^{2-}$ ② $ClO^-$ ③ $Cu^{2+}$ ④ $K^+$
この動画を見る
センター試験化学2020追試 第1問 問1
イオン1個に含まれる電子の総数が最も多いものを,次の①~④のうちから一つ選べ。ただし,塩素,カリウム,銅の原子番号はそれぞれ17,19,29である。
① $CO_3^{2-}$ ② $ClO^-$ ③ $Cu^{2+}$ ④ $K^+$
理論化学基礎演習31 汗はどれだけ体温を下げるのか?

単元:
#化学#化学理論#大学入試過去問(化学)#物質の変化と熱・光#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2024 崇城大学
汗が蒸発するときに周囲から奪った熱が,$1.1 × 10^3 kJ$であった。37 ℃の水50 kgから$1.1 × 10^3 kJ$の熱量が奪われたとき,水50 kgは冷却されて理論上何 ℃となるか。水1.0 gの温度を1.0 K上げるのに必要な熱量を4.2 Jとし,温度に依存しないとする。
この動画を見る
2024 崇城大学
汗が蒸発するときに周囲から奪った熱が,$1.1 × 10^3 kJ$であった。37 ℃の水50 kgから$1.1 × 10^3 kJ$の熱量が奪われたとき,水50 kgは冷却されて理論上何 ℃となるか。水1.0 gの温度を1.0 K上げるのに必要な熱量を4.2 Jとし,温度に依存しないとする。
1分で解いてほしい化学計算問題 (77) 電子のやり取りは何molか?

単元:
#化学#化学基礎2ー物質の変化#酸化還元反応#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$MnO_2$と$HCl$から,$MnCl_2$,$Cl_2$,および$H_2O$が生成する反応で,0.25 molの$Cl_2$が生成したとき,$Mn$が受け取る電子は何 molか。
①0.25 ②0.50 ③1.0 ④2.0 ⑤4.0 ⑥6.0
この動画を見る
$MnO_2$と$HCl$から,$MnCl_2$,$Cl_2$,および$H_2O$が生成する反応で,0.25 molの$Cl_2$が生成したとき,$Mn$が受け取る電子は何 molか。
①0.25 ②0.50 ③1.0 ④2.0 ⑤4.0 ⑥6.0
【旧センター試験化学】2019追試 第7問 問2 DNAに含まれる水素結合の数を数えよう!

単元:
#化学#大学入試過去問(化学)#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
センター試験化学 2019年追試 第7問 問2
DNAは,2本のポリヌクレオチド鎖が塩基の間で水素結合をつくり,二重らせん構造を形成している。DNAのヌクレオチド中の塩基には,図1(図は動画参照)に示すア~エの4種類があり,塩基の$N$原子に結合している$H$原子($NーH$)と,異なる塩基の$N$原子あるいは$O$原子との間で,$NーH\cdots O$
この動画を見る
センター試験化学 2019年追試 第7問 問2
DNAは,2本のポリヌクレオチド鎖が塩基の間で水素結合をつくり,二重らせん構造を形成している。DNAのヌクレオチド中の塩基には,図1(図は動画参照)に示すア~エの4種類があり,塩基の$N$原子に結合している$H$原子($NーH$)と,異なる塩基の$N$原子あるいは$O$原子との間で,$NーH\cdots O$
有機化学基礎演習(24) アルキンの構造決定問題

単元:
#化学#有機#有機化合物の特徴と構造#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
炭素原子間の三重結合を1つもつ化合物B102mgを完全燃焼させたところ,二酸化炭素330mgおよび水108mgが得られた。化合物Bに触媒を用いて水を付加させたところ,2種類の安定な化合物CおよびDが得られた。化合物CおよびDについて,それぞれをアンモニア性硝酸銀水溶液に加えて加熱したところ,どちらの化合物も反応しなかった。また,化合物CおよびDを還元したところ,化合物Cからは不斉炭素原子をもつ化合物E,化合物Dからは不斉炭素原子をもたない化合物Fが得られた。化合物B~Fの分子量はすべて100未満であり,化合物EおよびFはヒドロキシ基をもっていた。
・化合物Bの分子式を記せ。
・化合物CおよびDの構造式をならって記せ。
・ヨードホルム反応を示す化合物を,化合物C~Fの中からすべて選び,記号で答えよ。ヨードホルム反応を示す化合物がなければ「なし」と記せ。
この動画を見る
炭素原子間の三重結合を1つもつ化合物B102mgを完全燃焼させたところ,二酸化炭素330mgおよび水108mgが得られた。化合物Bに触媒を用いて水を付加させたところ,2種類の安定な化合物CおよびDが得られた。化合物CおよびDについて,それぞれをアンモニア性硝酸銀水溶液に加えて加熱したところ,どちらの化合物も反応しなかった。また,化合物CおよびDを還元したところ,化合物Cからは不斉炭素原子をもつ化合物E,化合物Dからは不斉炭素原子をもたない化合物Fが得られた。化合物B~Fの分子量はすべて100未満であり,化合物EおよびFはヒドロキシ基をもっていた。
・化合物Bの分子式を記せ。
・化合物CおよびDの構造式をならって記せ。
・ヨードホルム反応を示す化合物を,化合物C~Fの中からすべて選び,記号で答えよ。ヨードホルム反応を示す化合物がなければ「なし」と記せ。
【高校化学】エステルの異性体【毎週土曜日16時更新!】

単元:
#化学#理科(高校生)
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
次の文中の( )に適当な数値を入れよ。
分子式 C₅H₁₀O₂をもつ化合物のうち,エステルに分類されるものは(ア)種類存在し,それらのうち不斉炭素原子をもつものは(イ)種類である。
これらの構造異性体を加水分解して生じるカルボン酸およびアルコールの種類は,構造異性体を含めて数えると,それぞれ(ウ)種類および(エ)種類である。
生じたカルボン酸のうち, アンモニア性硝酸銀水溶液と反応して銀を析出するものは(オ)種類である。
また,生じたアルコールのうち, ヨードホルム反応を示すものは(カ)種類,酸化剤によってケトンを与えるものは(キ)種類である。
この動画を見る
次の文中の( )に適当な数値を入れよ。
分子式 C₅H₁₀O₂をもつ化合物のうち,エステルに分類されるものは(ア)種類存在し,それらのうち不斉炭素原子をもつものは(イ)種類である。
これらの構造異性体を加水分解して生じるカルボン酸およびアルコールの種類は,構造異性体を含めて数えると,それぞれ(ウ)種類および(エ)種類である。
生じたカルボン酸のうち, アンモニア性硝酸銀水溶液と反応して銀を析出するものは(オ)種類である。
また,生じたアルコールのうち, ヨードホルム反応を示すものは(カ)種類,酸化剤によってケトンを与えるものは(キ)種類である。
【高校物理】水平ばね振り子【毎週土曜日16時更新!】

単元:
#物理#力学#理科(高校生)
教材:
#中高教材#セミナー物理基礎・物理
指導講師:
理数個別チャンネル
問題文全文(内容文):
図のように、ばね定数kの軽いばねをなめらかで水平な台上に置き、一端を壁につけ、他端には質量mの物体をつなぐ。点Oから左向きに距離Aはなれ
た点Pまでばねを縮め、手をはなすと、物体は点Oを中心とするPQ間で単振動をした。
(1) 点Pで手をはなしたとき、物体にはたらく水平方向の力の大きさはいくらか。
(2)物体がPQ間で単振動をしているとき、点Oでの物体の速さはいくらか。
(3) 点Qでの物体の加速度を求めよ。
(4) 物体が、点Pから点Oまで進むのにかかる時間はいくらか。
(5) 物体が点Qに達した瞬間、物体とばねとの接続が外れた。その後、物体はどのような連動をするか。簡潔に説明せよ。
この動画を見る
図のように、ばね定数kの軽いばねをなめらかで水平な台上に置き、一端を壁につけ、他端には質量mの物体をつなぐ。点Oから左向きに距離Aはなれ
た点Pまでばねを縮め、手をはなすと、物体は点Oを中心とするPQ間で単振動をした。
(1) 点Pで手をはなしたとき、物体にはたらく水平方向の力の大きさはいくらか。
(2)物体がPQ間で単振動をしているとき、点Oでの物体の速さはいくらか。
(3) 点Qでの物体の加速度を求めよ。
(4) 物体が、点Pから点Oまで進むのにかかる時間はいくらか。
(5) 物体が点Qに達した瞬間、物体とばねとの接続が外れた。その後、物体はどのような連動をするか。簡潔に説明せよ。
理論化学基礎演習30 純水や塩酸に溶けるAgClの量

単元:
#化学#大学入試過去問(化学)#理科(高校生)#昭和薬科大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2021 昭和薬科大学(改)
AgClの式量 $143.5 Ksp 1.8×10^-10 (mol/L)^2$
それぞれ有効数字2桁で答えよ。
(1)純粋な水1.0 Lに対してAgClは何 g溶解するか。ただし,$\sqrt{1.8}=1.3$とする。
(2)0.10 mol/Lの硫酸1.0 Lに対してAgClは何 g溶解するか。ただし,溶解するAgClの濃度は塩酸の濃度に比べて十分に小さく,AgClの溶解により水溶液の体積は変化しないものとする。
この動画を見る
2021 昭和薬科大学(改)
AgClの式量 $143.5 Ksp 1.8×10^-10 (mol/L)^2$
それぞれ有効数字2桁で答えよ。
(1)純粋な水1.0 Lに対してAgClは何 g溶解するか。ただし,$\sqrt{1.8}=1.3$とする。
(2)0.10 mol/Lの硫酸1.0 Lに対してAgClは何 g溶解するか。ただし,溶解するAgClの濃度は塩酸の濃度に比べて十分に小さく,AgClの溶解により水溶液の体積は変化しないものとする。
【旧センター試験化学】2019追試 第6問 問2 何%加水分解したか?の計算問題
単元:
#化学#化学(高分子)#アミノ酸とタンパク質、核酸
指導講師:
ぺんぎん高校化学問題集
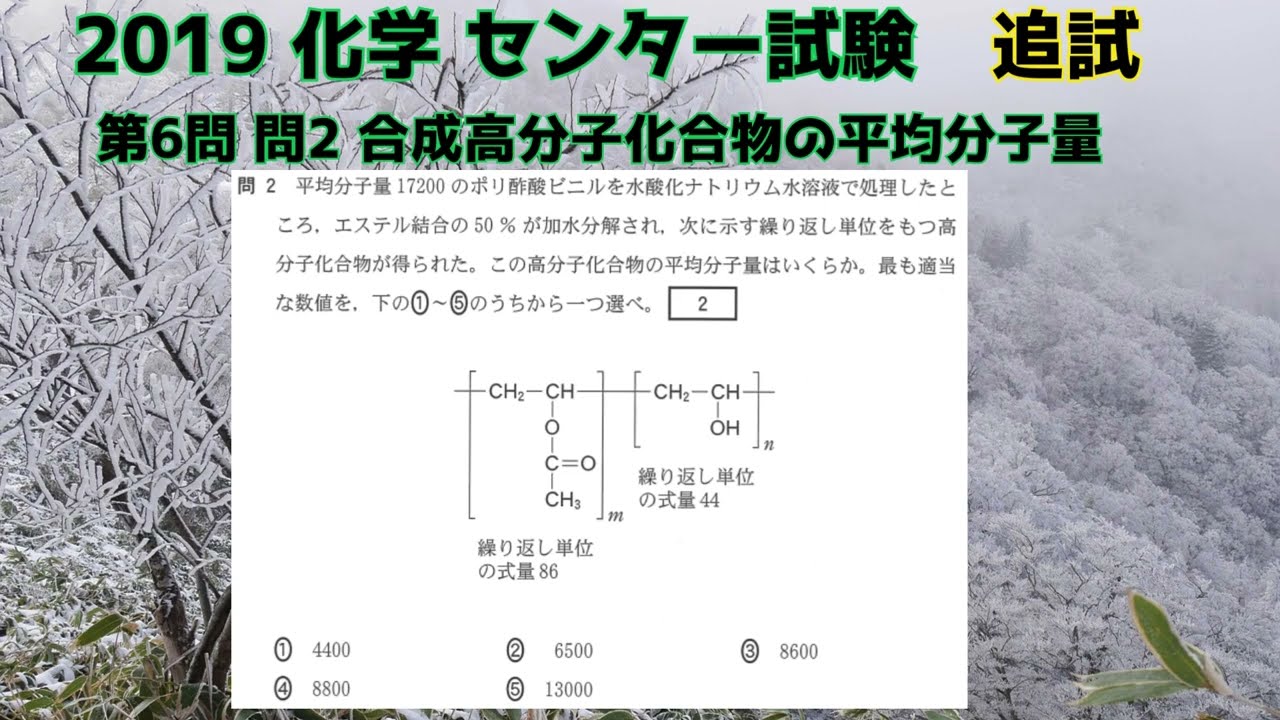
問題文全文(内容文):
平均分子量17200のポリ酢酸ビニルを水酸化ナトリウム水溶液で処理したところ,エステル結合の50%が加水分解され,次に示す繰り返し単位(動画内参照)をもつ高分子化合物が得られた。この高分子化合物の平均分子量はいくらか。最も適当な数値を,下の①~⑤のうちから一つ選べ。
①4400 ②6500 ③8600
④8800 ⑤13000
この動画を見る
平均分子量17200のポリ酢酸ビニルを水酸化ナトリウム水溶液で処理したところ,エステル結合の50%が加水分解され,次に示す繰り返し単位(動画内参照)をもつ高分子化合物が得られた。この高分子化合物の平均分子量はいくらか。最も適当な数値を,下の①~⑤のうちから一つ選べ。
①4400 ②6500 ③8600
④8800 ⑤13000
理論化学基礎演習29 圧力・体積のグラフを温度・体積のグラフに直すとどうなるか?

単元:
#化学#化学理論#気体の性質
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ピストン付きの容器に理想気体を封入した。気体の体積を10cm³,温度を100Kにしたところ,圧力は4×10⁵Paであった。(状態A)。この状態から気体の温度と圧力を調整しながらピストンを動かし,気体の圧力と体積を図1(動画内参照)の実線に沿って,A→B→C→D→Aの順に変化させた。この過程において,気体の温度と体積の変化を示したグラフは①~⑦(動画内参照)のうちどれか。最も適切なものを一つ選べ。
この動画を見る
ピストン付きの容器に理想気体を封入した。気体の体積を10cm³,温度を100Kにしたところ,圧力は4×10⁵Paであった。(状態A)。この状態から気体の温度と圧力を調整しながらピストンを動かし,気体の圧力と体積を図1(動画内参照)の実線に沿って,A→B→C→D→Aの順に変化させた。この過程において,気体の温度と体積の変化を示したグラフは①~⑦(動画内参照)のうちどれか。最も適切なものを一つ選べ。
1分で解いてほしい化学計算問題 (76) SBR中のブタジエンの割合

単元:
#化学#化学(高分子)#合成樹脂とゴム
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
スチレン-ブタジエンゴム50gに,触媒の存在下で水素を反応させたところ,水素0.70molを消費した。反応はブタジエン部分の二重結合だけで起こり,そのすべての二重結合で反応が生じたとすると,このスチレン-ブタジエンゴムのスチレンと1,3-ブタジエンの物質量の比はいくらか。
スチレンを1molとしたとき,1,3-ブタジエンは何molになるかを整数で示せ。
分子量:スチレン 104, ブタジエン 54
この動画を見る
スチレン-ブタジエンゴム50gに,触媒の存在下で水素を反応させたところ,水素0.70molを消費した。反応はブタジエン部分の二重結合だけで起こり,そのすべての二重結合で反応が生じたとすると,このスチレン-ブタジエンゴムのスチレンと1,3-ブタジエンの物質量の比はいくらか。
スチレンを1molとしたとき,1,3-ブタジエンは何molになるかを整数で示せ。
分子量:スチレン 104, ブタジエン 54
【旧センター試験化学】2019追試 第5問 問2 アミノ酸の反応

単元:
#化学#有機#有機化合物の特徴と構造
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
アミノ酸の一つであるアラニンは酸と塩基の両方の性質を示すが,化合物Aをエステル化すると,酸としての性質がなくなる。一方,化合物Bでアセチル化すると,塩基としての性質がなくなる。化合物Aと化合物Bの組合せとして最も適当なものを,下の①~⑥(動画内の表参照)のうちから一つ選べ。
この動画を見る
アミノ酸の一つであるアラニンは酸と塩基の両方の性質を示すが,化合物Aをエステル化すると,酸としての性質がなくなる。一方,化合物Bでアセチル化すると,塩基としての性質がなくなる。化合物Aと化合物Bの組合せとして最も適当なものを,下の①~⑥(動画内の表参照)のうちから一つ選べ。
【旧センター試験化学】2019追試 第5問 問1 高分子化合物

単元:
#化学#化学(高分子)#合成繊維と天然繊維
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
高分子化合物に関する記述として最も適当なものを,次の①~④のうちから一つ選べ。
①ポリプロピレンは,加熱すると軟化し,冷却すると硬くなる。
②紙おむつに用いられる樹脂が高い吸水性を示すのは,エステル結合が加水分解されるためである。
③すべての多糖は,単糖が直線状(鎖状)につながっている。
④アラミド繊維は,付加重合によって得られる。
この動画を見る
高分子化合物に関する記述として最も適当なものを,次の①~④のうちから一つ選べ。
①ポリプロピレンは,加熱すると軟化し,冷却すると硬くなる。
②紙おむつに用いられる樹脂が高い吸水性を示すのは,エステル結合が加水分解されるためである。
③すべての多糖は,単糖が直線状(鎖状)につながっている。
④アラミド繊維は,付加重合によって得られる。
【音声だけで復習!】聞き流し無機化学④〜炭素・ケイ素〜〔現役塾講師解説、高校化学、化学基礎〕

【高校物理】コンデンサーの接続【定期考査直前 特別企画!】【月・木・土 16時新作公開!】

単元:
#物理#電気#理科(高校生)
教材:
#中高教材#セミナー物理基礎・物理
指導講師:
理数個別チャンネル
問題文全文(内容文):
図において、C₁、C₂、C₃ は電気容量がそれぞれ 20µF、30µF、40µF のコンデンサー、E は 20V の電池、S はスイッチである。はじめ、すべてのコンデンサーの電気量は 0 であり、スイッチ S は開いてある。
(1) C₁、C₂ の 2 つの合成容量はいくらか。
(2) C₁、C₂、C₃ の合成容量はいくらか。
(3) スイッチ S を閉じた後、C₁ および C₂ の両端に加わる電圧はそれぞれいくらか。
(4) (3)において、C₁、C₂、C₃ にたくわえられる電気量はそれぞれいくらか。
この動画を見る
図において、C₁、C₂、C₃ は電気容量がそれぞれ 20µF、30µF、40µF のコンデンサー、E は 20V の電池、S はスイッチである。はじめ、すべてのコンデンサーの電気量は 0 であり、スイッチ S は開いてある。
(1) C₁、C₂ の 2 つの合成容量はいくらか。
(2) C₁、C₂、C₃ の合成容量はいくらか。
(3) スイッチ S を閉じた後、C₁ および C₂ の両端に加わる電圧はそれぞれいくらか。
(4) (3)において、C₁、C₂、C₃ にたくわえられる電気量はそれぞれいくらか。
無機化学基礎演習(18) 2族元素の性質

単元:
#化学#無機#典型金属元素の単体と化合物#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2024 愛知工業大学・改
文中の空欄(a)~(m)に当てはまる適切な数字,元素,物質あるいは語句を記せ。
ただし,(a)および(b)については数字を記し,(c)~(g)および(m)については元素記号を記し,また(i)~(l)については化学式を記せ。
周期表2族元素はすべて金属元素で,原子は価電子を(a)個もち,(b)価の陽イオンになりやすい。(c)と(d)は他の2族元素と異なり炎色反応を示さず,それらの単体は常温の水とは反応しない。単体の融点を比較すると,2族元素の単体中では(c)が最も高い。2族元素は,(c),(d)のほか,地殻中に含まれる割合(質量%)の最も大きい(e)と,(f),(g),Raでありアルカリ土類金属とよばれる。
(e)の炭酸塩は,(h)石や大理石の主成分である。
(e)の炭酸塩を強熱すると,熱分解し(i)を生じる。
(e)の炭酸塩と炭素(コークス)を混合して2000℃以上で加熱すると,(j)が得られる。(j)に水を作用させると可燃性の気体である(k)が発生する。(e)の酸化物(無水物)は凍結防止剤(融雪剤)などに利用されている。また,(f)の塩化物の水溶液に希硫酸または硫酸塩の水溶液を加えて生じる白色沈殿(l)は水に難溶で安定な物質であり,胃や腸のX線投影の造影剤に用いられる。(g)の硫酸塩も水に難溶である。これらの2族元素以外では,(m)の2価の陽イオンも硫酸イオンと反応して水に難溶な硫酸塩を生じる。
この動画を見る
2024 愛知工業大学・改
文中の空欄(a)~(m)に当てはまる適切な数字,元素,物質あるいは語句を記せ。
ただし,(a)および(b)については数字を記し,(c)~(g)および(m)については元素記号を記し,また(i)~(l)については化学式を記せ。
周期表2族元素はすべて金属元素で,原子は価電子を(a)個もち,(b)価の陽イオンになりやすい。(c)と(d)は他の2族元素と異なり炎色反応を示さず,それらの単体は常温の水とは反応しない。単体の融点を比較すると,2族元素の単体中では(c)が最も高い。2族元素は,(c),(d)のほか,地殻中に含まれる割合(質量%)の最も大きい(e)と,(f),(g),Raでありアルカリ土類金属とよばれる。
(e)の炭酸塩は,(h)石や大理石の主成分である。
(e)の炭酸塩を強熱すると,熱分解し(i)を生じる。
(e)の炭酸塩と炭素(コークス)を混合して2000℃以上で加熱すると,(j)が得られる。(j)に水を作用させると可燃性の気体である(k)が発生する。(e)の酸化物(無水物)は凍結防止剤(融雪剤)などに利用されている。また,(f)の塩化物の水溶液に希硫酸または硫酸塩の水溶液を加えて生じる白色沈殿(l)は水に難溶で安定な物質であり,胃や腸のX線投影の造影剤に用いられる。(g)の硫酸塩も水に難溶である。これらの2族元素以外では,(m)の2価の陽イオンも硫酸イオンと反応して水に難溶な硫酸塩を生じる。
【音声だけで復習!】聞き流し無機化学③〜窒素・リン〜〔現役塾講師解説、高校化学、化学基礎〕

【高校物理】抵抗率【定期考査直前 特別企画!】【月・木・土 16時新作公開!】

単元:
#物理#電気#理科(高校生)
教材:
#中高教材#セミナー物理基礎・物理
指導講師:
理数個別チャンネル
問題文全文(内容文):
長さ1.0m、断面積 5.0×10⁻⁷m² の円柱状の導体に、12V の電圧を加えると、2.0 Aの電流が流れた。次の各問に答えよ。
(1) 導体の抵抗はいくらか。また、抵抗率はいくらか。
(2) この導体と同じ材質を用いて、長さ 0.50m、断面積 1.0×10⁻⁶m² の導線をつくった。この導線の抵抗はいくらか。
この動画を見る
長さ1.0m、断面積 5.0×10⁻⁷m² の円柱状の導体に、12V の電圧を加えると、2.0 Aの電流が流れた。次の各問に答えよ。
(1) 導体の抵抗はいくらか。また、抵抗率はいくらか。
(2) この導体と同じ材質を用いて、長さ 0.50m、断面積 1.0×10⁻⁶m² の導線をつくった。この導線の抵抗はいくらか。
有機化学基礎演習(23) アルカンの塩素置換

単元:
#化学#有機#大学入試過去問(化学)#有機化合物の特徴と構造#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
関西大学 H 1 C 12 Cl 35.5 空欄を埋めてください。
メタンと塩素の混合気体に光を照射すると,置換反応が起きる。
メタンの1個の水素原子が1個の塩素原子に置き換わる反応は以下の反応式で表される。
{ }
同様の方法でn₌4の直鎖状アルカンの1個の水素原子を
1個の塩素原子で置換すると,立体異性体を区別しなければ,
( )種類の生成物が得られる。いま,n₌4の直鎖状アルカン5.80gを
塩素と混合した後,光を照射した。ここで,このアルカンの1個の
水素原子を1個の塩素原子で置換した生成物と未反応のアルカンの混合物が
7.87g得られたとする。このとき,n₌4の直鎖状アルカンの[ ]%が
反応したと計算できる。
この動画を見る
関西大学 H 1 C 12 Cl 35.5 空欄を埋めてください。
メタンと塩素の混合気体に光を照射すると,置換反応が起きる。
メタンの1個の水素原子が1個の塩素原子に置き換わる反応は以下の反応式で表される。
{ }
同様の方法でn₌4の直鎖状アルカンの1個の水素原子を
1個の塩素原子で置換すると,立体異性体を区別しなければ,
( )種類の生成物が得られる。いま,n₌4の直鎖状アルカン5.80gを
塩素と混合した後,光を照射した。ここで,このアルカンの1個の
水素原子を1個の塩素原子で置換した生成物と未反応のアルカンの混合物が
7.87g得られたとする。このとき,n₌4の直鎖状アルカンの[ ]%が
反応したと計算できる。
1分で解いてほしい化学計算問題 (75) 溶解度曲線

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#麻布大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
硝酸カリウムの個体結晶210gを80℃のみず150gに完全に溶解させて溶液全体が
360gになる硝酸カリウム水溶液を調製した。この溶液の温度を80℃付近から
徐々に低下させると,溶液の温度が何℃より低くなったときに固体の硝酸カリウム
が析出し始めるか。[2024 麻布大学]
(図は動画参照)
この動画を見る
硝酸カリウムの個体結晶210gを80℃のみず150gに完全に溶解させて溶液全体が
360gになる硝酸カリウム水溶液を調製した。この溶液の温度を80℃付近から
徐々に低下させると,溶液の温度が何℃より低くなったときに固体の硝酸カリウム
が析出し始めるか。[2024 麻布大学]
(図は動画参照)
理論化学基礎演習28 生理食塩水と同じ濃度のグルコース溶液を調製するには?

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#昭和薬科大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
(問題)塩化ナトリウム9.0gを水に溶解させ全量1000mLにした食塩水がある。この溶液と
浸透圧が等しいグルコース水溶液を作りたい。18gのグルコースをすべて使う場合,グルコース
水溶液の全量は何mLにすればよいか。以下のうち,最も近い数値を選び,番号を
マークしなさい。ただし,塩化ナトリウムは完全に電離しているものとする。※温度は等しい
(原子量 H 1 C 12 O 16 Na 23 Cl 35.5)
① 163 ② 325 ③ 650 ④ 1580 ⑤ 3240 ⑥ 3600
この動画を見る
(問題)塩化ナトリウム9.0gを水に溶解させ全量1000mLにした食塩水がある。この溶液と
浸透圧が等しいグルコース水溶液を作りたい。18gのグルコースをすべて使う場合,グルコース
水溶液の全量は何mLにすればよいか。以下のうち,最も近い数値を選び,番号を
マークしなさい。ただし,塩化ナトリウムは完全に電離しているものとする。※温度は等しい
(原子量 H 1 C 12 O 16 Na 23 Cl 35.5)
① 163 ② 325 ③ 650 ④ 1580 ⑤ 3240 ⑥ 3600
【高校物理】抵抗の消費電力【定期考査直前 特別企画!】【月・木・土 16時新作公開!】

単元:
#物理#電気#理科(高校生)
教材:
#中高教材#セミナー物理基礎・物理
指導講師:
理数個別チャンネル
問題文全文(内容文):
10Ωの抵抗R₁ , 30Ωの抵抗R₂ がある。次のように接続した場合, 抵抗 R₁ , R₂で消費される電力 P₁ , P₂ , および P₁ と P₂ との比はそれぞれいくらか。
(1) R₁ , R₂ を並列に接続し, 2.0Vの電圧を加えた場合。
(2) R₁ , R₂ を直列に接続し, 2.0Vの電圧を加えた場合。
この動画を見る
10Ωの抵抗R₁ , 30Ωの抵抗R₂ がある。次のように接続した場合, 抵抗 R₁ , R₂で消費される電力 P₁ , P₂ , および P₁ と P₂ との比はそれぞれいくらか。
(1) R₁ , R₂ を並列に接続し, 2.0Vの電圧を加えた場合。
(2) R₁ , R₂ を直列に接続し, 2.0Vの電圧を加えた場合。
【日本最速解答速報】2025年星薬科大学薬学部薬学科(6年制) 学校推薦型選抜 化学 解答速報【化学のタカシー】

単元:
#化学#大学入試過去問(化学)#理科(高校生)#大学入試解答速報#化学#星薬科大学#星薬科大学
指導講師:
理数個別チャンネル
問題文全文(内容文):
こちらの動画は、2024年11月24日(日)に実施された、2025年星薬科大学薬学部薬学科(6年制)学校推薦型選抜の化学解答速報です。
大学の正解発表ではなく、あくまで当チャンネルの講師が独自に解説をしているものですので、万が一内容に間違いがございましたらご容赦ください。
解説者は理数個別指導学院宮崎台校の化学のタカシー先生です。
https://www.youtube.com/playlist?list=PLdLgDY469Qr5qi7Un9JtVHCpSK5u3W5lZ
この動画を見る
こちらの動画は、2024年11月24日(日)に実施された、2025年星薬科大学薬学部薬学科(6年制)学校推薦型選抜の化学解答速報です。
大学の正解発表ではなく、あくまで当チャンネルの講師が独自に解説をしているものですので、万が一内容に間違いがございましたらご容赦ください。
解説者は理数個別指導学院宮崎台校の化学のタカシー先生です。
https://www.youtube.com/playlist?list=PLdLgDY469Qr5qi7Un9JtVHCpSK5u3W5lZ
【旧センター試験化学】2019追試 第4問 問4 C₆H₁₀の構造異性体の数(条件付き)

単元:
#化学#有機#大学入試過去問(化学)#有機化合物の特徴と構造#脂肪族炭化水素#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
分子式がC₆H₁₀である化合物の構造異性体のうち,環状構造を一つだけもち,
その環状構造が五つの炭素原子からなるものはいくつあるか,正しい数を,
次の①~⑥のうちから一つ選べ。ただし,立体異性体は考えないものとする。
① 1 ② 2 ③ 3 ④ 4 ⑤ 5 ⑥ 6
この動画を見る
分子式がC₆H₁₀である化合物の構造異性体のうち,環状構造を一つだけもち,
その環状構造が五つの炭素原子からなるものはいくつあるか,正しい数を,
次の①~⑥のうちから一つ選べ。ただし,立体異性体は考えないものとする。
① 1 ② 2 ③ 3 ④ 4 ⑤ 5 ⑥ 6
【旧センター試験化学】2019追試 第4問 問3 カルボン酸の性質

単元:
#化学#有機#大学入試過去問(化学)#有機化合物の特徴と構造#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
カルボン酸の記述として下線部に誤りを含むものを,次の①~⑤のうちから一つ選べ。
① ギ酸は,還元性を示す。
② リノレン酸 C₁₇H₂₉COOHは,炭素原子間に二重結合を三つもつ。
③ 乳酸 CH₃CH(OH)COOHには,光学異性体(鏡像異性体)が存在する。
④ 高級脂肪酸のナトリウム塩は,油汚れなどを落とすことが出来る。
⑤ ともに示性式C₂H₂(COOH)₂で表されるマレイン酸とフマル酸は,いずれも分子内で脱水して酸無水物をつくることができる。
(下線部は動画参照)
この動画を見る
カルボン酸の記述として下線部に誤りを含むものを,次の①~⑤のうちから一つ選べ。
① ギ酸は,還元性を示す。
② リノレン酸 C₁₇H₂₉COOHは,炭素原子間に二重結合を三つもつ。
③ 乳酸 CH₃CH(OH)COOHには,光学異性体(鏡像異性体)が存在する。
④ 高級脂肪酸のナトリウム塩は,油汚れなどを落とすことが出来る。
⑤ ともに示性式C₂H₂(COOH)₂で表されるマレイン酸とフマル酸は,いずれも分子内で脱水して酸無水物をつくることができる。
(下線部は動画参照)
【高校化学】油脂【毎週土曜日16時更新!】

単元:
#化学#有機
教材:
#中高教材#セミナー化学基礎・化学
指導講師:
理数個別チャンネル
問題文全文(内容文):
次の文中の( )に適当な語句を入れよ。
油脂は、高級脂肪酸と( ア )との( イ )であり、大豆油のように室温で液体のものを( ウ )、牛脂のように室温で固体のものを( エ )という。脂肪酸の不飽和の度合いが( オ )い油脂は室温で液体であり、空気中で酸化されて固体になりやすいので( カ )油とよばれ、塗料などに用いられる。また、ニッケルなどを触媒として、炭素原子間の二重結合に( キ )を付加させると、固体になる。このようにしてつくられた油脂は( ク )油とよばれ、マーガリンなどの原料になる。
この動画を見る
次の文中の( )に適当な語句を入れよ。
油脂は、高級脂肪酸と( ア )との( イ )であり、大豆油のように室温で液体のものを( ウ )、牛脂のように室温で固体のものを( エ )という。脂肪酸の不飽和の度合いが( オ )い油脂は室温で液体であり、空気中で酸化されて固体になりやすいので( カ )油とよばれ、塗料などに用いられる。また、ニッケルなどを触媒として、炭素原子間の二重結合に( キ )を付加させると、固体になる。このようにしてつくられた油脂は( ク )油とよばれ、マーガリンなどの原料になる。
