 溶液の性質
溶液の性質
 溶液の性質
溶液の性質
【旧センター試験化学】2020追試 第4問 問1 セッケンの性質

単元:
#化学#化学理論#有機#溶液の性質#酸素を含む脂肪族化合物
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
セッケンに関する記述として下線部に誤りを含むものを,次の①~⑤のうちから一つ選べ。
①セッケンは,塩基性を示す。
②セッケンは,油脂をけん化することにより得られる。
③セッケンは,水溶液中で集合してミセルをつくるとき,親水基を外側に向ける。
④セッケンは,水に溶かすと水の表面張力を低下させる。
⑤セッケンの洗浄力は,Ca$^{2+}$を多く含む硬水中でも低下しない。
この動画を見る
セッケンに関する記述として下線部に誤りを含むものを,次の①~⑤のうちから一つ選べ。
①セッケンは,塩基性を示す。
②セッケンは,油脂をけん化することにより得られる。
③セッケンは,水溶液中で集合してミセルをつくるとき,親水基を外側に向ける。
④セッケンは,水に溶かすと水の表面張力を低下させる。
⑤セッケンの洗浄力は,Ca$^{2+}$を多く含む硬水中でも低下しない。
【旧センター試験化学】2020追試 第3問 問3 溶解度積の大小関係

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#センター試験
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
銀イオン$Ag^+$と陰イオン$X^-,Y^-$がそれぞれ水溶液中で難溶性の塩$AgX,AgY$を生成するとき,次の反応が進行すれば,$AgY$の水への溶解度積は$AgX$より小さいことがわかる。
$AgX(固) + Y^- aq \to X^- aq + AgY(固)$
このことを用いて,$AgCl,AgI,AgSCN$の溶解度積の大小関係を調べる次の実験Ⅰ~Ⅲを行った。
実験Ⅰ 2本の試験管$A,B$にそれぞれ,$Fe(NO_3)_3$の水溶液をとった。溶液の色は黄褐色であった。
実験Ⅱ 試験管$A$の水溶液に白色の$AgSCN$の固体を加えた。さらに$KI$の水溶液を加え,よく振り交ぜて静置したところ,溶液の色は赤色になり,沈殿の色は黄色であった。
実験Ⅲ 試験管$B$の水溶液に$AgCl$の固体を加えた。さらに$KSCN$の水溶液を加えたところ,溶液の色は赤くなったが,よく振り交ぜて静置したところ,溶液の色は黄褐色になり,沈殿の色は白色であった。
実験Ⅰ~Ⅲから分かる$AgCl,AgI,AgSCN$の溶解度積の大小関係として最も適当なものを,次の①~⑥のうちから一つ選べ。
① $AgCl < AgI < AgSCN$ ② $AgCl < AgI < AgSCN$
③ $AgI < AgSCN < AgCl$ ④ $AgI < AgCl < AgSCN$
⑤ $AgSCN < AgCl < AgI$ ⑥ $AgSCN < AgI < AgCl$
この動画を見る
銀イオン$Ag^+$と陰イオン$X^-,Y^-$がそれぞれ水溶液中で難溶性の塩$AgX,AgY$を生成するとき,次の反応が進行すれば,$AgY$の水への溶解度積は$AgX$より小さいことがわかる。
$AgX(固) + Y^- aq \to X^- aq + AgY(固)$
このことを用いて,$AgCl,AgI,AgSCN$の溶解度積の大小関係を調べる次の実験Ⅰ~Ⅲを行った。
実験Ⅰ 2本の試験管$A,B$にそれぞれ,$Fe(NO_3)_3$の水溶液をとった。溶液の色は黄褐色であった。
実験Ⅱ 試験管$A$の水溶液に白色の$AgSCN$の固体を加えた。さらに$KI$の水溶液を加え,よく振り交ぜて静置したところ,溶液の色は赤色になり,沈殿の色は黄色であった。
実験Ⅲ 試験管$B$の水溶液に$AgCl$の固体を加えた。さらに$KSCN$の水溶液を加えたところ,溶液の色は赤くなったが,よく振り交ぜて静置したところ,溶液の色は黄褐色になり,沈殿の色は白色であった。
実験Ⅰ~Ⅲから分かる$AgCl,AgI,AgSCN$の溶解度積の大小関係として最も適当なものを,次の①~⑥のうちから一つ選べ。
① $AgCl < AgI < AgSCN$ ② $AgCl < AgI < AgSCN$
③ $AgI < AgSCN < AgCl$ ④ $AgI < AgCl < AgSCN$
⑤ $AgSCN < AgCl < AgI$ ⑥ $AgSCN < AgI < AgCl$
1分で解いてほしい化学計算問題 (75) 溶解度曲線

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#麻布大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
硝酸カリウムの個体結晶210gを80℃のみず150gに完全に溶解させて溶液全体が
360gになる硝酸カリウム水溶液を調製した。この溶液の温度を80℃付近から
徐々に低下させると,溶液の温度が何℃より低くなったときに固体の硝酸カリウム
が析出し始めるか。[2024 麻布大学]
(図は動画参照)
この動画を見る
硝酸カリウムの個体結晶210gを80℃のみず150gに完全に溶解させて溶液全体が
360gになる硝酸カリウム水溶液を調製した。この溶液の温度を80℃付近から
徐々に低下させると,溶液の温度が何℃より低くなったときに固体の硝酸カリウム
が析出し始めるか。[2024 麻布大学]
(図は動画参照)
理論化学基礎演習28 生理食塩水と同じ濃度のグルコース溶液を調製するには?

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#昭和薬科大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
(問題)塩化ナトリウム9.0gを水に溶解させ全量1000mLにした食塩水がある。この溶液と
浸透圧が等しいグルコース水溶液を作りたい。18gのグルコースをすべて使う場合,グルコース
水溶液の全量は何mLにすればよいか。以下のうち,最も近い数値を選び,番号を
マークしなさい。ただし,塩化ナトリウムは完全に電離しているものとする。※温度は等しい
(原子量 H 1 C 12 O 16 Na 23 Cl 35.5)
① 163 ② 325 ③ 650 ④ 1580 ⑤ 3240 ⑥ 3600
この動画を見る
(問題)塩化ナトリウム9.0gを水に溶解させ全量1000mLにした食塩水がある。この溶液と
浸透圧が等しいグルコース水溶液を作りたい。18gのグルコースをすべて使う場合,グルコース
水溶液の全量は何mLにすればよいか。以下のうち,最も近い数値を選び,番号を
マークしなさい。ただし,塩化ナトリウムは完全に電離しているものとする。※温度は等しい
(原子量 H 1 C 12 O 16 Na 23 Cl 35.5)
① 163 ② 325 ③ 650 ④ 1580 ⑤ 3240 ⑥ 3600
理論化学第32回 浸透圧の計算基礎

理論化学基礎演習11 酢酸の二分子会合と凝固点降下度

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
2024 愛知教育大学(改) H1 C 12 O 16
酢酸のベンゼン溶液中においては、酢酸分子は電離せず、
また、一部の酢酸分子は水素結合により2分子間で結びつき、
会合体(2量体)を形成する。
それ以外の酢酸分子はベンゼン溶液中で会合せずに単独で存在しており、単独で存在する酢酸分子と形成された2量体の間に、次式のように平衡(これを会合平衡という)が 成り立っている。
$\ce{CH3COOH}⇄\displaystyle \frac{1}{2} \ce{(CH3COOH)2} $
酢酸 $3.00\,\rm{g}$をベンゼン $500\,\rm{g}$に溶かしたベンゼン溶液の凝固点下度$△t$が$0.261\,\rm{K}$であったとき、ベンゼン中に溶かした酢酸分子の何%が2量体を形成したか。
有効数字$2$桁で求めよ。
ただし、このベンゼン溶液中で2量体を形成する酢酸分子の割合は温度に依存しないものとする。
(ベンゼンのモル凝固点降下:$5.12\,\rm{K·kg/mol}$)
この動画を見る
2024 愛知教育大学(改) H1 C 12 O 16
酢酸のベンゼン溶液中においては、酢酸分子は電離せず、
また、一部の酢酸分子は水素結合により2分子間で結びつき、
会合体(2量体)を形成する。
それ以外の酢酸分子はベンゼン溶液中で会合せずに単独で存在しており、単独で存在する酢酸分子と形成された2量体の間に、次式のように平衡(これを会合平衡という)が 成り立っている。
$\ce{CH3COOH}⇄\displaystyle \frac{1}{2} \ce{(CH3COOH)2} $
酢酸 $3.00\,\rm{g}$をベンゼン $500\,\rm{g}$に溶かしたベンゼン溶液の凝固点下度$△t$が$0.261\,\rm{K}$であったとき、ベンゼン中に溶かした酢酸分子の何%が2量体を形成したか。
有効数字$2$桁で求めよ。
ただし、このベンゼン溶液中で2量体を形成する酢酸分子の割合は温度に依存しないものとする。
(ベンゼンのモル凝固点降下:$5.12\,\rm{K·kg/mol}$)
理論化学第26回 ヘンリーの法則をイメージできるようにしよう!

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
・溶解度の小さい気体:ヘンリーの法則
(例)$N_2, 0℃, 1.0 \times 10^{5}Pa$
$1L$に対して$23mL$
$O_2, 0℃, 1.0 \times 10^{5}Pa$
$1L$に対して$49mL$
空気$N_2:O_2$が$4:1$
空気$5.0 \times 10^{5}Pa$で$10L$と接しているとき
溶けていた気体をとりだし、それぞれ$1.0 \times 10^{5}Pa$にするとそれぞれ何Lになるか?
この動画を見る
・溶解度の小さい気体:ヘンリーの法則
(例)$N_2, 0℃, 1.0 \times 10^{5}Pa$
$1L$に対して$23mL$
$O_2, 0℃, 1.0 \times 10^{5}Pa$
$1L$に対して$49mL$
空気$N_2:O_2$が$4:1$
空気$5.0 \times 10^{5}Pa$で$10L$と接しているとき
溶けていた気体をとりだし、それぞれ$1.0 \times 10^{5}Pa$にするとそれぞれ何Lになるか?
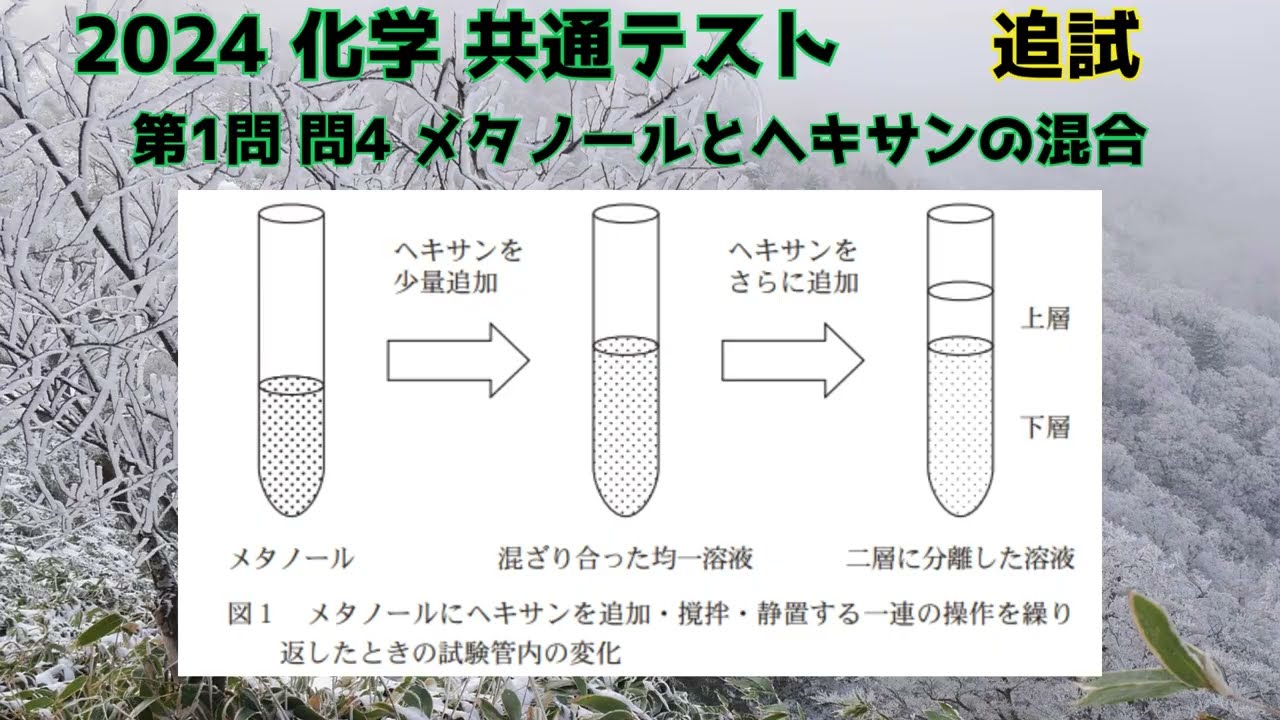
2024追試第1問 問4 メタノールとヘキサンの混合
単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
ヘキサンやメタノールの性質の記述として、誤りを含むものはどれか。
最も適当なものを、次の①~④のうちから一つ選べ。
① ヘキサンは、無極性分子である。
② メタノールは、極性分子である。
③ 室温でヘキサンは、水にほとんど溶けない。
④ 室温で水とメタノールは、混合する割合によっては二層に分離する。
※図は動画内参照
この動画を見る
ヘキサンやメタノールの性質の記述として、誤りを含むものはどれか。
最も適当なものを、次の①~④のうちから一つ選べ。
① ヘキサンは、無極性分子である。
② メタノールは、極性分子である。
③ 室温でヘキサンは、水にほとんど溶けない。
④ 室温で水とメタノールは、混合する割合によっては二層に分離する。
※図は動画内参照
理論化学第25回 溶解度計算② よくあるCuSO₄・5H₂Oの結晶の析出問題を攻略しよう!

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
化学式量 $\ce{CuSO4}:160, \ce{H2O}:18$とする。
$\ce{KNO3}$について
・$60℃$の飽和 $\ce{KNO3}$ 水溶液$100\,\rm{g}$を$15\,\rm{℃}$まで冷却したとき、析出する$\ce{KNO3}$は何$\rm{g}$か。
$\ce{CuSO4}$について
・$80\,\rm{℃}$の水$150\,\rm{g}$に $\ce{CuSO4}$ $30\,\rm{g}$を溶かした水溶液を徐々に冷却していくと、何$\rm{℃}$で結晶が 析出し始めるか。
・$60\,\rm{℃}$の水 $50.0\,\rm{g}$に $\ce{CuSO4}・5\ce{H2O} 25.0\,\rm{g}$を溶かし、
これを$20\,\rm{℃}$まで冷却したとき、 析出する $\ce{CuSO4}・5\ce{H2O}$の結晶は何$\rm{g}$か。
この動画を見る
化学式量 $\ce{CuSO4}:160, \ce{H2O}:18$とする。
$\ce{KNO3}$について
・$60℃$の飽和 $\ce{KNO3}$ 水溶液$100\,\rm{g}$を$15\,\rm{℃}$まで冷却したとき、析出する$\ce{KNO3}$は何$\rm{g}$か。
$\ce{CuSO4}$について
・$80\,\rm{℃}$の水$150\,\rm{g}$に $\ce{CuSO4}$ $30\,\rm{g}$を溶かした水溶液を徐々に冷却していくと、何$\rm{℃}$で結晶が 析出し始めるか。
・$60\,\rm{℃}$の水 $50.0\,\rm{g}$に $\ce{CuSO4}・5\ce{H2O} 25.0\,\rm{g}$を溶かし、
これを$20\,\rm{℃}$まで冷却したとき、 析出する $\ce{CuSO4}・5\ce{H2O}$の結晶は何$\rm{g}$か。
理論化学第24回 溶解度計算①

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
固体の溶解度は,溶媒 $100g$ に溶ける溶質の最大質量〔g〕の数値を用いて表す。
図 1 は,硝酸カリウム $KNO_3$,硫酸銅(II)$CuSO_4$および塩化ナトリウム $NaCl$ の水に対する溶解度曲線である。
この動画を見る
固体の溶解度は,溶媒 $100g$ に溶ける溶質の最大質量〔g〕の数値を用いて表す。
図 1 は,硝酸カリウム $KNO_3$,硫酸銅(II)$CuSO_4$および塩化ナトリウム $NaCl$ の水に対する溶解度曲線である。
理論化学基礎演習7 コロイドと浸透圧

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
塩化鉄(III)(式量162)を0.81g含む水溶液を、沸騰している水に加え、かき混ぜた。
冷却後,水を加えて$100mL$とした。
セロハン膜を使って精製したのち、$27℃$で浸透圧を測定したところ、$600Pa$を示した。
このコロイド粒子1個のなかには、平均で何個の鉄イオンが含まれているか。
最も 近い数値を選びなさい。
ただし、膜での精製過程、コロイド溶液の体積は変わらな
いものとする。(気体定数:$8.3 \times 10^{3}Pa・L/(K・mol))$
①$10$
②$20$
③$50$
④$100$
⑤$200$
⑥$500$
⑦$1000$
⑧$2000$
⑨$5000$
この動画を見る
塩化鉄(III)(式量162)を0.81g含む水溶液を、沸騰している水に加え、かき混ぜた。
冷却後,水を加えて$100mL$とした。
セロハン膜を使って精製したのち、$27℃$で浸透圧を測定したところ、$600Pa$を示した。
このコロイド粒子1個のなかには、平均で何個の鉄イオンが含まれているか。
最も 近い数値を選びなさい。
ただし、膜での精製過程、コロイド溶液の体積は変わらな
いものとする。(気体定数:$8.3 \times 10^{3}Pa・L/(K・mol))$
①$10$
②$20$
③$50$
④$100$
⑤$200$
⑥$500$
⑦$1000$
⑧$2000$
⑨$5000$
理論化学基礎演習6 CuSO₄・5H₂O 硫酸銅(Ⅱ)五水和物の溶解度問題

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$80℃$の硫酸銅(Ⅱ)飽和水溶液$50g 20℃$に冷やしたところ、硫酸銅(Ⅱ)五水和物の結晶が析出した。
設問(1),(2)に答えよ。
ただし、硫酸銅(Ⅱ)の$20℃, 80℃$における溶解度を、それぞれ20,56とする。
また、硫酸銅(Ⅱ)および硫酸銅(Ⅱ)五水和物の式量は、
$160$および$250$とする。
(回答は有効数字2桁)
(1) 80℃の硫酸銅(Ⅱ)飽和水溶液50gに含まれる硫酸銅(Ⅱ)の質量を答えよ。
(2) 析出した硫酸銅(Ⅱ)五水和物の質量を答えよ。
この動画を見る
$80℃$の硫酸銅(Ⅱ)飽和水溶液$50g 20℃$に冷やしたところ、硫酸銅(Ⅱ)五水和物の結晶が析出した。
設問(1),(2)に答えよ。
ただし、硫酸銅(Ⅱ)の$20℃, 80℃$における溶解度を、それぞれ20,56とする。
また、硫酸銅(Ⅱ)および硫酸銅(Ⅱ)五水和物の式量は、
$160$および$250$とする。
(回答は有効数字2桁)
(1) 80℃の硫酸銅(Ⅱ)飽和水溶液50gに含まれる硫酸銅(Ⅱ)の質量を答えよ。
(2) 析出した硫酸銅(Ⅱ)五水和物の質量を答えよ。
理論化学第23回 溶解平衡と溶解度曲線

理論化学第22回 溶解とは?

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
溶解とは?
溶媒・溶質・溶液
$\begin{eqnarray}
\left\{
\begin{array}{l}
極性溶媒 水\\
無極性溶媒 ヘキサンC_6H_{14}
\end{array}
\right.
\end{eqnarray}$
・水に溶けやすいものは?
・ヘキサンに溶けるものは?
※図は動画内参照
この動画を見る
溶解とは?
溶媒・溶質・溶液
$\begin{eqnarray}
\left\{
\begin{array}{l}
極性溶媒 水\\
無極性溶媒 ヘキサンC_6H_{14}
\end{array}
\right.
\end{eqnarray}$
・水に溶けやすいものは?
・ヘキサンに溶けるものは?
※図は動画内参照
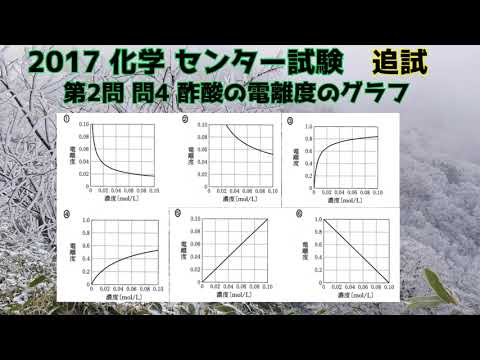
共通テスト(旧センター試験)過去問解説 化学 2017年追試 第2問 問4 酢酸の濃度と電離度の関係
単元:
#化学#化学理論#有機#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
酢酸の$25℃$での電離定数は$2.7\times 10^{-5}mol/L $である。
$25℃$における酢酸水溶液の濃度と電離度の関係を表すグラフとして最も適当なものを、
次の①~⑥のうちから一つ選べ。
※グラフは動画内参照
この動画を見る
酢酸の$25℃$での電離定数は$2.7\times 10^{-5}mol/L $である。
$25℃$における酢酸水溶液の濃度と電離度の関係を表すグラフとして最も適当なものを、
次の①~⑥のうちから一つ選べ。
※グラフは動画内参照
【化学】古い過去問 センター試験2004年度 第2問 問4 硝酸カリウムの溶解度に関する問題

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
図2は、の溶解度(水$100g$に溶ける溶質の最大質量$[g]$の数 値)と温度の関係を示す。
$55g$のを含む$60℃$の飽和水溶液をつくった。
この水溶液の温度を上げて、水の一部を蒸発させたのち、
$20℃$まで冷却したところ、$41g$が析出した。
蒸発した水の質量$[g]$はいくらか。
最も適当な数値を、下の①~⑤のうちから一つ選べ。
①$3$
②$6$
③$9$
④$12$
⑤$14$
※グラフは動画内参照
この動画を見る
図2は、の溶解度(水$100g$に溶ける溶質の最大質量$[g]$の数 値)と温度の関係を示す。
$55g$のを含む$60℃$の飽和水溶液をつくった。
この水溶液の温度を上げて、水の一部を蒸発させたのち、
$20℃$まで冷却したところ、$41g$が析出した。
蒸発した水の質量$[g]$はいくらか。
最も適当な数値を、下の①~⑤のうちから一つ選べ。
①$3$
②$6$
③$9$
④$12$
⑤$14$
※グラフは動画内参照
【化学】古い過去問 センター試験2002年度 第2問 問4 溶解度とモル濃度

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$80℃$で、$100g$の硝酸カリウム$KNO_3$を水$100g$に溶かした。
この溶液を$27℃$まで冷却したところ、硝酸カリウムが析出した。
次の問い(a・b)に答えよ。
ただし、硝酸カリウムは、水$100g$に対して$40g$、$80℃$で$169g$まで溶ける。
a 析出した硝酸カリウムの質量として最も適当な数値を、
次の①~⑤のうち から一つ選べ。
①$100$
②$80$
③$60$
④$40$
⑤$20$
b $27℃$における、この飽和水溶液$10.0ml$の質量は$12.0g$であった。
この溶液のモル濃度として最も適当な数値を、
次の①~⑤のうちから一つ選べ。
ただし、硝酸カリウムの式量は$101$である。
①$34$
②$29$
③$4.8$
④$4.1$
⑤$3.4$
この動画を見る
$80℃$で、$100g$の硝酸カリウム$KNO_3$を水$100g$に溶かした。
この溶液を$27℃$まで冷却したところ、硝酸カリウムが析出した。
次の問い(a・b)に答えよ。
ただし、硝酸カリウムは、水$100g$に対して$40g$、$80℃$で$169g$まで溶ける。
a 析出した硝酸カリウムの質量として最も適当な数値を、
次の①~⑤のうち から一つ選べ。
①$100$
②$80$
③$60$
④$40$
⑤$20$
b $27℃$における、この飽和水溶液$10.0ml$の質量は$12.0g$であった。
この溶液のモル濃度として最も適当な数値を、
次の①~⑤のうちから一つ選べ。
ただし、硝酸カリウムの式量は$101$である。
①$34$
②$29$
③$4.8$
④$4.1$
⑤$3.4$
【星薬科大学(薬)】令和5年度一般選抜試験(B方式) 溶解度積の計算

単元:
#化学理論#大学入試過去問(化学)#溶液の性質#理科(高校生)#星薬科大学
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
(問題抜粋)$\sqrt{ 2 }=1.41,\sqrt{ 3 }=1.73,\sqrt{ 5 }=2.24,\sqrt{ 7 }=2.65$とする。
硫酸バリウムの溶解度積は$25℃$の条件で$1.00 \times 10^{-10}(mol/L)^2$であり、
極めて水に溶けにくい。
$1.00L$の水に$1.00 \times 10^{-4}mol$の硫酸バリウムを加えて飽和水溶液を調製し、
さらに$1.00 \times 10^{-5}mol$の硫酸を加え、$25℃$の条件で十分な時間をおいた場合、
溶存するバリウムイオンの濃度は何$mol/L$か。
有効数字2桁で答えなさい。
ただし、硫酸バリウム、 硫酸アンモニウムを加えたことによる溶液の体積変化は無視できるものとし、加えた硫酸はすべて電離したものとする。
この動画を見る
(問題抜粋)$\sqrt{ 2 }=1.41,\sqrt{ 3 }=1.73,\sqrt{ 5 }=2.24,\sqrt{ 7 }=2.65$とする。
硫酸バリウムの溶解度積は$25℃$の条件で$1.00 \times 10^{-10}(mol/L)^2$であり、
極めて水に溶けにくい。
$1.00L$の水に$1.00 \times 10^{-4}mol$の硫酸バリウムを加えて飽和水溶液を調製し、
さらに$1.00 \times 10^{-5}mol$の硫酸を加え、$25℃$の条件で十分な時間をおいた場合、
溶存するバリウムイオンの濃度は何$mol/L$か。
有効数字2桁で答えなさい。
ただし、硫酸バリウム、 硫酸アンモニウムを加えたことによる溶液の体積変化は無視できるものとし、加えた硫酸はすべて電離したものとする。
これなに?
共通テスト(旧センター試験)過去問解説 化学 2016年追試 第1問 問5 気体の溶解(ヘンリーの法則)

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
この動画を見る
$50℃. 1.0×10^5 Pa$で、ある液体$A1.0L$に溶けるヘリウムと酸素の体積は、それぞれ$9.7mL, 48mL$である。
体積比$4:1$のヘリウムと酸素からなる十分な量の混合気体を、$0℃. 1.0×10^5 Pa$のもとで、液体$A1.0L$に十分長い時間接触させた。
このとき液体$A1.0L$に溶解したヘリウムの体積は、$0℃, 1.0 × 10^5 Pa$で何$mL$か。
最も適当な数値を、次の①~⑤のうちから一 つ選べ。
ただし、ヘリウムと酸素の溶解度は互いに影響せず、気体が溶解した後も、混合気体の圧力と組成は変わらないものとする。
また、ヘリウムと酸素は液体$A$と反応しない。
①$1.9$ ②$7.8$ ③$9.7$ ④$39$ ⑤$48$
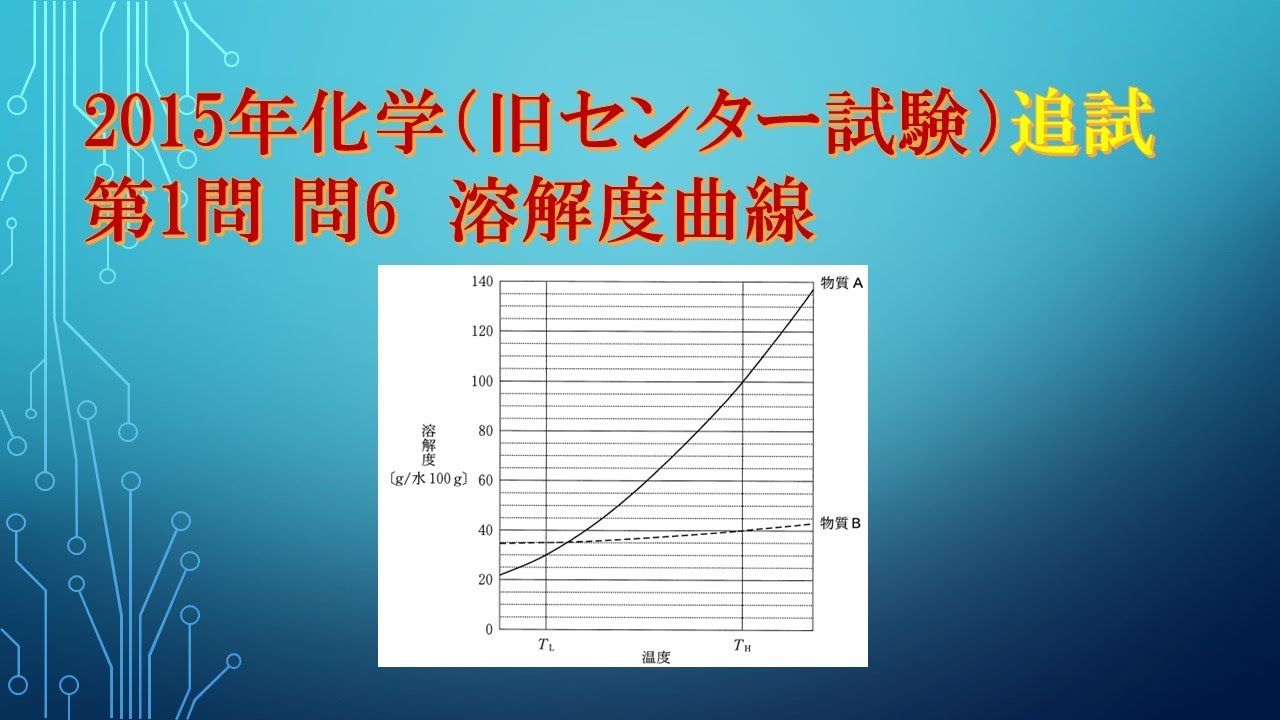
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第1問 問6 溶解度曲線
単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
図1は物質Aと物質Bの溶解度曲線を示している。
Aを140gとBを20g含む混合物を温度$T_H$の水100gに加えて十分にかきまぜた後、温度を$T_H$に保ったままでろ過した。
ろ液を温度$T_L$まで冷却したとき、AとBはそれぞれ何g析出するか。
最も適当な組合せを、下の①~⑥のうちから一つ選べ。
ただし、AとBは互いの溶解度に影響せず、いずれも水和水(結晶水)をもたない物質とする。
※図・表は動画内参照
この動画を見る
図1は物質Aと物質Bの溶解度曲線を示している。
Aを140gとBを20g含む混合物を温度$T_H$の水100gに加えて十分にかきまぜた後、温度を$T_H$に保ったままでろ過した。
ろ液を温度$T_L$まで冷却したとき、AとBはそれぞれ何g析出するか。
最も適当な組合せを、下の①~⑥のうちから一つ選べ。
ただし、AとBは互いの溶解度に影響せず、いずれも水和水(結晶水)をもたない物質とする。
※図・表は動画内参照
【短時間で演習!!】浸透圧の計算問題〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
演習編
浸透圧の計算
Q.スクロース(分子量342)34.2gを水に溶かして1.0Lにした溶液の27℃における浸透圧を求めよ。
この動画を見る
演習編
浸透圧の計算
Q.スクロース(分子量342)34.2gを水に溶かして1.0Lにした溶液の27℃における浸透圧を求めよ。
共通テスト(旧センター試験)過去問解説 化学 2015年追試 第1問 問4 凝固点降下度

単元:
#化学#化学理論#溶液の性質#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
純水1kgに溶質$0.1mol/L$を溶かした水溶液を冷却したとき、
凝固点降下が最も大きくなる溶質を、次の①~⑤のうちから一つ選べ。
ただし、電解質の電離 度は1とする。
① 酢酸ナトリウム
③ 塩化マグネシウム
② 塩化カリウム
④ グリセリン
⑤ グルコース
この動画を見る
純水1kgに溶質$0.1mol/L$を溶かした水溶液を冷却したとき、
凝固点降下が最も大きくなる溶質を、次の①~⑤のうちから一つ選べ。
ただし、電解質の電離 度は1とする。
① 酢酸ナトリウム
③ 塩化マグネシウム
② 塩化カリウム
④ グリセリン
⑤ グルコース
共通テスト追試 化学 2023年度 第5問 問4b 浸透圧による分子量計算

単元:
#化学#化学理論#溶液の性質#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
4 下線部(d)に関する次の問い(a・b)に答えよ。
a 浸透圧 Π に関するファントホッフの法則は,次の式(Ⅰ)のように表すことができる。
$Π = \displaystyle \frac{C_wRT}{M} $
ここで,$C_w$ は質量濃度とよばれ,溶質の質量$w$,溶液の体積 $V$ を用いて
$C_w = \displaystyle \frac{w}{V}$で定義される。
また,$R$ は気体定数,$T$ は絶対温度,$M$ は溶質のモル質量である。
式(1)はスクロースなどの比較的低分子量の非電解質の$M$
の決定に広く用いられている。
$300K,C_w =0.342g/L$のスクロース(分子量 $342$)水溶液の$Π$ は何 $Pa$か。
その数値を有効数字桁の次の形式で表すとき, $\boxed{ 28 } ~\boxed{ 30 } $ に当てはまる数字を,後の①~⓪のうちから一つずつ選べ。
ただし,同じものを繰り返し選んでもよい。
なお,気体定数は $R =8.31×10^3 Pa・L/(K・mol)$とする。
①$1$ ②$2$ ③$3$ ④$4$ ⑤$5$
⑥$6$ ⑦$7$ ⑧$8$ ⑨$9$ ⓪$0$
この動画を見る
4 下線部(d)に関する次の問い(a・b)に答えよ。
a 浸透圧 Π に関するファントホッフの法則は,次の式(Ⅰ)のように表すことができる。
$Π = \displaystyle \frac{C_wRT}{M} $
ここで,$C_w$ は質量濃度とよばれ,溶質の質量$w$,溶液の体積 $V$ を用いて
$C_w = \displaystyle \frac{w}{V}$で定義される。
また,$R$ は気体定数,$T$ は絶対温度,$M$ は溶質のモル質量である。
式(1)はスクロースなどの比較的低分子量の非電解質の$M$
の決定に広く用いられている。
$300K,C_w =0.342g/L$のスクロース(分子量 $342$)水溶液の$Π$ は何 $Pa$か。
その数値を有効数字桁の次の形式で表すとき, $\boxed{ 28 } ~\boxed{ 30 } $ に当てはまる数字を,後の①~⓪のうちから一つずつ選べ。
ただし,同じものを繰り返し選んでもよい。
なお,気体定数は $R =8.31×10^3 Pa・L/(K・mol)$とする。
①$1$ ②$2$ ③$3$ ④$4$ ⑤$5$
⑥$6$ ⑦$7$ ⑧$8$ ⑨$9$ ⓪$0$
【どうして起こるかを理解!!】コロイド(塩析、凝析、チンダル現象、ブラウン運動、電気泳動)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
コロイドについて解説します。
塩析、凝析、チンダル現象、ブラウン運動、電気泳動
この動画を見る
コロイドについて解説します。
塩析、凝析、チンダル現象、ブラウン運動、電気泳動
【違いをしっかり理解!!】希薄溶液の性質(蒸気圧降下・沸点上昇・凝固点降下・浸透圧)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
希薄溶液の性質について解説します。
蒸気圧降下・沸点上昇・凝固点降下・浸透圧
この動画を見る
希薄溶液の性質について解説します。
蒸気圧降下・沸点上昇・凝固点降下・浸透圧
共通テスト追試 化学 2023年度 第1問 問5b 固体の溶解度の問題 最後の罠に気をつけて

単元:
#化学#化学理論#溶液の性質#理科(高校生)#化学#共通テスト
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
図1に示す塩化カリウム$KCI$. 硝酸カリウム$KNO_3$, および硫酸マグネシウ$MgSO_4$の水に対する溶解度曲線を用いて、
固体の溶解および析出に関する後の問い(a・b)に答えよ。
b $MgSO_4$の水溶液を冷却して得られる結晶は、$MgSO_4$の水和物である。
水$100g$に、ある量の$MgSO_4$が溶けている水溶液Aを$14℃$に冷却する。
このとき、析出する$MgSO_4$の水和物の質量が$12.3g$であり、その中の水和水の質量が$6.3g$である場合、冷却前の水溶液Aに溶けている$MgSO_4$の質量は何$g$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$28$ ②$30$ ③$32$ ④$34$ ⑤$36$ ⑥$42$
※図は動画内参照
この動画を見る
図1に示す塩化カリウム$KCI$. 硝酸カリウム$KNO_3$, および硫酸マグネシウ$MgSO_4$の水に対する溶解度曲線を用いて、
固体の溶解および析出に関する後の問い(a・b)に答えよ。
b $MgSO_4$の水溶液を冷却して得られる結晶は、$MgSO_4$の水和物である。
水$100g$に、ある量の$MgSO_4$が溶けている水溶液Aを$14℃$に冷却する。
このとき、析出する$MgSO_4$の水和物の質量が$12.3g$であり、その中の水和水の質量が$6.3g$である場合、冷却前の水溶液Aに溶けている$MgSO_4$の質量は何$g$か。
最も適当な数値を、次の①~⑥のうちから一つ選べ。
①$28$ ②$30$ ③$32$ ④$34$ ⑤$36$ ⑥$42$
※図は動画内参照
共通テスト追試 化学 2023年度 第1問 問3 質量モル濃度

単元:
#化学#化学理論#大学入試過去問(化学)#溶液の性質#共通テスト#理科(高校生)
指導講師:
ぺんぎん高校化学問題集
問題文全文(内容文):
電解質$AB_2$(式量 200)は水中で陽イオン$A^{2+}$と陰イオン$B^{-}$に完全に電離する。
この電解質$AB_2$と非電解質$C$(分子量 150)との混合物$0.50g$が水$100g$に完全に溶けた溶液を考える。
すべての溶質粒子$A^{2+},B^{-},C$を合わせた質量モル濃度が$0.050 mol/kg$であるとき、混合物中の電解質$AB_2$の含有率(質量パーセント)は何$%$か。
最も適当な数値を、次の①~⑤のうちから一つ選べ。
ただし、水溶液中では$A^{2+},B^{-},C$はそれぞれ単独の溶質粒子として存在するとし、電離以外の化学反応は起こらないものとする。
①$20$ ②$33$ ③$40$ ④$50$ ⑤$67$
この動画を見る
電解質$AB_2$(式量 200)は水中で陽イオン$A^{2+}$と陰イオン$B^{-}$に完全に電離する。
この電解質$AB_2$と非電解質$C$(分子量 150)との混合物$0.50g$が水$100g$に完全に溶けた溶液を考える。
すべての溶質粒子$A^{2+},B^{-},C$を合わせた質量モル濃度が$0.050 mol/kg$であるとき、混合物中の電解質$AB_2$の含有率(質量パーセント)は何$%$か。
最も適当な数値を、次の①~⑤のうちから一つ選べ。
ただし、水溶液中では$A^{2+},B^{-},C$はそれぞれ単独の溶質粒子として存在するとし、電離以外の化学反応は起こらないものとする。
①$20$ ②$33$ ③$40$ ④$50$ ⑤$67$
【違いをしっかり理解!!】固体・気体の溶解度(固液平衡・溶解度曲線・気液平衡・ヘンリーの法則)〔現役講師解説、高校化学、化学基礎、2023年度版〕

単元:
#化学#化学理論#溶液の性質#理科(高校生)
指導講師:
3rd School
問題文全文(内容文):
固体・気体の溶解度について解説します。
固液平衡・溶解度曲線・気液平衡・ヘンリーの法則
0:00 この1本で計算をマスター!
3:24 硝酸カリウムは水$100$gに、$27$℃で$40$g、$80$℃で$169$g溶ける。
$80$℃の飽和水溶液$200$gに含まれる硝酸カリウムは何gか?
5:10 硝酸カリウムは水$100$gに、$40$℃で$64$g、$25$℃で$38$g溶ける。
$40$℃の飽和水溶液$100$gを$25$℃に冷却すると、硝酸カリウムは何g析出するか?
6:32 塩化カリウムは水$100$gに、$10$℃で$30$g、$80$℃で$52$g溶ける。
$80$℃の飽和水溶液$200$gから水$80$gを蒸発させたとき、塩化カリウムは何g析出するか?
7:53 気体の溶解度
10:38 ヘンリーの法則のルール
11:11 押した分だけ溶ける!
11:30 体積は圧力によらず一定である
13:12 $0$℃、$1.01×10^5$Pa (標準状態)において、酸素は$1$Lの水に$44.8$mL溶ける。
$0$°C,$5.05×10^5$Paで、$1$Lの水に溶ける酸素は何g?
18:33 $0$℃、$1.01×10^5$Pa (標準状態)において、メタンは$1$Lの水に$56$mL溶ける。
$0$°C,$2.02×10^5$Paで、$5$Lの水に溶けるメタンは何g?
この動画を見る
固体・気体の溶解度について解説します。
固液平衡・溶解度曲線・気液平衡・ヘンリーの法則
0:00 この1本で計算をマスター!
3:24 硝酸カリウムは水$100$gに、$27$℃で$40$g、$80$℃で$169$g溶ける。
$80$℃の飽和水溶液$200$gに含まれる硝酸カリウムは何gか?
5:10 硝酸カリウムは水$100$gに、$40$℃で$64$g、$25$℃で$38$g溶ける。
$40$℃の飽和水溶液$100$gを$25$℃に冷却すると、硝酸カリウムは何g析出するか?
6:32 塩化カリウムは水$100$gに、$10$℃で$30$g、$80$℃で$52$g溶ける。
$80$℃の飽和水溶液$200$gから水$80$gを蒸発させたとき、塩化カリウムは何g析出するか?
7:53 気体の溶解度
10:38 ヘンリーの法則のルール
11:11 押した分だけ溶ける!
11:30 体積は圧力によらず一定である
13:12 $0$℃、$1.01×10^5$Pa (標準状態)において、酸素は$1$Lの水に$44.8$mL溶ける。
$0$°C,$5.05×10^5$Paで、$1$Lの水に溶ける酸素は何g?
18:33 $0$℃、$1.01×10^5$Pa (標準状態)において、メタンは$1$Lの水に$56$mL溶ける。
$0$°C,$2.02×10^5$Paで、$5$Lの水に溶けるメタンは何g?
【なぜ溶けるのかを理解!!】溶解(極性溶媒・無極性溶媒、親水基・疎水基)〔現役講師解説、高校化学、化学基礎、2023年度版〕

